Cum poate o ceașcă de cafea să ajute la tratarea cancerului? Cofeina, testată ca activator al terapiei CRISPR
Cafeaua este una dintre cele mai consumate băuturi din lume. Într-un laborator din Statele Unite, însă, cofeina, molecula responsabilă pentru efectul său stimulant, este analizată dintr-o perspectivă complet diferită: ca posibil mecanism de control al editării genetice.
O echipă de la Texas A&M Health explorează utilizarea cofeinei nu ca tratament în sine, ci ca semnal de activare pentru sisteme genetice programate anterior. La baza acestei abordări se află tehnologia CRISPR, un instrument utilizat pentru editarea precisă a ADN-ului.
La prima vedere, asocierea dintre cafea și editare genetică pare improbabilă. Nu este vorba despre proprietățile metabolice ale cafelei și nici despre un efect direct asupra celulelor tumorale. Ideea este mult mai tehnică: folosirea unei molecule familiare drept comutator pentru terapii genetice avansate.
CRISPR: instrumentul care a schimbat regulile jocului
Pentru a înțelege relevanța acestei idei, este necesar să revenim la mecanismul CRISPR. Tehnologia își are originea într-un mecanism natural de apărare al bacteriilor, care folosesc secvențe repetitive din ADN pentru a identifica și neutraliza material genetic viral. Adaptat pentru utilizare medicală, sistemul permite cercetătorilor să taie ADN-ul într-un punct extrem de precis.
O moleculă-ghid de ARN identifică secvența-țintă, iar enzima Cas9 acționează ca un bisturiu molecular. După realizarea tăieturii, celula își activează mecanismele proprii de reparare, iar în acel moment pot fi introduse modificări precum corectarea unei mutații, dezactivarea unei gene sau inserarea unei secvențe noi.
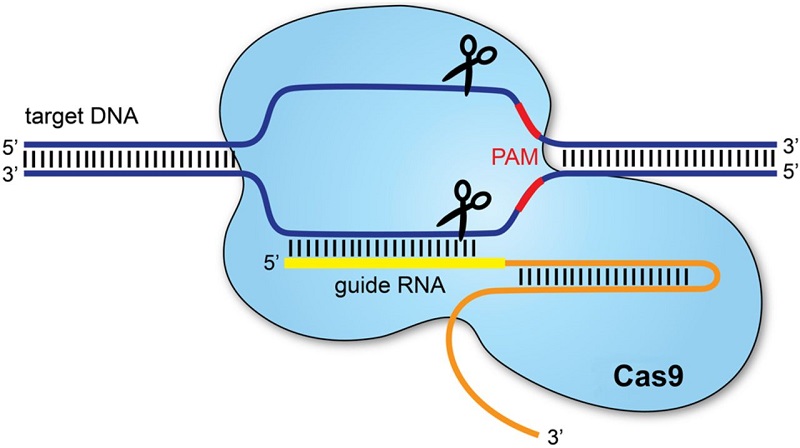
Această precizie a transformat CRISPR într-un instrument central al medicinei de precizie. Totuși, odată cu capacitatea de a modifica ADN-ul apare o întrebare esențială: cum poate fi controlată durata activării sistemului?
În terapiile genetice și celulare, timpul nu este un detaliu tehnic. O activare prelungită sau excesivă poate crește riscul reacțiilor adverse, inclusiv în cazul imunoterapiilor moderne. De aceea, cercetătorii caută metode prin care intervenția să fie nu doar precisă, ci și reglabilă în timp.
Caffebodies: un întrerupător inspirat din cafea
Pentru a introduce acest nivel suplimentar de control, echipa a dezvoltat un sistem bazat pe chemogenetică, adică modificarea celulelor astfel încât acestea să răspundă la o moleculă administrată din exterior.
Celulele sunt programate să producă, pe lângă mecanismul CRISPR, un nanocorp proiectat să reacționeze la cofeină. Acest nanocorp a fost denumit „caffebody”. În prezența cofeinei, caffebody-ul se leagă de o proteină parteneră, iar această apropiere fizică activează sistemul CRISPR.
În absența cofeinei, mecanismul rămâne inactiv. Când cofeina este prezentă în organism, chiar și în cantități moderate, ea funcționează ca semnal de pornire pentru editarea genetică.
Este esențial de precizat că cofeina nu editează ADN-ul și nu tratează direct boala. Rolul ei este exclusiv acela de întrerupător chimic într-un sistem genetic preconfigurat.

Control temporar, intervenție reversibilă
Un element care diferențiază această abordare este caracterul său temporar și reversibil. Activarea sistemului durează atât timp cât cofeina circulă în organism – de regulă câteva ore, în funcție de metabolism.
În plus, cercetătorii au demonstrat că mecanismul poate fi oprit prin administrarea rapamicinei, un medicament utilizat în prevenirea rejetului de organ. Rapamicina determină separarea proteinelor implicate și întrerupe activitatea sistemului genetic.
Rezultatul este un sistem cu dublu control: activare prin cofeină și dezactivare prin rapamicină. În contextul terapiilor genetice sau al imunoterapiilor, unde activarea excesivă poate declanșa reacții severe, această posibilitate de reglaj fin al intervenției poate avea implicații importante pentru siguranță.
De la laborator la posibile aplicații clinice
În prezent, cercetarea se află în fază preclinică. Totuși, aplicațiile potențiale sunt relevante.
În diabet, ar putea fi concepute celule modificate genetic pentru a produce insulină doar atunci când primesc un semnal extern. Cofeina ar putea funcționa ca declanșator temporar al secreției hormonale, oferind un control suplimentar asupra momentului activării.
În oncologie, aplicația ar putea viza terapiile CAR-T, în care celulele T ale pacientului sunt modificate genetic pentru a ataca tumora. Deși eficiente în anumite tipuri de cancer, aceste terapii pot produce reacții inflamatorii severe, generate de activarea intensă a sistemului imun.
Integrarea unui sistem bazat pe caffebodies ar putea permite controlul activității celulelor T: activare temporară, ajustarea intensității răspunsului sau întreruperea intervenției atunci când apar reacții adverse.
Nu este vorba despre simplificarea tratamentului, ci despre adăugarea unui mecanism suplimentar de siguranță într-o intervenție puternică.
Molecule familiare, roluri noi
Dincolo de detaliile tehnice, această cercetare reflectă o direcție mai amplă în medicina contemporană: reutilizarea unor molecule bine cunoscute pentru funcții complet noi.
Cofeina este una dintre cele mai studiate substanțe la nivel global. Rapamicina este utilizată de decenii în practica medicală. Profilul lor farmacologic este bine caracterizat. În acest context, ele nu devin tratamente în sine, ci semnale de control pentru terapii genetice sofisticate.
Această strategie de repurposing al unor compuși deja cunoscuți ar putea facilita, în timp, tranziția către aplicații clinice. În loc să fie dezvoltate exclusiv molecule complet noi pentru control, cercetătorii folosesc substanțe ale căror mecanisme sunt deja înțelese.
Mesajul central nu este că o cafea tratează cancerul. Miza reală este dezvoltarea unor terapii genetice controlabile, reversibile și reglabile în timp.
Dacă tehnologia CRISPR a făcut posibilă modificarea precisă a ADN-ului, sistemele bazate pe caffebodies adaugă o dimensiune suplimentară: controlul temporal al intervenției genetice.
Astfel, puterea unei terapii nu va fi definită doar de capacitatea de a interveni asupra genei potrivite, ci și de posibilitatea de a ajusta intervenția în funcție de contextul clinic. Iar uneori, acest control ar putea veni din molecule pe care le asociam, până acum, doar cu rutina zilnică.
Material redactat cu ajutorul AI, verificat și editat de echipa Raportul de Gardă, formată din specialiști în domeniul medical.

