Premiul Nobel pentru Chimie 2019: dezvoltarea acumulatorilor pe bază de ioni de litiu. Cine sunt laureații?
Al treilea premiu Nobel anunțat onorează descoperirile remarcabile din Chimie. Anul acesta a fost recunoscută dezvoltarea acumulatorilor cu ioni de litiu, datorată cercetătorilor John Goodenough, Stanley Whittingham și Akira Yoshino.

Inovația premiată anul acesta a contribuit decisiv atât la dezvoltarea tehnologiilor pe care le utilizăm zilnic (precum telefonul mobil sau laptopul), cât și la stocarea energiei din surse regenerabile (precum energia eoliană sau solară) sau la o autonomie mai mare a mașinilor electrice.
Cum funcționează bateriile litiu-ion?
Bateriile litiu-ion sunt disponibile pe piață din anul 1991, însă dezvoltarea lor a început din anii 1970.
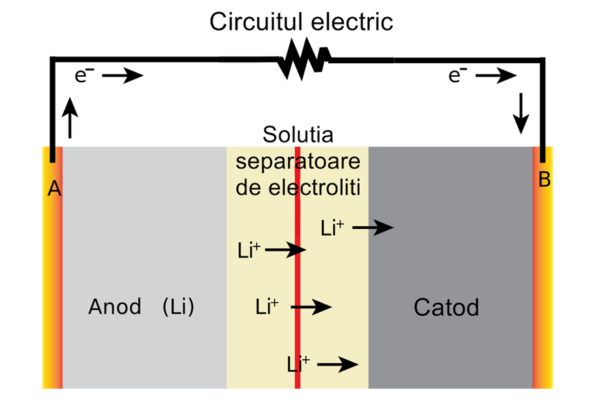
Sursa foto: Wikimedia Creative Commons (Sdk16420 CC BY-SA 4.0)
La fel ca bateriile precedente, bateriile litiu-ion sunt formate dintr-un anod, un catod și o soluție de electroliți între ele, cu rol de separare. Principiul pe care se bazează bateriile este diferența de potențial între anod și catod. Astfel, în momentul în care o baterie este introdusă într-un circuit electric, anodul eliberează electroni, care călătoresc prin circuit spre catod (astfel furnizând electricitate circuitului), iar prin intermediul conductorului, între anod și catod are loc o reacție chimică de oxidare-reducere.
Pe măsură ce bateria este utilizată iar anodul și catodul reacționează, diferența de potențial scade, iar bateria se consumă. În cazul bateriilor reîncărcabile, dacă sunt conectate la o sursă de electricitate, reacția se poate inversa, iar diferența de potențial între catod și anod este restabilită.
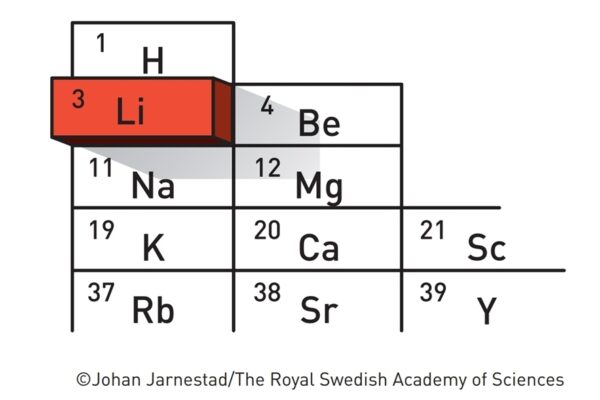
Litiul, descoperit în 1817, a fost considerat vreme îndelungată un potențial candidat pentru dezvoltarea bateriilor. În primul rând, este cel mai ușor metal, cu o densitate mai mică decât a apei, de 0.53 g/cm3. De asemenea, prezintă un potențial de reducere foarte scăzut, ceea ce înseamnă că manifestă o tendință pronunțată de a elibera electroni și de a se oxida (fiind astfel un component esențial al anodului).
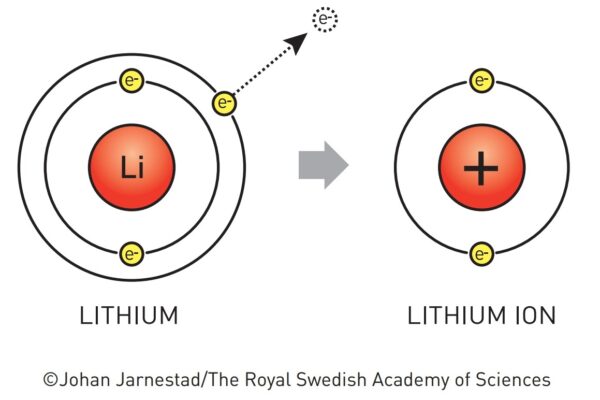
Astfel, poate conduce la dezvoltarea de baterii ușoare, care pot furniza cantități ridicate de energie. Dezavantajul acestui element chimic este reactivitatea chimică ridicată – nu poate intra în contact cu aerul sau cu apa fără reacții explozive. Acestea au fost caracteristicile litiului luate în calcul de cei trei laureați ai Premiului Nobel 2019.
Provocări și inovații
Povestea bateriilor be bază de litiu ne arată că, în știință, marile descoperiri sunt formate din inovații succesive, care vin drept răspuns la o nevoie reală și urgentă a societății.
În anii 1970, cercetătorii au tras un semnal de alarmă: petrolul, resursă esențială în numeroase industrii, este o resursă finită și trebuie folosită în mod echilibrat. De aceea, companiile petroliere au decis să investească în studiul altor surse de energie, rapid regenerabile și sustenabile. Astfel, în 1972, Stanley Whittingham a fost angajat de compania petrolieră Exxon.
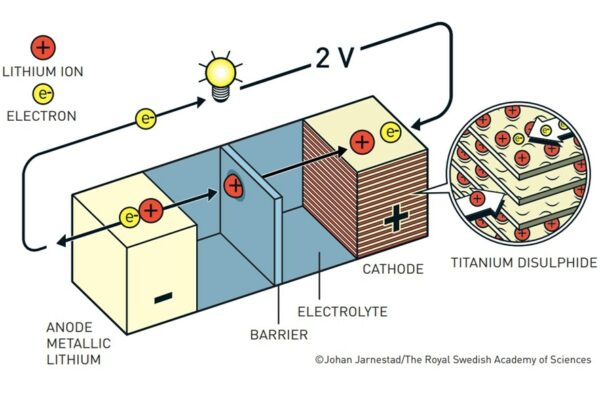
Acesta s-a concentrat pe dezvoltarea unei baterii cu anodul format din litiu metalic, iar catodul dintr-o substanță chimică cu structură lamelară – astfel, în timpul utilizării bateriei, reacția de oxidare-reducere conduce la formarea de ioni de litiu, care traversează soluția de electrolit până la catod, unde se intercalează printre straturile acestuia. În momentul încărcării bateriei, ionii de litiu parcurg drumul invers, iar structura lamelară a catodului rămâne neafectată.
Bateria dezvoltată de Whittingham utiliza un catod din sulfură de titan (TiS2) și înmagazina un voltaj de 2.5 V, o evoluție semnificativă față de bateriile clasice. De asemenea, nu se degrada după un număr ridicat de cicluri încărcare-descărcare.
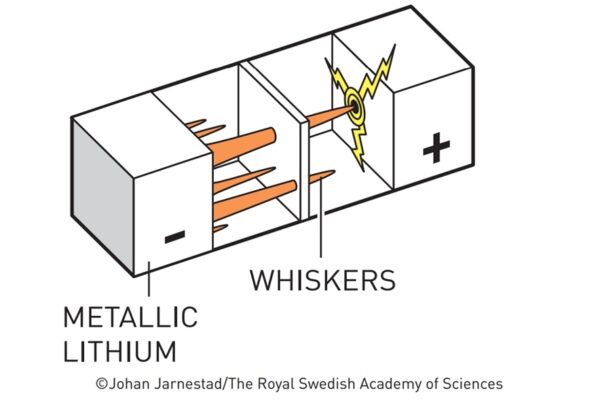
Acest prim model nu a rezolvat, însă, problema reactivității chimice a litiului: în interiorul bateriei se acumulează, în timp, precipitate liniare de litiu metalic, care cresc de la anod la catod, iar în momentul în care cele două sunt conectate, are loc un scurt-circuit cu un risc ridicat de explozie și incendiu. Această problemă a fost rectificată, iar bateria a fost produsă în cantități mici, începând cu anul 1976.
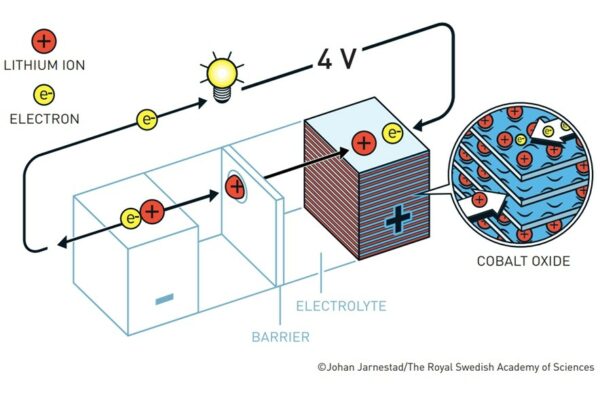
Următorul pas în direcția bateriilor moderne a fost făcut în 1980, de către John Goodenough. Acesta, împreună cu echipa sa, și-a concentrat cercetările pe ameliorarea structurii catodului. Astfel, sulfura de titan a fost înlocuită cu dioxidul de cobalt. Cele două substanțe au structuri lamelare înalt similare, însă ionul de oxigen, mai electronegativ decât ionul de sulf, contribuie la o diferență de potențial anod-catod mai mare. Astfel, bateria lui Goodenough era capabilă de voltaje de 4-5 V.
Ultima etapă spre dezvoltarea bateriilor comerciale pe bază de ioni de litiu a fost stimulată de nevoia industriei electronice japoneze pentru acumulatori ușori, puternici și stabili. În 1985, grupul de cercetare condus de Akira Yoshino, în cadrul companiei Asahi Kasei, a decis înlocuirea litiului metalic din anod cu o structură lamelară similară catodului.
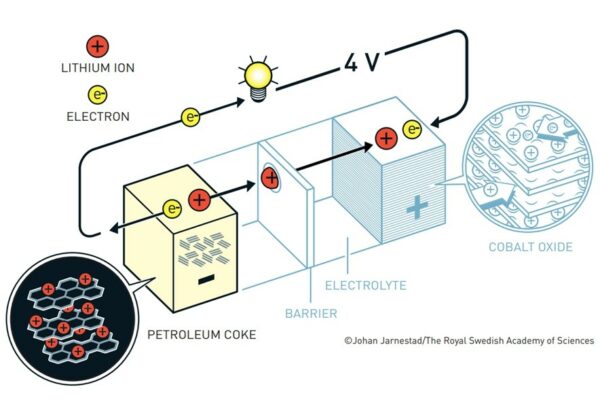
Aceștia au avut cele mai bune rezultate cu cocsul, o structură tridimensională, parțial cristalizată, formată din atomi de carbon și obținută prin prelucrarea petrolului. Astfel, litiul metalic, instabil și reactiv, a fost înlocuit cu litiul ionic, mult mai stabil, care călătorește între anod și catod rapid, de-a lungul a numeroase cicluri de încărcare-descărcare.
Această baterie, cu un voltaj de până la 4.1 V, a fost lansată pe piață în 1991 și a stat la baza dezvoltării electronice mobile de care ne bucurăm astăzi. Conceptul de baterie pe bază de ioni de litiu continuă să fie îmbunătățit – grupul de cercetare condus de Goodenough a propus noi structuri chimice catodice (fosfat de fier și oxid de mangan), cu o rezistență îndelungată la mai multe cicluri de încărcare-descărcare, fiind astfel mai sustenabilă și având un impact scăzut asupra mediului.
Despre laureați
Cei trei laureați de anul acesta ai Premiului Nobel pentru Chimie au contribuit în mod egal la dezvoltarea acumulatorilor cu litiu-ion, de aceea au împărțit premiul de 9 milioane de coroane suedeze.

John B. Goodenough s-a născut în 1922, în Jena, Germania. Acesta a absolvit studiile doctorale în 1952, la Universitatea din Chicago, SUA. Acesta este profesor la Universitatea din Texas, Austin, SUA și a contribuit la dezvoltarea bateriilor be bază de litiu în cadrul Universității Oxford. În acest moment, este cel mai în vârstă laureat al Premiului Nobel (97 de ani), depășindu-l pe laureatul Premiului Nobel pentru Fizică 2018, Arthur Ashkin.

Stanley Whittingham s-a născut în 1941, în Marea Britanie, și este profesor la Universitatea Binghamton, New York, SUA. A absolvit studiile doctorale în 1968 la Universitatea Oxford, Marea Britanie, și a efectuat cercetările premiate Nobel în cadrul laboratoarelor companiei Exxon.

Akira Yoshino s-a născut în 1948, în Suita, Japonia. Și-a realizat doctoratul la Universitatea Osaka și este profesor la Universitatea Meijo, din Nagoya, Japonia. Actualmente este Colaborator Onorific la Asahi Kasei Corporation, din Tokyo, unde a efectuat cercetările care au condus la prima baterie pe bază de ioni de litiu comercială.
Citește și:
- Premiul Nobel pentru Fiziologie și Medicină 2019: descifrarea mecanismelor prin care celulele detectează și răspund la variațiile oxigenului
- Premiul Nobel pentru Chimie 2018: aplicarea principiilor lui Darwin în eprubete și dezvoltarea de medicamente biologice în beneficiul întregii umanități
- Premiul Nobel pentru Medicină 2018. James Allison și Tasuku Honjo au deschis un nou domeniu în lupta cu cancerul: imuno-oncologia
Sursa foto: Medalia Premiului Nobel
© Nobel Media. Photo: Alexander Mahmoud

