De la Premiul Nobel la primul medicament: blocarea genelor patologice prin interferența ARN. Patisiran – primul medicament cu rezultate promițătoare
În 2006 Andrew Fire și Craig Mello câștigau premiul Nobel pentru Medicină pentru descoperirea tipurilor de ARN care permit inhibarea expresiei anumitor gene într-un proces numit ARNi (ARN interference). După 20 ani de cercetări ale aplicabilității acestui mecanism, pentru prima dată rezultatele unui studiu de fază 3 sunt încurajatoare și creează premisele apariției unei clase noi de substanțe. Alnylam, companie farmaceutică dedicată studierii ARNi, în parteneriat cu Sanofi, a dezvoltat medicamentul patisiran pentru tratarea polineuropatiei amiloide familiale (sau amiloidozei familiale cu transtiretină – ATTR), o boala genetică rară.
“ARNi are potențialul de a contribui la dezvoltarea uneia dintre cele mai mari clase de medicamente cu aplicabilitate largă după anticorpii monoclonali și proteinele recombinante.” – John Maraganore, Director Executiv la Alnylam
Patisiran a dovedit beneficii semnificative la pacienții cu ATTR. Acest tip de amiloidoză este o boala neurodegenerativă care determină pierderea progresivă a funcțiilor motorii. Substratul patologic este reprezentat de agregate de proteine care au la bază transtiretina (o proteină care transportă în ser și în lichidul cefalorahidian hormonul tiroidian T4 și retinolul) și care se depun la nivelul sistemului nervos periferic. Boala debutează între 20 și 40 de ani, iar speranța de viață este de 15 ani de la diagnostic.
Au fost înrolați în studiu 227 de pacienti cu amiloidoză familială cu transtiretină, reprezentând 39 de genotipuri. Două treimi dintre pacienți au primit 0,3 mg/kg patisiran intravenos, o dată la 3 saptămâni, timp de 18 luni. O treime a primit placebo. Rezultatele au fost semnificative din punct de vedere statistic pentru patisiran. S-a obținut un scor favorabil al gradului de dizabilitate produsă de polineuropatie. A fost atins și obiectivul secundar, îmbunătățirea calității vieții.
De asemenea, substanța s-a dovedit eficientă și în ceea ce privește forța musculară, viteza de deplasare și alți parametri care se evaluează la pacienții cu această formă de amiloidoză. Mai mult decât atât, profilul de siguranță s-a dovedit acceptabil. Rata mortalității a fost mai mare în grupul placebo – 7,8%, comparativ cu patisiran (4,7%).
Aceste date sunt încurajatoare, având în vedere eșecul a două studii anterioare care au evaluat alte medicamente – revusiran si fitusiran și au fost întrerupte din cauza reacțiilor adverse.
Drumul de la o inovație câstigatoare a premiului Nobel la dezvoltarea de medicamente
Craig Mello si Andrew Fire, profesori la universitatea din Massachusetts, au observat că în anumite cazuri o formă particulară de ARN determină distrugerea ARN-ului mesager înainte de a fi utilizat în sinteza proteinelor. Majoritatea medicamentelor funcționează prin inhibarea diferitelor proteine. Realizarea acestui proces prin blocarea genelor s-a dovedit o descoperire remarcabilă. Cei doi au publicat această descoperire în 1998, în revista Nature, iar în 2006 au primit premiul Nobel.

Alnylam Pharmaceuticals a fost fondată în 2002 cu scopul de cerceta modul în care noile molecule pot fi folosite pentru producerea de medicamente pe scară largă. Principala problemă a fost transformarea descoperirii într-un medicament fezabil, din moment ce simpla injectare determina distrugerea substanței atunci când ajungea în sânge. În 2012, Alnylam a investit 65 milioane de dolari în Arbutus Biopharma pentru obținerea unui medicament stabil.
Ce este ARNi și în ce domenii poate fi folosit?
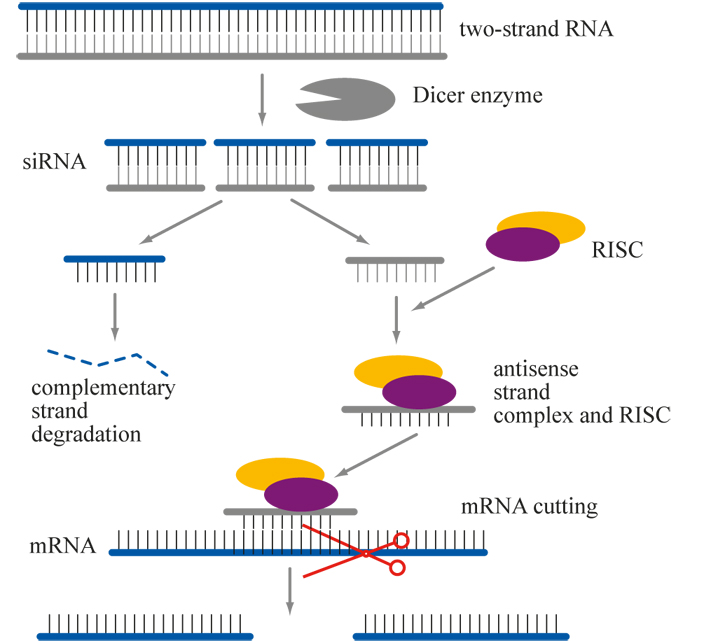
Două tipuri de acid ribonucleic (ARN) – microRNA și small interfering RNA – joacă un rol central în procesul de interferență ARN. Aceste molecule mici de ARN se pot lega de ARN-ul mesager, care conține gene ce urmează a fi traduse în proteine. Efectul este blocarea producției de proteine, mecanism numit și “gene silencing”.
ARNi are aplicabilitate extinsă în medicină, nu doar în ceea ce privește bolile rare. The Medicines Company a derulat studii care au evaluat un medicament împotriva hipercolesterolemiei, inclisiran. Acesta are ca țintă inhibarea sintezei proteinei PCSK9, cu rol în degradarea receptorilor pentru LDL – colesterol.
Oncologia este un alt domeniu unde se așteaptă rezultate promițătoare de la ARNi, însă există limitări mari legate de administrare și apariția reacțiilor adverse. În prezent se lucrează la obținerea unor nanoparticule care să permită administrarea optimă a acestei noi terapii. De asemnea, ARNi are implicații majore și în procesul de screening al cancerului.
Oamenii de știință de la Broad Institute of MIT and Harvard, alături de Institutul Dana-Faber, au lucrat la o “hartă” a vulnerabilității genetice asociată cancerului. Cu ajutorul ARNi au fost identificate peste 760 de gene de care multe tipuri de celule canceroase depind pentru a prolifera.
“Cel mai simplu lucru pe care îl putem face cu celulele canceroase este să le observam cum prolifereaza în timp și să le identificam pe cele care supraviețuiesc. Dacă celule pe care le-am modificat prin procesul de gene silencing dispar, înseamnă că acea gena era esențială pentru creșterea lor.” – David Root, director al Genetic Perturbation Platform de la The Broad Institute
Deși ARNi reprezintă un mecanism promițător pentru aplicații în industria farmaceutică, sunt necesare încă numeroase studii care să ateste în special profilul de siguranță al acestei potențiale clase de medicamente. O analiză genomică a arătat că rata de erori este de aproximativ 10%, acestea fiind atribuite în special efectelor off-target.
Următoarea animație ilustrează The Cancer Dependency Map dezvoltată de The Broad Institute of MIT and Harvard:

