Erleada, primul tratament aprobat de FDA care întârzie în medie cu 2 ani apariția metastazelor în cancerul de prostată rezistent la terapia hormonală
Food and Drug Administration (FDA) a aprobat săptămâna trecută medicamentul apalutamida (Erleada), care a primit anterior statut prioritar, pentru pacienții cu cancer prostatic fără metastaze, rezistent la castrare.
Erleada scade riscul de metastaze sau mortalitatea cu 72% comparativ cu placebo și crește rata medie de supraviețuire fără metastaze cu mai mult de doi ani.
Această aprobare marchează o premieră, deoarece s-a utilizat ca obiectiv primar rata de supraviețuire fără metastaze în studiul SPARTAN care a stat la baza deciziei FDA. Agenția demonstrează, astfel, că pentru a grăbi accesul pacienților la cele mai bune terapii ia în considerare alte abordări ale studiilor clinice, punând accentul pe noi criterii.
„Nevoia de a întârzia apariția metastazelor este critică în cazul cancerului de prostată. Aproape 90% dintre pacienții cu cancer de prostată rezistent la castrare vor dezvoltă metastaze osoase, moment în care prognosticul se înrăutățește semnificativ” – Dr. Mathai Mammen, Janssen Research & Development
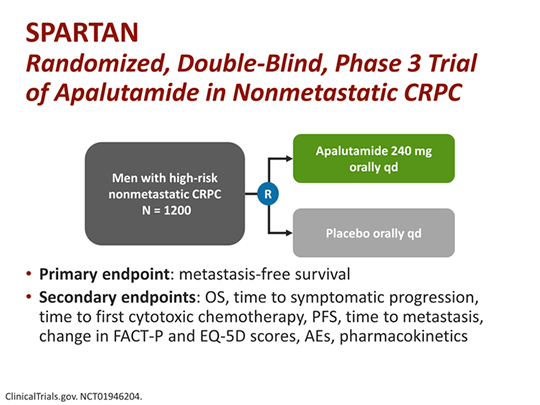
Principalele rezultate ale studiului SPARTAN:
- Erleada reduce cu 72% riscul de metastaze sau deces
- Între Erleada și placebo există o diferență de 24,31 luni în ceea ce privește supraviețuirea medie fără metastaze
- Timpul până la apariția metastazelor a fost de 40,51 luni pentru Erleada și de 17 luni pentru pacienții care au primit placebo
- Rata de supraviețuire fără progresie a bolii este de 40,51 în grupul care a primit Erleada și de 14,72 în grupul cu placebo
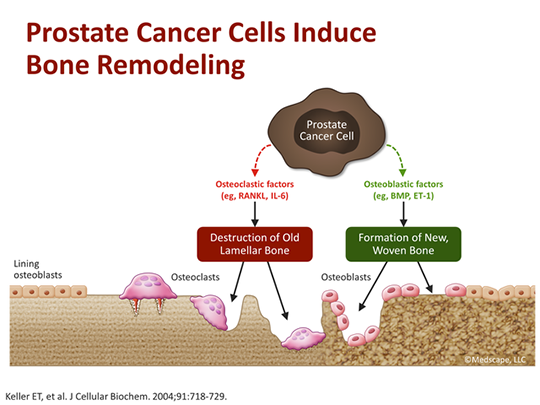
Conform National Cancer Institute (NCI), cancerul de prostată este al doilea tip de cancer ca frecvență la bărbați în Statele Unite. În 2017 au fost diagnosticați peste 160.000 de bărbați și se estimează ca aproximativ 26.000 vor muri din această cauză. Între 10 și 20% dintre cancerele de prostată sunt rezistente la castrare și în jur de 16% dintre pacienții cu acest diagnostic nu prezintă dovezi ale unei diseminări a procesului neoplazic la momentul stabilirii rezistenței la castrare.
Rata de supraviețuire la 3 ani pentru pacienții cu cancer prostatic avansat este de 30%.
Prin cancer prostatic non-metastatic rezistent la castrare se face referirea la un stadiu al bolii în care pacientul nu mai răspunde la tratamentul medical sau chirurgical prin care se încearcă scăderea testosteronului, dar nici nu s-au descoperit încă metastaze prin tehnici imagistice. În acest stadiu, pacienții prezintă valori crescute ale antigenului specific prostatic (PSA) deși se află pe terapie de deprivare androgenică și au valori ale testosteronului seric sub 50 ng/dl.
Erleada funcționează prin blocarea receptorilor de androgeni, hormoni din care categorie face parte și testosteronul, care susține creșterea tumorală. Medicamentul inhibă translocația nucleară a receptorului și determină scăderea proliferării celulelor tumorale și reducerea volumului tumoral.
Siguranța și eficacitatea medicamentului au fost stabilite printr-un studiu clinic randomizat de fază 3, SPARTAN, care a fost publicat în New England Journal of Medicine și a fost prezentat în cadrul Simpozionului ASCO pentru Cancere Genitourinare, desfășurat la San Francisco.
1.207 pacienți cu cancer prostatic non-metastatic, rezistent la castrare au fost incluși în studiu și li s-a administrat fie Erleada fie placebo. Toți pacienții au fost tratați concomitent cu hormonoterapie, fie terapie cu analog de hormon eliberator de gonadotropina (GnRH) sau prin castrare chirurgicală având ca scop scăderea nivelului de testosteron.
Eficacitatea medicamentului a fost stabilită în urma unor rezultate semnificative obținute din evaluarea obiectivelor secundare:
- timpul până la apariția metastazelor
- rata de supraviețuire fără progresie a bolii
- timpul până la progresia simptomatică
Rata de supraviețuire medie fără metastaze a fost de 40,5 luni pentru pacienții care au primit Erleada comparativ cu 16,2 în cazul pacienților care au primit placebo.
Erleada scade riscul de metastaze sau mortalitatea cu 72% și îmbunătățește rata de supraviețuire fără metastaze cu mai mult de doi ani.
FDA folosește mai multe criterii pentru a cuantifica eficacitatea unui medicament, acestea reprezentând obiectivele studiilor pe baza cărora se aprobă diferite substanțe. În cazul acestui studiu, pentru prima dată s-a luat în considerare în cadrul deciziei de aprobare supraviețuirea fără metastaze, măsurându-se durata de timp în care tumora nu s-a răspândit în alte părți ale organismului sau cuantificând mortalitatea după debutul tratamentului.
Pentru a asigura un acces mai rapid al pacienților la medicamente moderne, FDA își schimbă constant mecanismele prin care sunt realizate studiile, precum și criteriile de aprobare.
„Pe măsură ce impactul cancerului de prostată continuă să crească, ne amintim în fiecare zi cât este de importante sunt opțiunile terapeutice care le pot oferi pacienților șansa de a supraviețui mai mult. Aprobarea această înseamnă că bolnavii de cancer prostatic non-metastatic, rezistent la castrare au de acum o posibilitate de tratament care le oferă noi speranțe.” – Dr. Mark Scholz, Director al Prostate Cancer Research Institute
Articole similare
- #ASCO2017: Abiraterona – mai sigură și la fel de eficientă ca docetaxel la pacienții cu cancer de prostată metastatic, de grad înalt
- #ASCO2017: Abiraterona ar putea deveni prima linie de tratament în cancerul de prostată avansat
- #Dr. Karim Fizazi: abiraterona, mai sigură decât chimioterapia la bolnavii de cancer de prostată metastatic

