UPDATE. Începe programul de vaccinare în masă din Marea Britanie, iar prima persoană care primește vaccinul Pfizer/BioNTech este Margaret Keenan, o femeie în vârstă de 90 de ani. Citiți detalii despre prospectul publicat de guvernul britanic
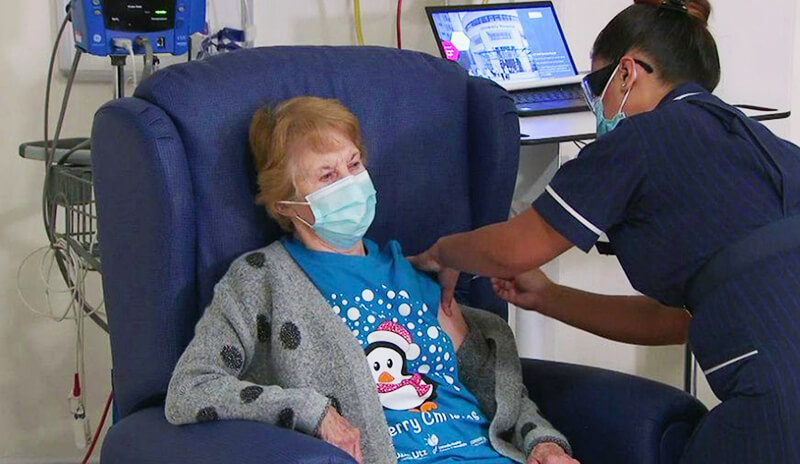
UPDATE 8 decembrie 2020. Prima persoană din lume care a primit vaccinul Pfizer/BioNTech în afara unui studiu clinic este Margaret Keenan, o femeie în vârstă de 90 de ani, din Irlanda de Nord. La mai puțin de o săptămână de la aprobarea condiționată a vaccinului, începe programul de vaccinare în masă din Marea Britanie.
„Mă simt atât de privilegiată să fiu prima persoană vaccinată împotriva Covid-19, este cel mai bun cadou timpuriu pentru ziua de naștere pe care mi l-aș putea dori pentru că înseamnă că pot în sfârșit să petrec timp cu familia și prietenii în noul an, după ce am fost singură pentru cea mai mare parte a anului”, a declarat Margaret Keenan pentru BBC News.
Prospectul vaccinului Pfizer/BioNTech împotriva COVID-19 a fost publicat de guvernul britanic. Ce conține vaccinul și care sunt indicațiile?
UPDATE. 03 Decembrie 2020. Guvernul britanic a publicat prospectul pentru vaccinul COVID-19, BNT162b2, produs de Pfizer/BioNTech, primul vaccin de tip ARN mesager aprobat de o autoritate de reglementare din lume, în regim de urgență. Conform datelor oficiale, acesta poate fi administrat adulților și adolescenților începând cu vârsta de 16 ani.
Principala substanță din compoziția vaccinului este ARNm care codifică proteina spike din structura virusului SARS-CoV-2. Vaccinul determină producția de anticorpi în organism și stimulează celulele imune să ofere protecție împotriva bolii COVID-19. Moleculele de ARNm sunt asamblate în nanoparticule lipidice și administrate în organismul uman prin injecție intramusculară, în două doze, la un interval de 21 de zile.
Vaccinul trebuie să fie stocat la temperaturi de -80°C până la -60 °C, în ambalajul original pentru a fi ferit de lumină.
Se recomandă administrarea cu precauție pentru anumite categorii de persoane, la indicația medicului:
- Persoanele care au raportat anumite probleme precum reacții alergice sau probleme respiratoria în urma administrării vaccinului ARNm BNT162b2;
- Cei cu afecțiuni severe, cu febră mare. Febra ușoară sau o infecție ușoară de căi aeriene superioare nu reprezintă contraindicații pentru vaccinare.
- Persoanele imunosupresate, cum ar fi cei care au infecție HIV sau care urmează un tratament care determină imunosupresie ar trebui să consulte medical înainte de a primi vaccinul;
- Persoanele care au tulburări de coagulare a sângelui sau care urmează tratament anticoagulant.
Nu există încă date privind utilizarea în sarcină. Vaccinul nu este indicat la femeile însărcinate și se recomandă evitarea unei sarcini pentru cel puțin 2 luni după a doua doză de vaccin.
Ca toate vaccinurile, BNT162b2 poate provoca reacții adverse. Cele mai multe dintre acestea sunt ușoare sau moderate și dispar în câteva zile.
- Reacțiile adverse frecvente (pot afecta mai mult de o persoană din 10) includ: durere la locul injectării, oboseală, cefalee, durere musculară, frisoane, dureri articulare, febră.
- Reacțiile adverse care pot afecta cel mult o persoană din 10: tumefacția sau înroșirea zonei în care se realizează injecția, greața.
- Reacții adverse rare (pot afecta o persoană din 100): mărirea ganglionilor limfatici, stare generală alterată.
Mai multe informații despre compoziția vaccinului pot fi găsite în prospect. De asemenea, a fost publicat documentul cu informații dedicate personalului medical.
Vaccinul împotriva COVID-19, de tip ARNm, realizat de Pfizer/BioNTech a primit aprobare pentru utilizare în regim de urgență în Marea Britanie. Campania de imunizare va începe săptămâna viitoare, conform declarațiilor Secretarului de Stat Matt Hancock.
Guvernul britanic a acceptat recomandările comitetului MHRA (Medicines and Healthcare products Regulatory Agency), care a validat datele care arată că vaccinul îndeplinește standardele de eficiență, siguranță și calitate. JCVI, Comitetul pentru Vaccinare și Imunizare, urmează să publice recomandările pentru categoriile de populației prioritare pentru vaccinare, care ar trebui să includă grupurile vulnerabile: persoanele vârstnice, cele instituționalizate, personalul medical, anumite categorii de persoane cu boli cronice. 10 milioane de doze de vaccin se așteaptă să ajungă în Marea Britanie până la finalul anului.
Help is on its way.
The MHRA has formally authorised the Pfizer/BioNTech vaccine for Covid-19.
The NHS stands ready to start vaccinating early next week.
The UK is the first country in the world to have a clinically approved vaccine for supply.
— Matt Hancock (@MattHancock) December 2, 2020
În urma analizei finale a studiului de fază III, Pfizer a anunțat că vaccinul de tip ARN BNT162b2 este eficient în 95% din cazuri împotriva COVID-19, începând cu 28 de zile după prima doză. Eficacitatea a fost similară indiferent de vârstă, sex, rasă și etnie. În cazul adulților în vârstă de peste 65 de ani, eficacitatea vaccinului a fost de peste 94%. Vaccinul a fost bine tolerat de participanții la studiu, fără a ridica probleme legate de siguranță.
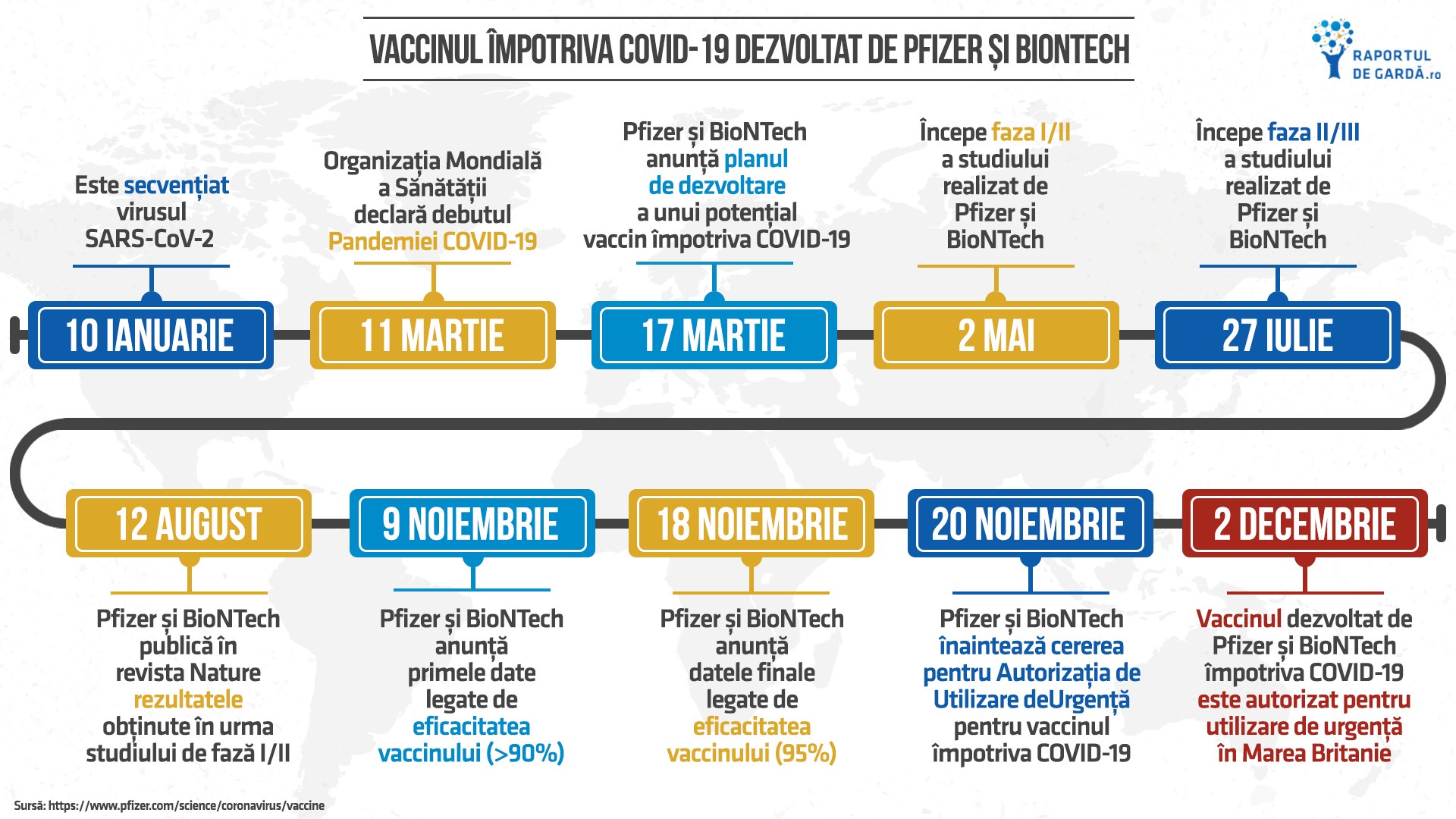
Aprobarea din Marea Britanie reprezintă un alt moment istoric în lupta împotriva pandemiei COVID-19. La doar o lună de la apariția primelor cazuri, genomul noului coronavirus a fost secvențiat. Chiar înainte de publicarea genomului, primele variante de teste pentru diagnostic erau realizate, pe baza experienței anterioare cu alte tipuri de coronavirusuri. La mai puțin de un an de la declararea pandemiei, primul vaccin este deja aprobat în regim de urgență de o autoritate de reglementare și alte tipuri de vaccinuri se află în stadii avansate ale studiilor clinice.

Vaccinul Pfizer/BioNTech este primul vaccin aprobat care folosește tehnologia ARN mesager. Pentru a declanșa un răspuns imun vaccinurile clasice implică introducerea unui virus atenuat în organism sau a unor proteine virale. Vaccinurile de tip ARNm aduc o nouă abordare: introducerea unui fragment de material genetic (ARN) care codifică o proteină virală. Vaccinul Pfizer/BioNTech se bazează pe utilizarea unei molecule de ARNm care care codifică o parte a proteinei spike ce se găsește pe suprafața SARS-CoV-2. Odată ce materialul genetic intră în celulele umane acestea pot produce proteina de interes, față de care va apărea un răspuns imun. Materialul genetic nu pătrunde în nucleul celulei și este distrus după ce setul de instrucțiuni a contribuit la producerea fragmentului viral.
Mecanismele clasice de producere a vaccinurilor implică etape care durează perioade lungi, și nu pot răspunde unei crize de sănătate publică precum pandemia actuală. Unul dintre avantajele vaccinurilor de tip ARNm este că procesul de producție poate fi standardizat și produs rapid pe scară largă.
„Credem că derularea programului de vaccinare din Marea Britanie va reduce numărul persoanelor la risc înalt spitalizate. Scopul nostru e să aducem un vaccin sigur și eficient la persoanele care au nevoie de el. Datele prezentate autorităților de reglementare din întreaga lume sunt rezultatul unui program riguros și etic de cercetare” – Ugur Sahin, CEO BioNTech
Toate acestea au fost posibile datorită progreselor tehnologiei, dezvoltării domeniului genomicii, dar și a concentrării eforturilor lumii științifice, deschiderii către colaborare și împărtășire a datelor.
Deși disponibilitatea unui vaccin reprezintă un pas esențial pentru limitarea răspândirii infecției cu noul coronavirus, nu trebuie uitat faptul că finalizarea pandemiei depinde de mai mulți factori. Oficialii britanici au atras atenția asupra acestui fapt:
„Pentru a contribui la succesul programului de vaccinare este vital ca fiecare persoană să respecte în continuare restricțiile necesare din zona în care se află pentru a limita răspândirea virusului și pentru a permite ca NHS să își desfășoare activitățile fără a suprasolicita sistemul” – Department of Health and Social Care
Companiile farmaceutice Pfizer și BioNTech au trimis către FDA (Food and Drug Administration) și Agenția Europeană a Medicamentelor (EMA – European Medicines Agency) solicitările de obținere a Autorizației de Utilizare de Urgență pentru vaccinul împotriva COVID-19. În condițiile aprobării cererii, vaccinul va putea fi administrat primilor cetățeni americani și europeni înainte de sfârșitul lunii decembrie 2020.
EMA organizează o întâlnire publică cu părțile implicate în dezvoltarea și autorizarea vaccinurilor împotriva SARS-CoV-2, în cadrul unui eveniment difuzat live la data de 11 decembrie 2020.
Citește și:
- Esențial COVID-19: cele mai importante știri ale săptămânii. Pfizer a înaintat către FDA cererea de autorizare a utilizării de urgență pentru vaccinul SARS-CoV-2
- Bătălia #COVID19 în laborator. Pfizer și BioNTech au primit aprobarea FDA pentru accelerarea dezvoltării a două vaccinuri împotriva SARS-CoV-2
- Esențial COVID-19: cele mai importante știri ale săptămânii. Aprobarea FDA de urgență a bamlanivimab și ghidul EMA de monitorizare a vaccinurilor

