#EHA2020. Terapia CAR-T Liso-Cel induce o rată generală de răspuns de 89% în limfomul non-Hodgkin cu celule B recidivant sau refractar
Tratamentul CAR-T lisocabtagene maraleucel (Liso-Cel) conduce la rate mari de răspuns în cazul pacienților cu limfom non-Hodgkin cu celule B mari recidivant sau refractar, determinând răspunsuri durabile complete la pacienții care prezintă un prognostic nefavorabil. Acestea sunt noile date provenite din studiul de fază II, TRANSCEND-PILOT, prezentate în cadrul celui de-al 25-lea Congres Anual al Asociației Europene de Hematologie.
Rezultatele pun în evidentă următoarele:
- O rată generală de răspuns de 89%, toți pacienții obținând un răspuns obiectiv până în ziua 30;
- Rată de răspuns complet (RC) de 56%, iar 10 din 12 pacienți care aveau un RC la cel puțin o evaluare ulterioară au rămas cu RC;
- Răspunsurile parțiale (RP) au fost observate la 33% dintre pacienți iar 2 pacienți au prezentat RP care a putut fi convertit într-un RC;
- Probabilitatea de răspuns continuu (măsurată cu ajutorul instrumentului statistic Kaplan-Meier) a fost de 63% la 3 luni și 53% la 6 luni.
„Studiul de fază 2, PILOT, este primul studiu care evaluează siguranța și eficacitatea unui tratament de tip CAR-T ca terapie de linia a doua pentru pacienții cu limfom non-Hodgkin agresiv cu celule B mari, pacienți care sunt considerați candidați slabi pentru transplant din cauza profilului foarte fragil, al comorbidităților asociate și care prezintă un prognostic nefavorabil.”- a declarat co-autorul studiului dr. Nilanjan Ghosh, director al Programului, din cadrul Institutului de Oncologie Levine, Atrium Health.
Pacienții cu limfom non-Hodgkin cu celule B mari recidivant sau refractar agresiv pot, în urma chimioimunoterapiei de primă linie, să obțină vindecarea, dacă răspund la chimioterapie și sunt eligibili pentru a urma transplantatul autolog de celule stem. Din păcate, doar un procent mic dintre pacienți sunt capabili să finalizeze cu succes tratamentul, acest lucru fiind cauzat de caracteristicile prognostice slabe care determină rezistența la chimioterapie sau alte comorbidități asociate care ar putea reduce toleranța pacienților la o abordare terapeutică mai agresivă, de intensitate ridicată.
Mai mult decât atât, dr. Ghosh a subliniat fapul că în momentul actual nu există un standard de îngrijire pentru pacienții care nu sunt eligibili pentru transplant sau care nu pot primi chimioterapie în doze ridicate, lăsând această categorie a populației de pacienți cu o nevoie semnificativă neacoperită.
„Știm din studiile raportate anterior că terapia CAR-T a arătat răspunsuri durabile la pacienții cu limfom non-Hodgkin cu celule B mari recidivant sau refractar în linia a treia sau alte linii de tratemanent. Acest lucru a furnizat motivele pentru a explora eficacitatea și siguranța liso-cel în linia a doua la pacienții care prezintă recidivă sau sunt refractari, cu alte cuvinte, pentru candidații neeligibili sau cu o rată probabilă de succes a transplantului scăzută.”- a menționat dr. Ghosh.
Despre studiu
Studiul de faza 2, TRANSCEND-PILOT, a inclus pacienți cu vârsta medie de 72 de ani (86% având peste 65 de ani), 62% dintre aceștia au fost de sex masculin. Aceștia au urmat procesul de leucafereză după care terapia a fost implementată. Pacienții cu limfom difuz cu celule mari, limfom cu celule B cu creștere rapidă (grad înalt) sau limfom folicular de grad 3B au fost eligibili pentru începerea tratamentului.
Condițiile de includere în studiu menționau că pacienții aveau în antecedente linii de terapie constând în chimioterapie cu compuși din clasa antraciclinelor și un agent țintit antiCD20 și erau, în plus, neeligibili pentru chimioterapia în doze mari, urmată de transplant. De asemenea, a fost necesar să îndeplinească cel puțin una sau mai multe criterii de neeligibilitate pentru transplant.
Criteriile de neeligibilitate pentru transplant au inclus (62% dintre pacienți au îndeplinit 2 sau mai multe criterii):
- vârsta de ≥70 de ani;
- statutul de performanță ECOG de 2 (statusurile de performanță ECOG- Eastern Cooperative Oncology Group sunt criterii folosite de medici și cercetători pentru a evalua modul în care boala unui pacient progresează și afectează abilitățile zilnice ale pacientului, determinând astfel tratamentul și prognosticul adecvat);
- clearance-ul creatininei mai mare de 30 și mai mic de 60 mL/min/1,73 mp.
Scopul principal al studiului a fost de a identifica rata generală de răspuns, iar punctele secundare cheie au inclus efecte adverse (EA), rata completă de raspuns, durata răspunsului, supraviețuirea generală și lipsită de progresia bolii, farmacocinetica, modificările testelor de laborator și calitatea vieții.
„O altă modalitate pentru a evalua comorbiditățile este scorul HCT-CI (hematopoietic stem cell transplantation comorbidities index) care poate prezice mortalitatea non-recidivă [N.A. NRM-non-relapse mortality after transplantation – termenul este folosit frecvent în literatura de specialitate și este definit ca deces fără recidivă. Moartea care a avut loc după recidivă a fost întotdeauna atribuită bolii]. S-a demonstrat în studiile anterioare că subiecții care au un scor de 3 sau mai mare au un risc mai mare de mortalitate non-recidivă. În studiul nostru, scorul HCT-CI median a fost de 3, cu 52% dintre pacienți cu un scor de 3 sau mai mare, ceea ce indică din nou o populație cu risc ridicat.”- a adăugat dr. Ghosh.
Despre siguranță și reacții adverse
În ceea ce privește siguranța, s-a constatat că terapia liso-cel are un profil de toxicitate acceptabil. Au fost raportate reacții adverse (de orice fel) asociate tratamentului la 86% dintre pacienți și 69% au fost gradul 3-4 de severitate, iar 3% au fost de gradul 5.
Reacții adverse asociate tratamentului au inclus: oboseală (34,5%), neutropenie (34,5%), anemie (28%), leucopenie (24%), sindromul de eliberare de citokine (21%), limfopenie (21%), trombocitopenie (21%), tuse (17%), hipotensiune arterială (17%) și greață (17%).
„Aceste date susțin evaluarea suplimentară a liso-cel în tratamentul de linia a doua pentru pacienții cu limfom non-Hodgkin cu celule B mari recidivant sau refractar, care nu sunt candidați pentru transplantul de celule stem.”- a concluzionat dr. Ghosh.
Despre limfomul difuz cu celule B mari
Limfomul difuz cu celule B mari (DLBCL- Diffuse large B-cell lymphoma) este cel mai frecvent și cel mai agresiv tip de limfom non-Hodgkin (LNH), reprezentând trei din cinci cazuri diagnosticate. Aproximativ o treime din pacienții prezintă o recidivă după ce au primit tratamentul de primă linie și aproximativ 10% au boală refractară.
Potrivit datelor actuale, speranța de viață mediană pentru pacienții care recidivează sau sunt refractari la standardul actual de tratament de îngrijire, după mai multe linii de terapie, este de aproximativ șase luni.
Despre liso-cel
Lisocabtagene maraleucel (liso-cel) reprezintă o terapie CAR-T direcționată contra CD19 (glicoproteină de suprafață exprimată în timpul dezvoltării normale a celulelor B și menținută în urma transformării maligne a acestora).
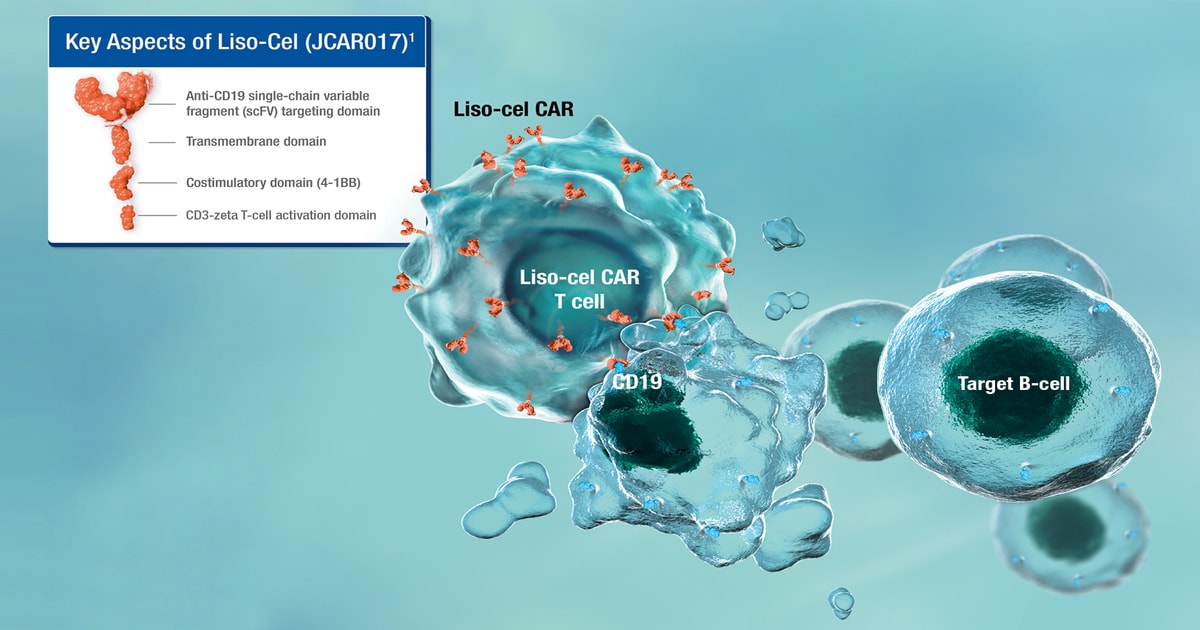
Celulele CAR-T Liso-cel urmăresc să țintească celulele care exprimă CD19 printr-o construcție CAR (de tip receptor himeric antigenic) care include un fragment cu un singur lanț variabil anti-CD19, domeniu care țintește și care are rol în specificitatea antigenului, un domeniu transmembranar, un domeniu costimulator 4-1BB pentru a crește proliferarea și persistența celulelor T și un domeniu de activare a celulelor T CD3-zeta. Compoziția definită de celule CAR T CD4 + și CD8 + din liso-cel poate limita variabilitatea produsului; cu toate acestea, semnificația clinică a compoziției definite nu este cunoscută.
În mai 2020 FDA a prelungit cu trei luni data pentru cererea de licență biologică pentru lisocabtagene maraleucel (Liso-cel) pentru tratamentul adulților cu limfom non-Hodgkin cu celule B refractar sau recidivant după cel puțin două linii anterioare de terapie .
Citește și:
- #EHA2020. Ruxolitinib, rate înalte de răspuns în boala grefă-contra-gazdă acută, pentru mai multe categorii de pacienți refractari la steroizi
- #EHA2020. Adulții cu anemie falciformă au risc crescut de evoluție severă în cazul infecției COVID-19
- #AACR20. COVID-19 la pacienții oncologici: riscul de evoluție severă este de 9 ori mai mare în cazul cancerelor hematologice

