FDA aprobă primul test de biopsie lichidă care utilizează tehnologia NGS pentru diagnosticul cancerului pulmonar cu mutații EGFR
Administrația Alimentelor și Medicamentelor din SUA (FDA) a aprobat un nou test diagnostic al mutației EGFR la nivelul tumorilor pulmonare metastatice, non-microcelulare (NSCLC). Acesta este primul test companion care utilizează două tehnologii inovative în diagnosticul mutațiilor care pot declanșa cancerul: biopsia lichidă (identificarea ADN-ului neoplazic dintr-o probă de sânge) și next-generation sequencing (NGS, analiza rapidă a întregului genom și identificarea simultană a mai multor mutații posibile).
Testul aprobat spre utilizare, denumit Guardant360 CDx și produs de Guardant Health, poate fi utilizat pentru detecția mutației EGFR în cancerul pulmonar non-microcelular metastatic, și pe baza rezultatului pozitiv pacientului i se poate indica tratamentul țintit osimertinib (denumire comercială Tagrisso).
“Aprobarea unui test diagnostic companion care utilizează atât biopsia lichidă, cât și secvențierea genomică de nouă generație, anunță o nouă eră în testele pentru prezența mutațiilor. Pe lângă avantajul unei testări minim invazive, pacienții vor beneficia și de identificarea simultană a mai multor mutații. Spre deosebire de testarea mutațiilor una câte una, acest model diagnostic conduce la rezultate relevante într-un timp mai scurt, ceea ce permite debutul terapiei potrivite mai rapid, și poate aduce indicii prețioase în ceea ce privește rezistența la tratament,” afirmă dr. Tim Stenzel, director al Departamentului de Diagnostic in vitro și radiologic, din cadrul FDA.
Acest test diagnostic a primit statutul de Dispozitiv Inovator (Breakthrough Device) din partea FDA, care a oferit consultanță în ceea ce privește cel mai rapid și eficient proces de dezvoltare a testului și de obținere a aprobării.

Rezultatele Guardant360 CDx au fost confirmate de o serie de studii clinice: într-un studiu prospectiv asupra a 323 de pacienți cu NSCLC metastatic, adăugarea biopsiei lichide la biopsia clasică a crescut rata de detecție a unei mutații acționabile de la 20,5% la 35,8%. Mai mult, studiul NILE a demonstrat o concordanță de peste 98,2% între Guardant360 CDx și biopsia clasică, cu o valoare predictivă pozitivă de 100%, în detecția a patru mutații acționabile din cadrul NSCLC (EGFR, ALK, ROS1, BRAF). În plus, biopsia lichidă a condus la rezultate mai rapid cu aproximativ o săptămână.
Despre biopsia lichidă și NGS
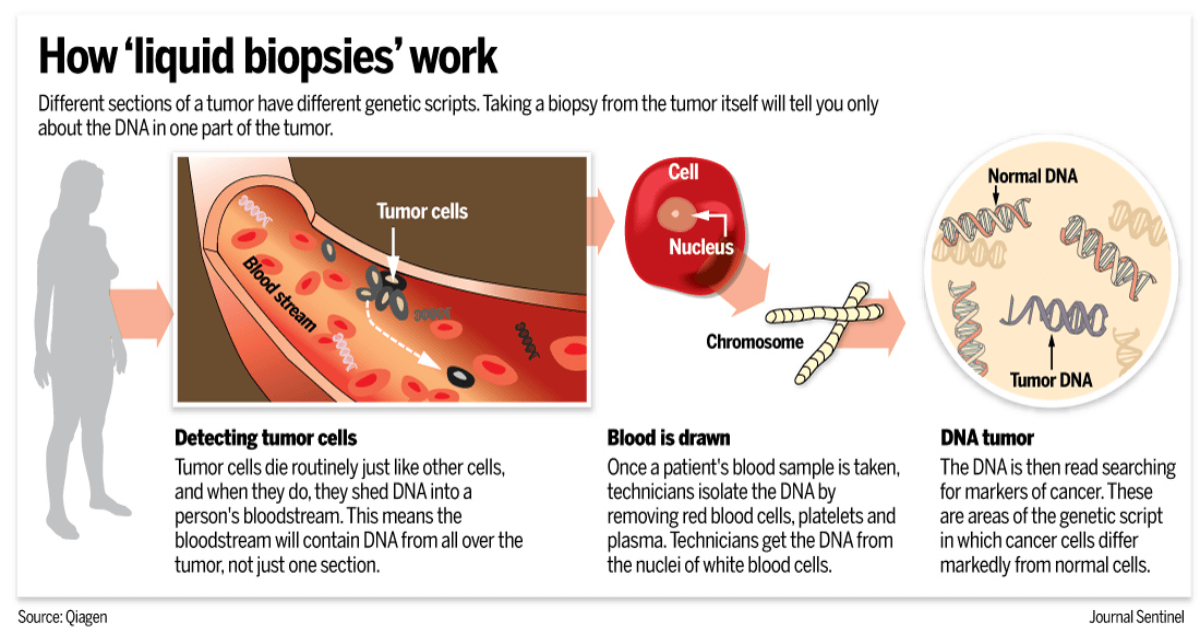
Biopsia lichidă reprezintă un pas înainte important în domeniul diagnosticului oncologic, deoarece permite identificarea ADN-ului tumoral la nivelul unei probe de sânge prelevate de la pacient. Tot mai multe studii aduc argumente în privința eficienței acestui procedeu, care prezintă o serie de avantaje: este mai puțin invaziv decât biopsia clasică, poate fi repetat în mod mai facil și poate reprezenta chiar singura modalitate de a diagnostica tumora, în cazul în care aceasta este localizată într-o regiune inaccesibilă biopsiei.
Tehnologia NGS implică secvențierea simultană a întregului genom tumoral și identificarea rapidă a mai multor mutații posibile, care pot fi țintite în mod specific cu ajutorul noilor terapii. Avantajul NGS este că materialul tumoral necesar este de obicei redus cantitativ și permite testarea mai multor modificări genetice pentru a detecta pacienții care pot beneficia de terapii țintite, personalizate. Această tehnologie permite testului Guardant360 CDx să diagnostice mutații în 55 de gene, cunoscute drept promotori frecvenți ai neoplaziilor. Totuși, aprobarea curentă a FDA permite utilizarea Guardant360 CDx doar în diagnosticul EGFR, în scopul administrării osimertinib la pacienții cu cancer pulmonar non-microcelular metastatic.
Cancerul pulmonar este cea mai frecventă formă de cancer și principala cauză de mortalitate prin cancer la nivel mondial. În ciuda faptului că este în mare măsură prevenibilă, 1 din 5 decese cauzate de cancer în Europa se datorează cancerului pulmonar. În țările occidentale, rata de supraviețuire la cinci ani pentru cancerul pulmonar este în medie de 15%. În România, rata de supraviețuire la cinci ani între 2010-2014 a fost de 11,2%.
Tipul non-microcelular reprezintă 85% din totalul cazurilor de cancer pulmonar. O proporție variabilă dintre aceste cazuri se asociază cu mutația EGFR – între 13% și 36%. Această mutație este relativ frecventă printre pacienții cu cancer pulmonar fără istoric de fumat, de sex feminin. Deoarece au fost dezvoltate molecule mici care tratează în mod țintit anomaliile celulare cauzate de mutațiile EGFR (precum osimertinib), identificarea acestei mutații este esențială în gestionarea corectă a NSCLC.
Citește și:
- ISTORIC. Diagnosticul cancerului pulmonar, mai precis și mai rapid. FDA aprobă primul test bazat pe NGS, Oncomine DX
- #AACR20. Biopsia lichidă poate identifica precoce peste 50 de tipuri de cancere
- Raport IHE. Progrese în diagnosticul cancerului: cum au schimbat testarea genomică și biomarkerii standardul european?

