ISTORIC. Diagnosticul cancerului pulmonar, mai precis și mai rapid. FDA aprobă primul test bazat pe NGS, Oncomine DX
Esențialul despre știre:
- Oncomine Dx este primul test de secvențiere a genomului de ultimă generație aprobat vreodată în lume pentru diagnosticul cancerului
- Rezultatele sunt mult mai rapide (4 zile) și mai precise, fiind în măsură să ghideze alegerea tratamentului personalizat al cancerului pulmonar
- NGS este termenul utilizat pentru a descrie o nouă tehnologie de secvențiere ADN care a revoluționat testarea genomului. Cu noua metodă, întregul genom uman poate fi secvențiat într-o singură zi, pentru aproximativ 1.000 de lire.
Testul Oncomine Dx dezvoltat de către compania Thermo Fisher Scientific va fi folosit pentru selectarea pacienților care au mutația BRAF V600E în vederea tratării acestora cu dabrafenib și trametinib în combinație, pentru selectarea pacienților cu mutația EGFR și tratarea cu gefitinib (Iressa) și mutația ROS1 pentru tratamentul cu crizotinib (Xalkori). Aprobarea Oncomine Dx este în sine un moment istoric, fiind primul test de secvențiere a genomului de ultimă generație (NGS) aprobat de către FDA (Food and Drug Administration).
Unul dintre avantajele majore ale acestui test îl constituie aplicarea lui pe o singură mostră de țesut, o singură dată. Testul detectează prezența mutațiilor genetice BRAF (mutație specifică mai multor tipuri de cancer, printre care cancerul pulmonar, melanomul și cancerul colorectal), ROS1 (gena care codifică tirozin-kinaza, specifică mai multor tipuri de tumori canceroase), EGFR (receptorul pentru factorul de creştere epidermică, receptor tirozin-kinazic) sau alterări ale țesutului tumoral la pacienții care suferă de cancer pulmonar fără celule mici (NSCLC).
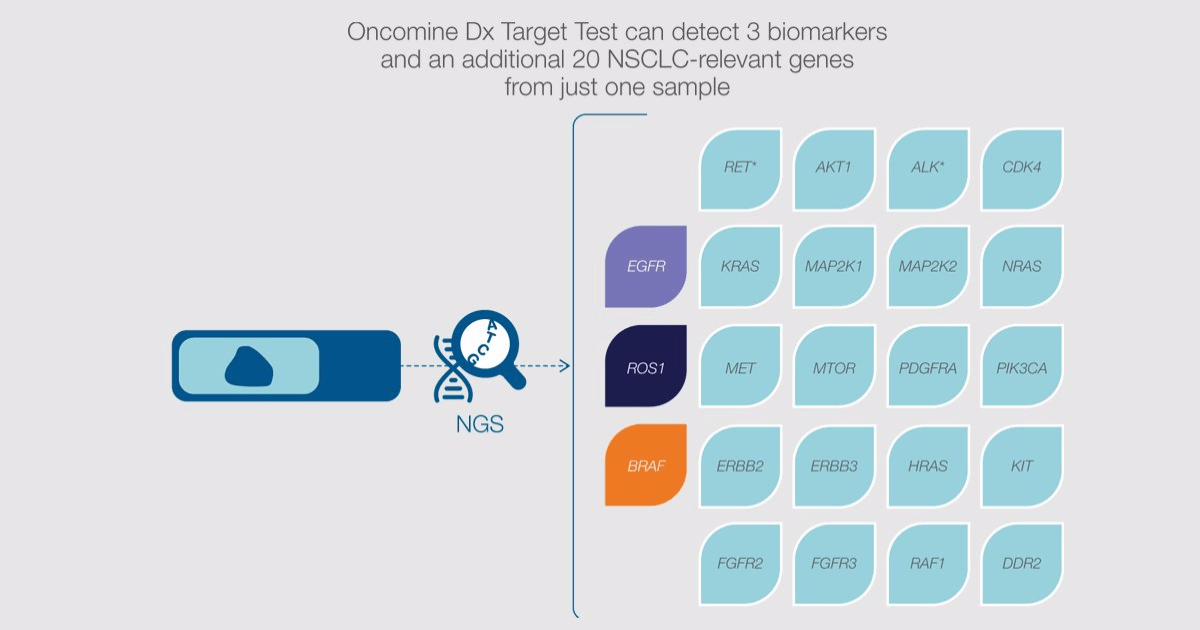
Noul test a fost dezvoltat ca urmare a provocării pe care testarea secvențială a mutațiilor individuale o aduce pentru laboratoarele clinice. Oncomine Dx recunoaște multipli biomarkeri și oferă rezultatele în decursul a patru zile. De asemenea, testul vizează alte 20 de mutații ale cancerului pulmonar fără celule mici, însă studiile efectuate pe această ramură nu s-au finalizat.
„Pentru oamenii care se luptă cu cancerul pulmonar fără celule mici, timpul este critic și fiecare zi contează. Testul țintit Onconime Dx ghidează rapid medicii oncologi spre terapia țintită potrivită cu scopul de a îmbunătăți experiența pacientului cu boala și pentru ca acesta să beneficieze de un tratament cost-eficient”, a declarat Joydeep Goswami, președintele departamentului de NGS și oncologie în cadrul Thermo Fisher.
Ce desemnează termenul NGS (next-generation sequencing)?
NGS este termenul utilizat pentru a descrie o nouă tehnologie de secvențiere ADN care a revoluționat testarea genomică. Utilizând noua metodă, întregul genom uman poate fi secvențiat într-o singură zi. Spre comparație, tehnologia Sanger a avut nevoie de cel puțin 10 ani pentru a livra rezultatul final în cazul secvențierii primului genom uman.
Există mai multe platforme de secvențiere de nouă generație, toate rulând milioane de bucăți mici de ADN în paralel. Analiza bioinformatică este utilizată pentru a lega aceste mici fragmente și a crea o hartă de referință. De exemplu, mutația BRAF V600E a fost evidențiată în anul 2002 ca mutație specifică melanomului în cadrul cercetărilor efectuate cu secvențierea Sanger.
Variația ADN-ului în genomul uman constă în substituții, inserții și deleții ale exonilor sau ale unor gene întregi, dar și rearanjamente – inversii și translocații. Secvențierea tradițională Sanger se rezuma la descoperirea substituțiilor, a inserțiilor și a delețiilor mici. Pentru restul mutațiilor, erau efectuate cercetări amănunțite, cum ar fi fluorescențele locale și hibridizările pentru cariotipul clasic sau hibridizările genomice comparative pentru detectarea schimbărilor cromozomiale, a microdelețiilor. Aceste date pot fi preluate cu ușurință și din metoda NGS, prin extragerea întregii hărți a genomului deodată.
Singurele limitări ale metodei NGS sunt legate de infrastructură: capacitatea calculatoarelor, spațiul de stocare și interpretarea datelor. Datele trebuie analizate atent pentru a extrage informațiile cu importanță clinică. Costul unei astfel de proceduri este neglijabil comparativ cu cel al metodei Sanger. O platformă de tip NGS poate genera 150 de milioane de citiri cu aproximativ 1.000 de lire, în timp ce o singură citire Sanger costă aproximativ o liră.
Aprobare FDA și pentru combinația dabrafenib-trametinib
Odată cu aprobarea testului și apariția posibilității de a selecta rapid pacienții eligibili pentru tratament, FDA a aprobat și administrarea de dabrafenib și trametinib (TAFINLAR și MEKINIST, produse ale Novartis Pharmaceuticals Inc.).
Aprobarea celor două medicamente s-a bazat pe studiul BRF113928, un studiu nerandomizat, deschis, efectuat pe pacienți la care existența mutației BRAFV600E în cancerul pulmonar fără celule mici era confirmată deja. 93 de pacienți au fost tratați cu dabrafenib (150 mg administrate oral de două ori pe zi) și trametinib (2 mg administrate oral odată pe zi) în combinație. Dintre cei 93 de pacienți, 36 nu au primit nicio altă terapie sistemică pentru tratarea NSCLC metastazat, iar 57 dintre ei au primit cel puțin un tratament complet cu chimioterapie bazată pe platină și au demonstrat în continuare progresia bolii. De asemenea, un grup de 78 de pacienți care fuseseră tratați anterior pentru NSCLC au primit monoterapie cu drabrafenib.
Incidența și severitatea reacțiilor adverse apărute în cazul pacienților au fost similare cu cele raportate anterior în cazul pacienților cu melanom. Cele mai întâlnite reacții adverse au fost pirexia, oboseala, amețeala, voma, diareea, pielea uscată, apetitul scăzut și edemul. Administrarea de dabrafenib a fost sistată din cauza reacțiilor adverse la 18% dintre pacienți, respectiv 19% în cazul administrării de trametinib.
Dozele recomandate sunt dabrafenib 150 mg, oral, la 12 ore, în combinație cu trametinib 2 mg administrat oral o dată pe zi.
Mai multe detalii în următoarele articole:
- FDA grants regular approval to dabrafenib and trametinib combination for metastatic NSCLC with BRAF V600E mutation
- Onconime Dx Target Test
- What is next generation sequencing?
Sursa foto: Thermofisher.com

