Brolucizumab, recomandat spre aprobare în UE pentru tratamentul degenerescenței maculare legate de vârstă
Brolucizumab, un anticorp monoclonal anti-VEGF, a primit recomandare spre aprobare de către Comisia pentru Medicamente pentru Uz Uman (CHMP) din cadrul EMA, pentru tratamentul degenerescenței maculare legate de vârstă, forma neovasculară (DMLV „umed”).
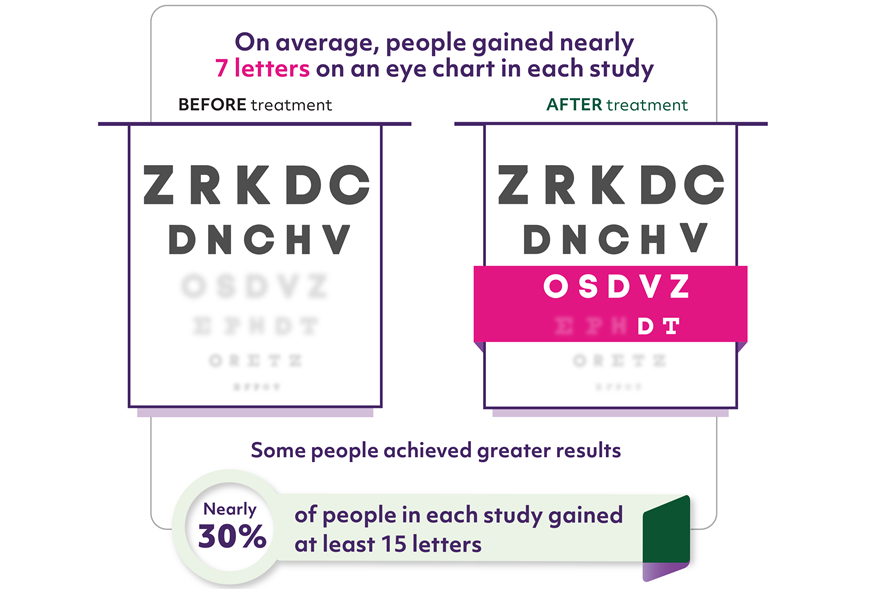
Această opinie pozitivă a venit în urma rezultatelor studiilor de fază III HAWK și HARRIER, care au demonstrat ameliorarea funcției vizuale la pacienții care au primit tratament cu brolucizumab.
Rezultatele studiului
Studiile HAWK și HARRIER au ajuns la concluzia că brolucizumab este non-inferior aflibercept, un alt agent terapeutic țintit, utilizat deja în tratamentul DMLV neovascular.
Cei 1817 de pacienți incluși în studii prezentau neovascularizație coroidiană netratată, secundară degenerescenței maculare legate de vârstă. După 48 de săptămâni, acuitatea vizuală (AV) a celor două grupuri de pacienți (brolucizumab și aflibercept) a fost comparată (AV fiind estimată în funcție de numărul de litere vizibile pentru pacient la testul cu optotipul).

În studiul HAWK, care a comparat un grup brolucizumab 3 mg, unul brolucizumab 6 mg, cu un grup aflibercept 2 mg:
- Grupul brolucizumab 3 mg a obținut o ameliorare medie de 6.1 litere pe optotip, iar în urma dozei de 6 mg, 6.6 litere pe optotip;
- Grupul aflibercept a obținut o ameliorare medie de 6.8 litere pe optotip;
- 24% dintre pacienții din grupul brolucizumab 6 mg au prezentat o forma activă a bolii, față de 34.5% în grupul aflibercept;
- Mai puțini pacienți prezintă lichid intraretinian (consecință a vaselor de neoformație din cadrul DMLV neovascular) în grupul brolucizumab 6 mg (31.2%), față de grupul aflibercept (44.6%).
În studiul HARRIER, care a comparat un grup brolucizumab 6 mg cu un grup aflibercept 2 mg:
- Grupul brolucizumab a obținut o ameliorare medie de 6.9 litere pe optotip, față de 7.6 litere în grupul aflibercept
- 22.7% dintre pacienții din grupul brolucizumab au prezentat o forma activă a bolii, față de 32.2% în grupul aflibercept;
- Mai puțini pacienți prezintă lichid intraretinian în grupul brolucizumab (25.8%), față de grupul aflibercept ( 43.9%).
Sursa foto Novartis
Frecvența și tipul reacțiilor adverse au fost similare între grupurile de pacienți, în ambele studii.
Degenerescența maculară legată de vârstă
DMLV este principala etiologie a cecității, printre persoanele peste 50 de ani. Aceasta reprezintă o degenerare a stratului interior al ochiului- retina- mai exact zona responsabilă cu acuitatea vizuală maximă- macula. În afară de vârstă, DMLV este favorizată și de sexul feminin, dietă, factorii de risc cardiovasculari cunoscuți, și de asemenea de prezența simultană a hipermetropiei.
Sursa foto (adaptat după) Novartis
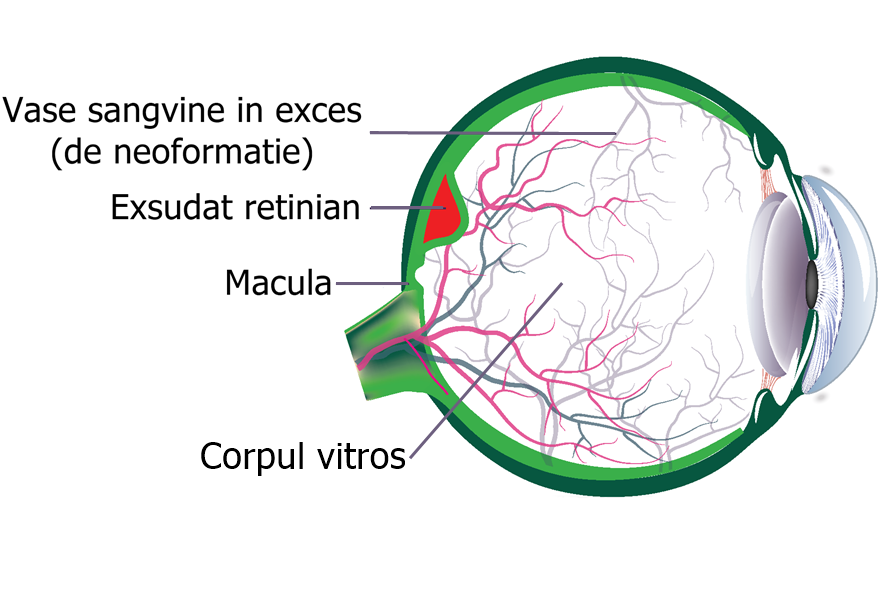
Degenerescența maculară legată de vârstă neovasculară (sau „umedă”) este cauzată de proliferarea anormală a vaselor sangvine de neoformație, care invadează retina și se poate complica cu hemoragii, exsudate sau chiar dezlipire de retină. Datorită mecanismului de producere vascular, unul dintre cele mai eficiente tratamente ale DMLV neovascular este inhibarea VEGF (factorul de creștere vascular endotelial), astfel inhibând apariția de noi vase la nivelul retinei.
Brolucizumab este unul dintre cei mai recenți agenți terapeutici care inhibă în mod specific VEGF-A. Acesta a fost aprobat pentru tratamentul DMLV neovascular de către FDA în SUA, în decursul acestui an, iar Comisia pentru Medicamente pentru Uz Uman (CHMP) din cadrul EMA l-a recomandat spre aprobare în UE. Avantajul brolucizumb, față de alți agenți anti-VEGF, este o frecvență mai scăzută de administrare. Aceste terapii necesită injecție intraoculară (la nivelul corpului vitros) frecventă, la aproximativ 8 săptămâni, față de brolucizumab, care necesită injecție la 12 săptămâni.
Citește și:
- BREAKING NEWS. Luxturna, prima terapie genică aprobată în UE pentru distrofia retiniană ereditară, o frecventă cauză a pierderii vederii
- Tratamentul neovaselor din retinopatie: actualități și direcții terapeutice viitoare
- MiSight, primele lentile de contact care corectează și încetinesc progresia miopiei la copii, aprobate de FDA

