#ASCO22. Vaccinul terapeutic personalizat, bazat pe ARNm, determină remisiunea la jumătate din cazurile de cancer pancreatic, într-un studiu de fază I
După succesul demonstrat de tehnologia ARNm în vaccinarea împotriva COVID-19, noi date dintr-un studiu de fază I arată potențialul acestei abordări în tratamentul cancerului pancreatic. Administrarea unui vaccin terapeutic personalizat bazat pe ARNm determină activarea limfocitelor T și un răspuns imun semnificativ care se corelează cu o rată crescută a supraviețuirii fără recurența bolii la pacienții cu adenocarcinom ductal pancreatic rezecat. Rezultatele au fost prezentate la Întâlnirea Anuală a Societății Americane de Oncologie Clinică (ASCO2022).
Autogene cevumeran este un vaccin candidat dezvoltat de BioNTech în colaborare cu Genentech, pentru mai multe tipuri de tumori solide. Acesta poate fi creat pentru fiecare pacient în parte, fiecare doză cuprinde până la 20 de neoantigene specifice tumorii pacientului, fiind dezvoltat pe baza platformei BioNTech – individualized neoantigen-specific immunotherapy (iNeST). Vaccinul oncologic a demonstrat activitate clinică semnificativă și un profil bun de siguranță în cazul cancerului pancreatic.
Deși folosește o tehnologie asemănătoare cu a vaccinului împotriva COVID-19, există diferențe între cele două tipuri de vaccinuri. Autogene cevumeran nu este administrat cu scop preventiv, ci de tratament: nu previne apariția cancerului, ci stimulează răspunsul imun, prin celulele T, țintind antigene tumorale (este un tip de imunoterapie).
În octombrie 2021, BioNTech a raportat administrarea vaccinului oncologic personalizat realizat prin platforma iNeST, primului pacient cu cancer colorectal, stadiile II/III, într-un studiu de fază II. De asemenea, BioNTech și Genentech evaluează în prezent, autogene cevumeran în combinație cu pembrolizumab pentru tratamentul de linia I al melanomului.
Studiul de fază I care a evaluat vaccinul pentru cancerul pancreatic a fost realizat la Memorial Sloan Kettering Cancer Center, New York.
În urma intervenției chirurgicale, pacienții cu adenocarcinom pancreatic au primit un inhibitor PD-L1, atezolizumab, în săptămâna a 6-a, urmat de autogene cevumeran (administrat la 8 săptămâni), apoi chimioterapie (FOLFIRINOX). Obiectivul primar a fost evaluarea profilului de siguranță.
După o perioadă de urmărire de 18 luni s-au obținut următoarele rezultate:
- S-a obținut un răspuns imun semnificativ la 50% (8 din 16) din pacienți, determinând activarea de limfocite T specifice pentru neoantigenele administrate. Datele preliminare arată că răspunsul imun indus de aceste neoantigene se corelează cu evoluția pacienților;
- Pacienții cu răspunsuri imune de novo (8 cazuri) au avut o rată de supraviețuire fără recurența bolii mult mai mare;
- Combinația terapeutică are un profil bun de siguranță;
- Procesul de fabricație pentru vaccinul candidat este fezabil, fiind posibilă obținerea produsului final în timp util pentru tratamentul pacienților.
Pe baza datelor din studiul de fază I, BioNTech și Genentech plănuiesc un studiu randomizat pentru a evalua eficacitatea și siguranța vaccinului în combinație cu atezolizumab și chimioterapie la pacienți cu adenocarcinom pancreatic ductal rezecat.
Dezvoltarea unui vaccin oncologic personalizat pentru cancerul pancreatic
Adenocarcinomul ductal pancreatic (PDAC, pancreas ductal adenocarcinoma) reprezintă o nevoie neacoperită în oncologie, fiind un tip tumoral asociat cu o supraviețuire redusă (90% din pacienți nu supraviețuiesc mai mult de 24 de luni de la diagnostic). Până acum, acesta a fost refractar la imunoterapie, fiind caracterizat de o rată redusă de mutații, însă s-a observat că anumite categorii de pacienți, care supraviețuiesc mai mult, prezintă și un răspuns imun anti-tumoral mai ridicat.
Tumorile rezecate de la aceste cazuri prezentau niveluri ridicate ale limfocitelor T, care recunoșteau proteine exprimate de celulele maligne numite neoantigene. În cele mai multe cazuri, aceste neoantigene nu sunt detectate de sistemul imun, astfel încât celulele tumorale nu sunt percepute ca ținte. Neoantigenele de la subsetul de pacienți care supraviețuiau mai mult erau, însă, recunoscute de sistemul imun. Conform cercetărilor realizate în cadrul MSK, limfocitele T pot recunoaște neoantigenele circulante în sânge și până la 12 ani după ce tumorile pancreatice au fost îndepărtate. Acest răspuns a persistat, la fel cum vaccinurile determină memorie imunologică pe termen lung și pot proteja contra infecțiilor chiar și mai multe decenii. Pornind de la aceste observații, publicate în Nature în 2017, s-au explorat mecanisme prin care se poate activa sistemul imun și pentru alte categorii de pacienți cu cancer pancreatic
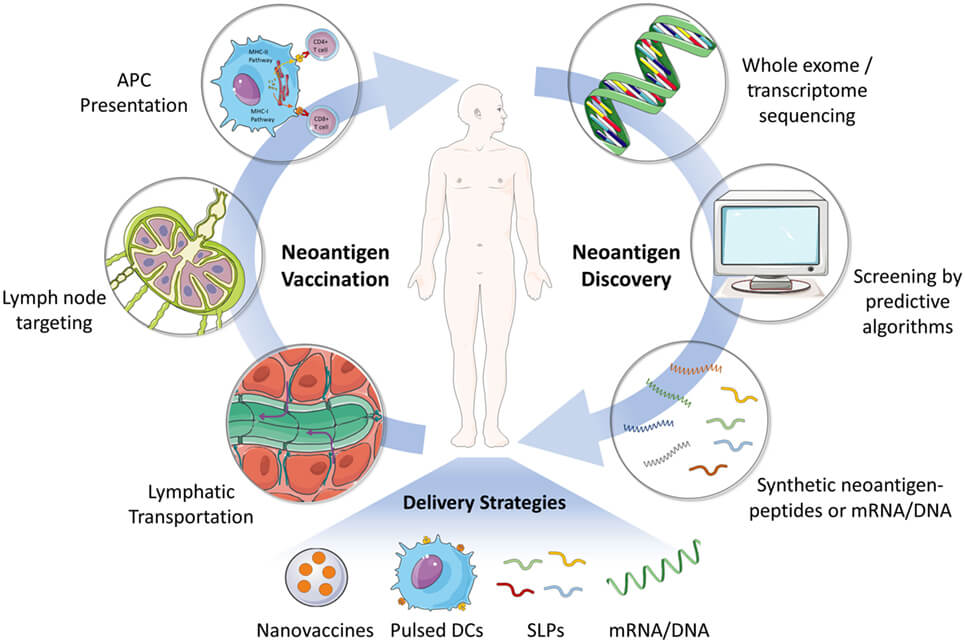
Moleculele de ARNm pot fi utilizate în producerea de vaccinuri sau pentru tratamentul și prevenția diferitelor patologii. Spre deosebire de vaccinurile bazate pe ADN și vectorii virali, acestea au avantajul de a nu prezenta riscul de inserție în genomul gazdei. ARNm este translatat în proteine imediat după ce intră în citoplasmă iar expresia proteinelor poate fi tranzitorie, de aceea permite administrări repetate. Un alt avantaj ține de faptul că permite flexibilitate în alegerea antigenelor, pot fi codificate mai multe tipuri de neoantigene, dar și molecule imunomodulatoare, care pot influența atât răspunsul imun înnăscut, cât și pe cel dobândit. Limfocitele T sunt principalul efector care mediază răspunsul terapeutic al acestor vaccinuri.
Vaccinurile oncologice personalizate au intrat deja în studii clinice, demonstrând eficacitate și siguranța pentru anumite tumori solide și hematologice.
Citește și:
- #ASCO22. Importanța biomarkerilor în selectarea pacienților cu cancer de colon și cancer mamar, în stadii incipiente, care pot evita chimio/radioterapia
- #ASCO22. Progrese în ţintirea terapeutică a mutaţiilor KRAS pentru pacienţii cu cancer pulmonar non-microcelular

