STUDIU. Medicii oncologi trebuie să fie informați asupra posibilei origini germinale a variantelor patogenice identificate în cursul testării NGS comprehensive la nivel tumoral
Variante cu semnificație patogenă la nivelul liniei germinale sunt descoperite frecvent la pacienții pentru care se efectuează testare comprehensivă genomică tumorală. Cu toate acestea, nu există o metodă standardizată pentru interpretarea acestor informații, considerate „incidentale”, care reprezintă adesea o provocare pentru medicii oncologi.
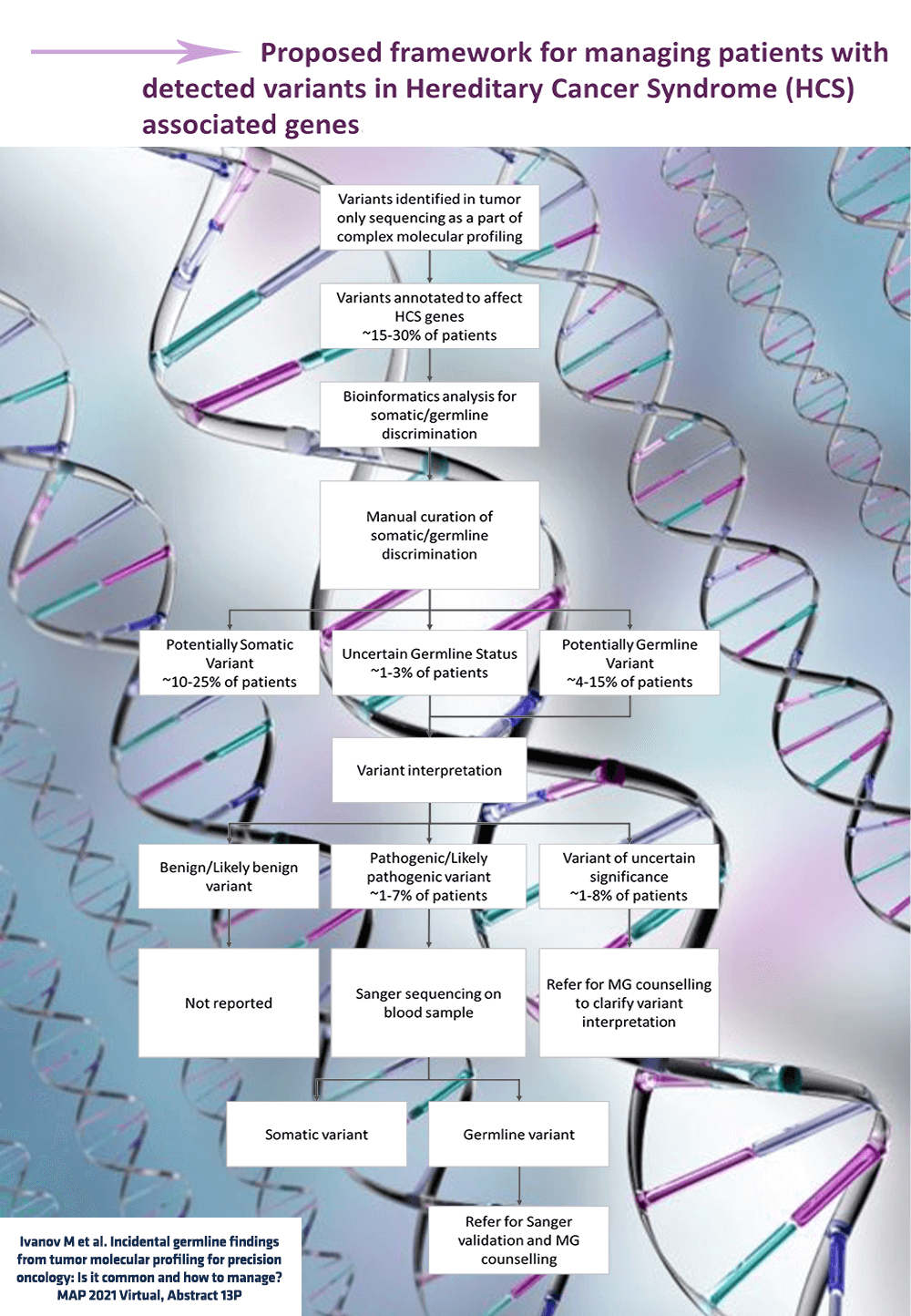
O analiză prezentată în cadrul Congresului de analiză moleculară și oncologie de precizie (MAP virtual 2021) indică importanța integrării în practică a acestor tipuri de date. Autorii propun, de asemenea, un algoritm de management al pacienților pentru care se identifică mutații în gene asociate sindroamelor de predispoziție la cancer.
„Dacă vrem să folosim informațiile obținute din analiza NGS în beneficiul pacienților, trebuie să creștem conștientizarea în rândul medicilor oncologi în ceea ce privește posibila origine germinală a variantelor patogene și să punem la dispoziție resursele necesare pentru a înțelege implicațiile acestor rezultate atât pentru pacienți, cât și pentru familiile acestora”, a declarat dr. Judith Balmaña, de la Institutul Oncologic Vall dʹHebron din Barcelona.
În ultimii 10 ani au fost tot mai frecvent utilizate în practică metode de analiză moleculară tumorală prin secvențiere cu ajutorul unor paneluri extinse de gene în scopul personalizării tratamentului în oncologie. În urma obținerii rezultatelor cu semnificație patogenică, nu de puține ori este neclar dacă originea acestor variante este una strict somatică sau constituțională (germinală). Aceste paneluri pot identifica mutații în gene de susceptibilitate la cancer, iar originea la nivel germinal conferă pacientului un risc crescut de a dezvolta unul sau mai multe tipuri de cancere de-a lungul vieții individului. Astfel de rezultate pot fi dificil de gestionat de către medicii oncologi în condițiile în care cea mai frecventă abordare în clinică este în primul rând analiza țesutului tumoral.
O analiză a Institutului de Fizică și Tehnologie din Moscova care a inclus 183 de pacienți cu diferite tipuri de cancere: colorectal, pancreatic, pulmonar și alte tumori, a constatat că din cele 56 de variante identificate prin secvențiere, 17 erau de origine germinală. Dintre acestea, 6 au fost variante patogene sau potențial patogene și 9 au fost variante cu semnificație incertă (VUS). Autorii estimează că pentru până la 7% din cazuri este necesară analiza țesutului sănătos (pentru variante patogene și potențial patogene), iar consilierea genetică se impune în 2 până la 15% din cazuri (incluzând și cazurile cu VUS-uri în gene de susceptibilitate la cancer).
Aceștia au propus un algoritm de management al pacienților pentru care se identifică mutații în gene asociate sindroamelor de predispoziție la cancer, care să conducă analiza datelor în zona de transpunere în scenarii clinice.
J. Balmana, unul dintre autorii studiului, a subliniat provocările pe care le impun aceste tipuri de analize, în specialhttps://oncologypro.esmo.org/meeting-resources/map-2021/incidental-germline-findings-from-tumor-molecular-profiling-for-precision-oncology-is-it-common-and-how-to-manage cu privire la expertiza membrilor din comisiile oncologice în ceea ce privește interpretarea rezultatelor, adesea raportate ca descoperiri “incidentale”.
„Identificarea unei mutații în linia germinală este doar vârful icebergului. Managementul acestor descoperiri poate îmbunătăți prognosticul pacientului dacă este realizat corespunzător și ar trebui să reprezinte o prioritate pentru orice medic oncolog”.
Pe lângă informarea continuă necesară pentru medici, și pacienții ar trebui să fie bine informați în legătură cu implicațiile pe care le aduce testarea moleculară tumorală și despre cum rezultatele acestora pot avea atât implicații terapeutice, cât și posibilitatea de a conduce cazul către consiliere genetică.

Despre sindroamele de predispoziție la cancer
Cancerul reprezintă o boală complexă, produsă prin acumularea unor modificări la nivelul genomului celulelor, care conduc la alterarea sistemelor de control și reglare a diviziunii celulare. De cele mai multe ori, aceste modificări sunt pur somatice, apărute de-a lungul vieții individului la nivelul anumitor celule din organism sau pot exista încă de la formarea embrionului, de novo sau moștenite de la unul dintre părinți, în toate celulele organismului nou-format (constituționale), ca factor de predispoziție ereditară la anumite forme de cancer, în funcție de variantele existente.
Se estimează că 5 până la 10% din cazurile de cancer colorectal, cancer de sân sau ovarian apar la persoanele purtătoare ale unei variante patogenice la nivelul unei gene de susceptibilitate pentru cancer; aceste procente sunt variabile în funcție de tipurile de cancer și de genele implicate.
În pofida posibilităților tehnologice de identificare a acestor persoane cu un risc semnificativ de a dezvolta anumite forme de cancer pe parcursul vieții, multe dintre acestea nu sunt recunoscute sau sunt detectate tardiv, după unul sau mai multe diagnostice de cancer. Astfel, șansele de înrolare în programe de prevenție presonalizate pentru riscul lor scad semnificativ, iar consilierea genetică nu mai este la fel de eficientă.
Citește și:
- STUDIU. Primele hărți comprehensive ale regiunilor enhancer de la nivelul genomului uman: noi instrumente pentru predicția riscului de boală și selectarea markerilor GWAS relevanți
- #BiotechWeek2020. Dr. Benedikt Westphalen, expert în onco-genomică: „Oncologia de precizie este precum un puzzle. Avem toate piesele și datoria să le potrivim, pentru ca pacienții să poată beneficia de întregul potențial”
- Planul european de luptă împotriva cancerului: inovația, factorul care trebuie să reducă diferența Est-Vest

