Premiul Nobel pentru Medicină 2018: înțelegerea mecanismelor prin care sistemul imunitar luptă împotriva cancerului
Astăzi, pe 1 octombrie, la Karolinska Institutet din Solna, Suedia, au fost anunțați laureații Premiului Nobel pentru Medicină sau Fiziologie 2018: James Allison și Tasuku Honjo, pentru cercetările asupra imuno-oncologiei, mai precis identificarea “frânelor” moleculare de la nivelul sistemului imun, pe care s-a bazat dezvoltarea inhibitorilor punctelor de control.

Despre laureați
James P. Allison, născut în 1948, este un imunolog american și profesor la Centrul Oncologic M. D. Anderson. Acesta a efectuat cercetările asupra CTLA-4 în laboratoarele Universității Berkeley din California.
Tasuku Honjo, născut în 1942 în Kyoto, este un imunolog japonez și profesor la Universitatea din Kyoto. Aici a efectuat experimentele ce au condus la stabilirea importanței PD-1 în oncologie.
Sub denumirea de cancer stau o multitudine de boli diferite. Răspunsul fiecărui pacient la tratamentul oncologic este influențat de numeroși factori: tipul de cancer stabilit cu precizie, stadiul în care acesta este descoperit și sănătatea generală a pacientului. De-a lungul istoriei, au existat 3 metode principale de luptă împotriva acestei maladii: chirurgia, iradierea și chimioterapia. Totuși, acestea nu sunt soluții optime în cazul tumorilor avansate, care se asociază de altfel și cu o mortalitate ridicată. În acest context a fost dezvoltat conceptul de imuno-oncologie – utilizarea sistemului imunitar propriu organismului în lupta contra celulelor tumorale. Acest concept a reprezentat un punct de turnură esențial în modul în care numeroase tumori sunt abordate (de exemplu cancerul pulmonar, colorectal ori melanomul).
Importanța imuno-oncologiei este astăzi confirmată: premiul Nobel pentru Medicină sau Fiziologie a fost decernat pentru descifrarea mecanismelor ce stau la baza interacțiunii între sistemul imunitar și tumorile maligne, mai exact funcția inhibitorilor punctelor de control.

Despre cancer și imunitate
O oarecare interacțiune între imunitate și cancer a fost observată încă din secolele 19 și 20. Unele tumori intrau în remisiune după ce pacientul trecea printr-un episod de infecție. Ipoteza că activarea sistemului imunitar împotriva bacteriilor aduce concomitent și un efect benefic contra cancerului a fost testată, dar nu s-a ajuns la rezultate concludente (în afară de utilizarea vaccinului BCG contra uroteliomului).
Sistemul imunitar este deosebit de complex și este structurat astfel încât să evite atacarea celulelor proprii organismului (în mod contrar, pot apărea boli autoimune și autoinflamatorii). Aceasta reprezintă proprietatea de a deosebi elementele self (proprii organismului) de cele non-self (străine organismului, precum bacteriile ori tumorile).
Limfocitele T citotoxice sunt esențiale în atacul contra elementelor non-self. Aceste celule prezintă o serie de proteine pe suprafața lor, care le inhibă acțiunea distructivă asupra celulelor corpului uman, self: CTLA-4, PD-1. Celulele tumorale pot profita de aceste „frâne” moleculare ale sistemului imunitar pentru a prolifera.
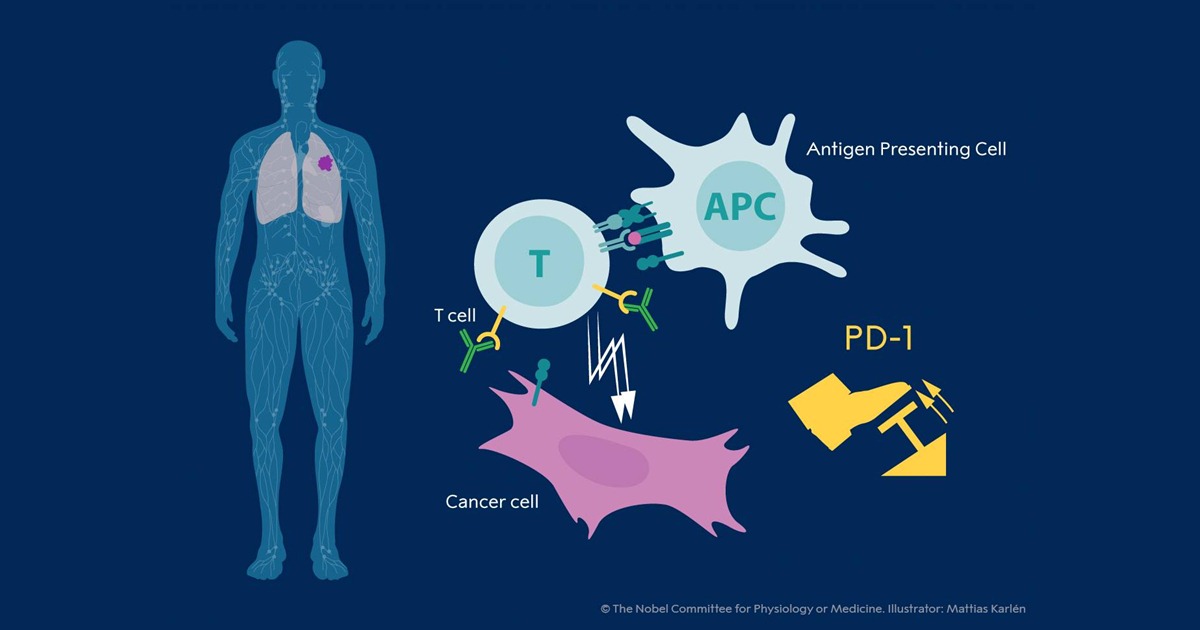
Tasuku Honjo și proteina PD-1
Tasuku Honjo, laureat al Premiului Nobel în acest an, a descoperit proteina PD-1 în 1992. Acesta este un acronim pentru Programmed Cell Death – inițial se credea despre PD-1 că este implicat în procesul de apoptoză. Cercetări ulterioare ale acestuia au revelat funcția de „frână” a PD-1 asupra limfocitului T – o celulă esențială în lupta organismului cu celulele tumorale sau infecțioase. Ulterior au fost descoperiți și liganzii PD-1, PD-L1 și PD-L2– substanțe de la suprafața celulelor care au efect inhibitor asupra limfocitului T. Astfel, prin legarea PD-1 de PD-L1 sau PD-L2, limfocitul T primește mesajul de a stopa reacția imună de la diferite celule normale imune, precum macrofagele sau celulele dendritice. Însă, de acest mecanism profită și celulele tumorale – acestea pot prezenta pe suprafața lor liganzi pentru PD-1 și pot inhiba atacul limfocituluI T.
Primul anticorp monoclonal care inhibă țintit PD-1 a fost nivolumab, urmat de pembrolizumab, ambele aprobate astăzi în Statele Unite ale Americii și Uniunea Europeană pentru mai multe indicații, printre care și melanomul ori cancerul pulmonar.
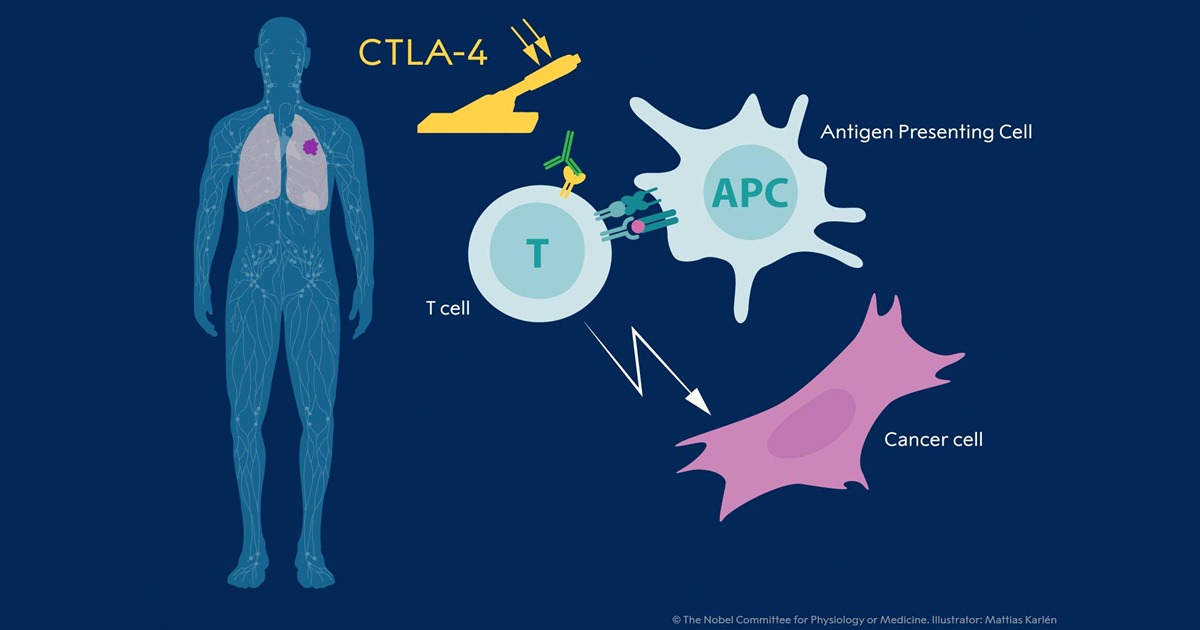
James P. Allison și proteina CTLA-4
În anii ’90, James Allison, și el laureat al Premiului Nobel din acest an, a studiat funcția unei proteine, descoperită în 1987 și denumită CTLA-4 (cytotoxic T lymphocyte antigen 4 – antigenul 4 al limfocitului T citotoxic). Aceasta are rolul de reglare negativă, de inhibiție a limfocitului T. Allison a observat potențialul acestei descoperiri în domeniul oncologic. A efectuat experimente pe animale de laborator (șoricei) care aveau diferite tipuri de tumori: prin inocularea unui anticorp careare inhibă CTLA-4, tumorile acestora au involuat spectaculos, iar unii șoricei au fost chiar vindecați. Această linie terapeutică a fost ulterior studiată în alte laboratoare pe modele animale de cancer prostatic, mamar sau melanom malign.
Primul anticorp monoclonal care inhibă țintit CTLA-4 și are efecte semnificative împotriva tumorilor este ipilimumab, dezvoltat în 1999. În 2011, ipilimumab a fost aprobat în Statele Unite ale Americii și în Uniunea Europeană pentru tratamentul melanomului metastatic nerezecabil.
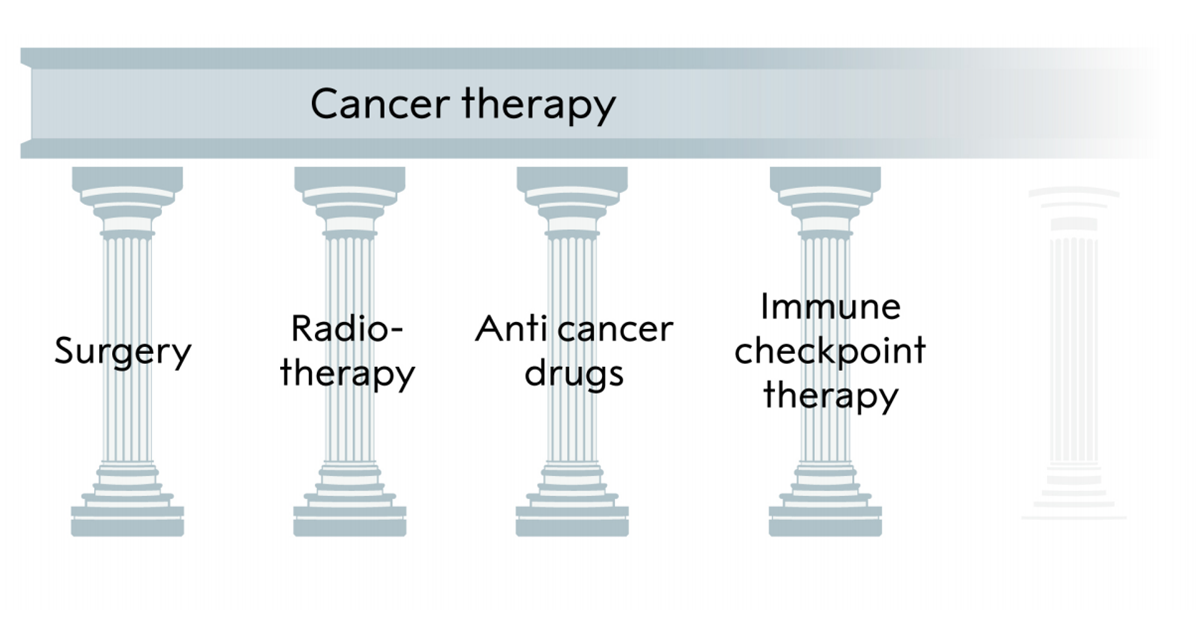
Importanța imuno-terapiilor
Inhibitorii punctelor de control, la a căror dezvoltare au contribuit laureații Premiului Nobel 2018, au reprezentat o evoluție importantă în tratamentul cancerului. Această terapie se adresează mai ales tumorilor în stadii avansate și metastatice, care au de obicei un prognostic deosebit de rezervat.
Citește și:
- State of Innovation 2018: Dr. Marius Geantă, despre accesul la imunoterapii și cum trebuie regândit sistemul în oncologie
- Procentul românilor care au auzit de medicina personalizată a crescut cu 14% în ultimii doi ani
- 5 inovații care vor schimba pentru totdeauna tratamentul cancerului, folosind sistemul imun al organismului

