O nouă imunoterapie este compensată în România: nivolumab, contract cost-volum semnat pentru cancerul pulmonar și cancerul renal
Nivolumab va fi disponibil în aceste zile pentru pacienții români cu NSCLC (cancer pulmonar fără celule mici) cu forme scuamoase și nescuamoase, tratați anterior cu chimioterapie, și pentru pacienții care au carcinom cu celule renale. Contractul cost-volum a fost semnat de către CNAS (Casa Națională de Asigurări de Sănătate) și compania farmaceutică BMS (Bristol-Myers Squibb) care deține APP-ul (autorizația de punere pe piață) pentru nivolumab. Protocolul de prescriere a fost finalizat și urmează să fie publicat în Monitorul Oficial. Acesta este încă un moment important pentru România în ceea ce privește accesul pacienților la imunoterapii.
Decizia de a introduce nivolumab în rândul terapiilor la care au acces pacienții români se bazează pe numeroasele avantaje pe care medicamentul le-a dovedit în tratarea tipurilor de cancer. Atât în cazul tratamentului pentru NSCLC, cât și în cazul carcinomului cu celule renale, noua terapie s-a dovedit mai eficientă decât vechile variante de tratament, crescând astfel speranța de viață și calitatea vieții pacientului, prin eliminarea efectelor adverse pe care le determină chimioterapia.
Aprobarea nivolumab (Opdivo – denumirea comercială) pentru tratarea NSCLC, după chimioterapie, a survenit în urma studiului clinic CheckMate017, un studiu de fază III, randomizat, care a urmărit eficacitatea nivolumabului administrat în doză de 3mg/kg, la două săptămâni.
Acesta fost efectuat pe un lot de 272 de pacienți care au fost împărțiți în mod egal în două grupuri:
- un grup de pacienți cărora li s-a administrat o perfuzie intravenoasă cu nivolumab în doză de 3mg/kg la fiecare 2 săptămâni;
- un grup de pacienți cărora li s-a administrat o perfuzie intravenoasă cu docetaxel (vechea terapie) în doză de 75mg/m² la fiecare 3 săptămâni.
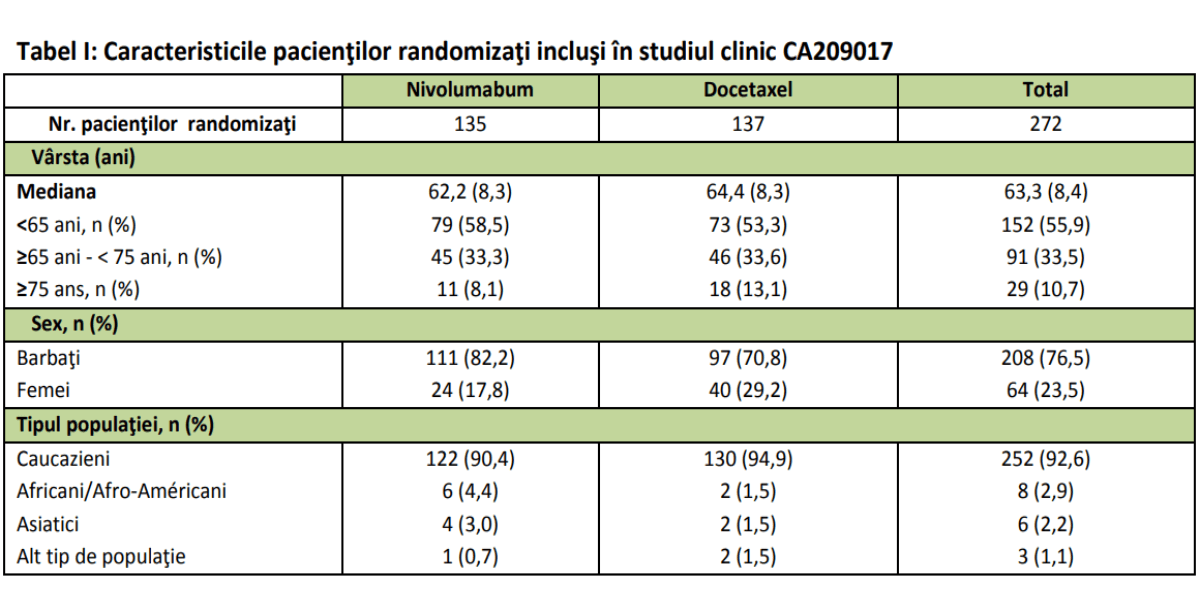
Principalele avantaje observate au fost:
- Rata de răspuns a fost de 20% în grupul tratat cu nivolumab comparativ cu 8,8% în grupul tratat cu docetaxel (p <0,0083). La momentul analizei intermediare, mediana duratei răspunsului a fost de 8,41 luni în grupul cu docetaxel și nu a fost atins în grupul cu nivolumab;
- Rata de supravieţuire fără progresia bolii a fost de 3,48 luni în grupul tratat cu nivolumab comparativ cu 2.83 luni în grupul tratat cu docetaxel, rezultând o diferență de aproximativ 19 zile (p <0,0004).
Întregul raport de evaluare al ANM, aici.
În cazul aprobării pentru tratamentul carcinomului cu celule renale, nivolumab a fost comparat în studiile clinice cu everolimus.
Studiul clinic CA209025 a inclus pacienți diagnosticați cu carcinom renal cu celule clare, avansat sau metastatic, pretratați (1-2 tratamente angiogenice și nu mai mult de 3 terapii sistemice) cu scor KPS ≥ 70%. Pacienții au fost împărțiți în două grupuri:
- 410 pacienți au fost tratați cu Nivolumab 3mg/kg i.v. la 2 săptămâni;
- 411 pacienți au primit everolimus 10 mg/zi p.o.
Rata de răspuns obiectiv s-a dovedit superioară după administrarea de nivolumab comparativ cu everolimus: 25,1% versus 5,4%.
Întregul raport de evaluare al ANM, aici.
Nivolumab este un așa-numit checkpoint inhibitor, conceput pentru a valorifica în mod unic propriul sistem imunitar al organismului cu scopul de a ajuta la restabilirea răspunsului imun antitumoral.
La acest moment, este în desfășurare și un contract cost-volum pentru nivolumab ca tratament pentru pacienții români cu melanom malign metastatic.
De asemenea, este posibilă încheierea, până la sfârșitul anului, a unui alt contract cost-volum, pentru pembrolizumab în linia I și linia a II-a a NSCLC, medicamentul primind aprobarea ANM (Agenția Națională a Medicamentului) săptămâna trecută pentru includerea condiționată pe lista medicamentelor compensate.

