ANALIZĂ. 2.004 imunoterapii se află în dezvoltare, în 3.024 de studii clinice pentru 303 tipuri de cancer
Aproximativ 8,8 milioane de decese sunt atribuite cancerului în fiecare an. Imuno-oncologia a demonstrat că în cazul cancerului apărarea este cel mai bun atac. Tratarea cancerului prin stimularea propriului sistem imun să atace celulele maligne poate oferi o calitate a vieții incomparabilă cu cea garantată prin chimioterapie, radioterapie sau chirurgie.
Pentru pacienții cu cancer, în prezent există cele mai multe medicamente imuno-oncologice aprobate și în stadii experimentale. Cea mai mare analiză care ne arată unde a ajuns imuno-oncologia astăzi a fost realizată de Cancer Research Institute (CRI).
Ce avem în acest moment? Foarte multe date. Foarte multe întrebări. Foarte multe șanse. Și din ce în ce mai multe substanțe inovatoare care sunt aprobate într-un ritm fără precedent.
- 2004 imunoterapii sunt în proces de dezvoltare sau au apărut deja pe piață în întreaga lume cu indicații în 303 tipuri de cancer.
- 3042 de studii evaluează aceste terapii
- 864 de companii sunt implicate
- 17 tipuri de cancer au deja cel puțin o imunoterapie ca opțiune de tratament aprobată
Explozia de numere încurajatoare nu este, însă, o garanție a faptului că aceste terapii vor marca începutul sfârșitului pentru cancer. Conform analizei CRI, cursa pentru descoperirea tratamentului ideal pentru cancer este ținută pe loc de studii clinice care repetă, lipsa de colaborare dintre instituții, modele invechite ale studiilor, studii unicentrice. Este nevoie de o SCHIMBARE în modul în care cercetăm cancerul pentru că în final scopul este comun – EFICIENȚA.
Pe scurt, cum arată I-O la inceput de 2018…
- 940 de medicamente imuno-oncologice aflate în studii clinice
- 1.064 de medicamente în faza de testări preclinice
- 344 de vaccinuri pentru cancer fie în stadiul de studiu clinic fie disponibile deja pe piață
- în ultimii 3 ani au primit aprobări cinci inhibitori ai punctelor de control (checkpoint inhibitors), două noi terapii celulare (având ca țintă CD19) și un anticorp bispecific îndreptat împotriva moleculei CD3
- 244 de studii clinice care evaluează eficacitatea terapiilor celulare în tratarea cancerului sunt în derulare în prezent
- 99 de substanțe imunomodulatoare ce țintesc celulele T sunt pe piață sau în curs de dezvoltare
- Opdivo se preconizează a fi numărul 2 la nivel mondial în materie de vânzări în următorii ani
- 291 de terapii CAR-T diferite identificate, dintre care 162 sunt testate clinic
- 5 agenți PD-1/PD-L1 au fost aprobați în prezent însă există aproximativ 1.502 studii care evaluează aceste substanțe
- toate cele 26 de terapii imuno-oncologice aprobate în prezent sunt deținute de companii farmaceutice
Dintre cele 2.004 medicamente I-O aflate în dezvoltare, conform datelor din în septembrie 2017, 940 erau în studii clinice pe subiecți umani sau medicamente aprobate după ce studiile au fost încheiate. Restul 1.064 de medicamente erau în faze de testări preclinice.
Aceste medicamente țintesc 303 tipuri SPECIFICE de cancer. Pentru cele 940 de medicamente aflate în faze de cercetare, CRI a identificat 3.042 studii intervenționale în derulare care includ 577.076 pacienți, pentru evaluarea acestor substanțe.
Din numărul impresionat de substanțe I-O experimentale doar 26 au fost aprobate până în septembrie 2017. 17 tipuri de cancer au cel puțin o imunoterapie ca opțiune de tratament.
Primul a fost interferonul alfa în 1986 pentru leucemia cu celule paroase.
Încă de acum 100 de ani, începeau să de contureze principiile imuno-oncologiei. Chirurgul oncolog William Coley (supranumit și tatăl imunoterapiei) a introdus specii de Streptococ la pacienții cu boli maligne precum sarcom, limfom sau carcinom testicular obținând rezultate încurajatoare, dar ulterior s-a lovit de limitările de înțelegere ale mecanismelor, specifice vremurilor. El este printre primii care au făcut observații asupra modului în care sistemul imunitar poate fi „antrenat” să lupte împotriva cancerului.
Un alt moment istoric a fost anul 2011 când Bristol-Myers-Squibb a primit aprobarea pentru medicamentul Yervoy (ipilimumab), un checkpoint inhibitor, utilizat în cazul melanomului avansat.
Un alt CI dezvoltat tot de BMS, Opdivo (nivolumab) se preconizează a fi numărul 2 la nivel mondial în materie de vânzări în următorii ani.
În ultimii 3 ani au primit aprobări cinci CI (care țintesc fie PD-1 fie PD-L1), două noi terapii celulare ( având ca țintă CD19) și un anticorp bispecific îndreptat împotriva moleculei CD3.
CRI a identificat 344 de vaccinuri pentru cancer fie stadiul de studiu clinic fie disponibile deja pe piață. Acestea au indicații atât pentru prevenirea cancerului cât și pentru a trata cazurile deja existente.
Terapii celulare
244 de studii clinice care evaluează eficacitatea terapiilor celulare în tratarea cancerului sunt în derulare în prezent. Acest tip de terapie presupune injectarea de celule modificate, de exemplu limfocite T programate să atace țesturile transformate malign. Kymriah este prima terapie celulară, dezvoltată de Novartis și aprobată în august 2017 pentru tratamentul leucemiei limfobalstice acute cu precursori ai celulelor B (ALL). În luna octombrie a urmat aprobarea unei alte substanțe din această clasă, produsă de Gilead Sciences, Yescarta, cu indicații în tratarea limfomului cu celule B mari.
99 de substanțe imunomodulatoare ce țintesc celulele T sunt pe piață sau în curs de dezvoltare. Alte 170 de substanțe aflate în studii țintesc alte celule imune sau micromediul din jurul tumorii.
Terapiile celulare CAR-T, în rapidă creștere. China, pe primul loc
Limfocitele T ale pacientului pot fi modificate prin tehnici complexe de biotehnologie astfel încât să atace celulele canceroase. Aceste celule imune se preiau din sângele bolnavului și li se adaugă un receptor special care se leagă de anumite proteine de la suprafața celulelor maligne. Receptorul special se numește chimeric antigen receptor (CAR).
S-au înregistrat rate de remisiune completă de până la 90% la adulți și copii tratați prin terapie CAR-T pentru leucemie limfocitară acută (ALL).
Terapia CAR-T a demonstrat rezultate fără precedent. 291 de terapii CAR-T diferite identificate iar 162 sunt testate clinic. CD-19 este cea mai frecventă țintă pentru aceast tratament folosită în prezent – 56 de terapii sunt incluse în studii clinice.
Cele mai multe sunt dezvoltate de companii sau centre de cercetare din China. 98 de substanțe aflate în fază clinică de cercetare sunt deținute de 46 de companii din China comparativ cu cele 51 de terapii CAR-T deținute de 22 de companii din SUA.
Cum au evoluat terapiile cu inhibitori PD-1/ PD-L1?
5 agenți PD-1/PD-L1 au fost aprobați în prezent însă există aproximativ 1502 studii care evaluează aceste substanțe.
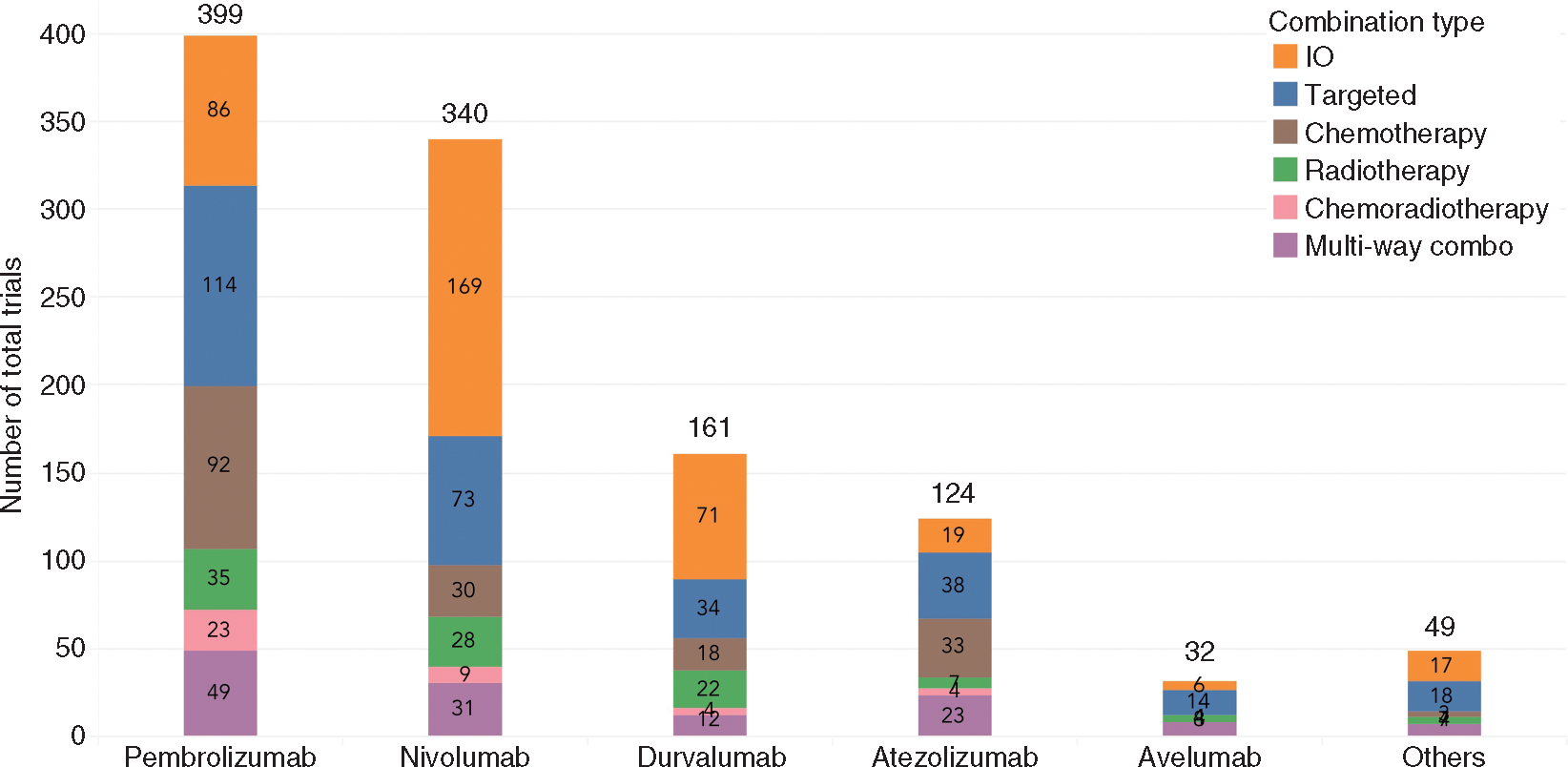
Dintre acestea, 1.105 examinează combinațiile dintre PD-1/PD-L1 și alte imunoterapii, terapii țintite, chimioterapie, radioterapie. Doar 46 de trialuri care studiază combinații terapeutice includ substanțe care nu au fost încă aprobate. Doar în 2017 au fost inițiate 469 de studii noi, având ca țintă includerea a peste 50.000 de pacienți.
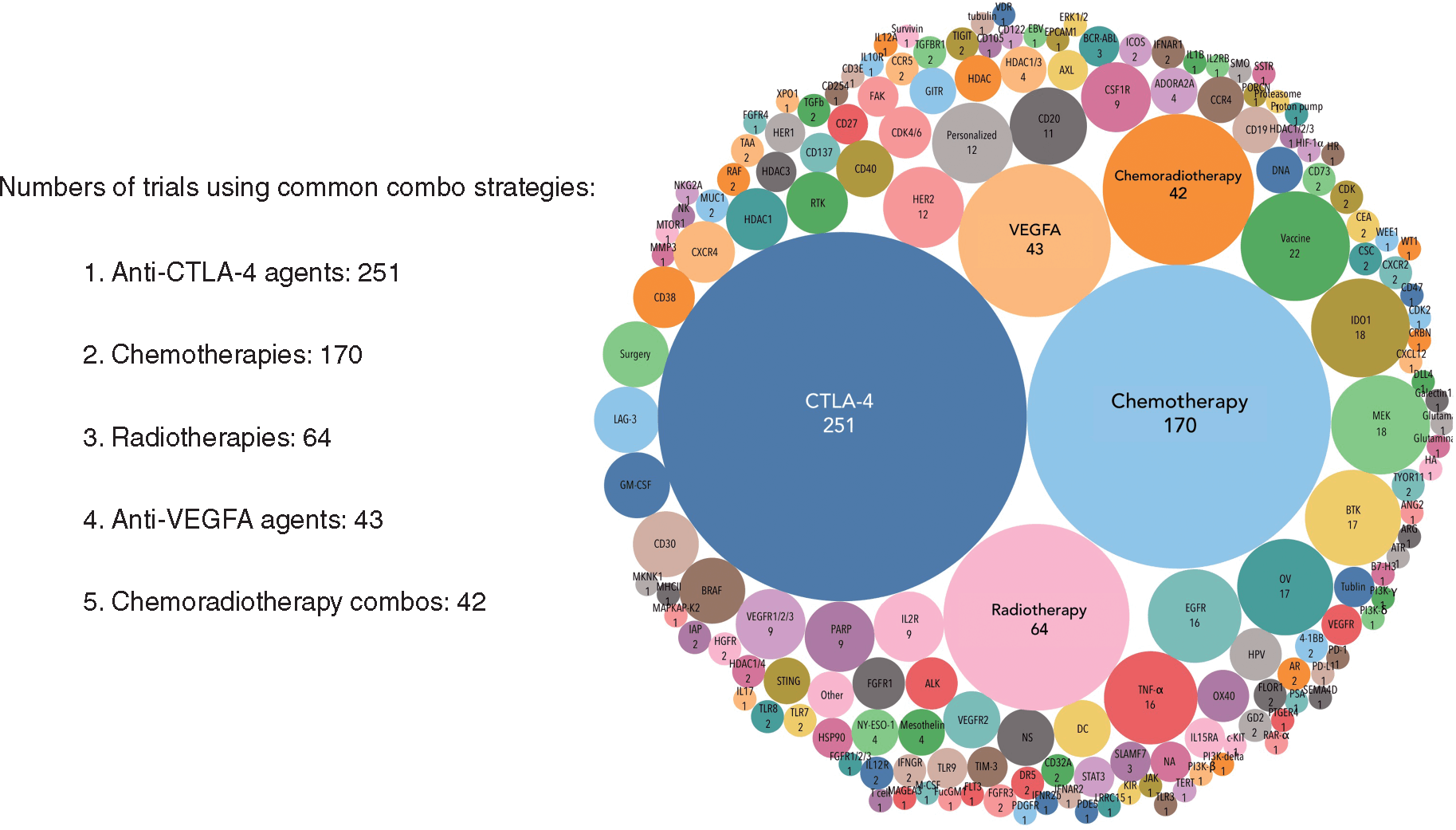
Mai mult înseamnă mai bine în acest caz?
Este evident că domeniul imuno-oncologiei este în plină expansiune, în fiecare zi apar terapii experimentale promițătoare, actualizări de la conferințe notabile în oncologie, articole din jurnale științifice, etc.
Ce ar trebui să înțeleagă clinicienii din toate datele acumulate? Care este cea mai bună opțiune pentru pacienții lor?
CRI a declarat că toate datele sugerează că dezvoltarea imunoterapiilor este promițătoare și va oferi multe inovații care vor schimba standardul de tratament pentru multe tipuri de cancer. Totuși, specialiștii CRI adaugă despre cercetarea în I-O:
„Domeniul este foarte aglomerat, fragmentat și cu un număr mare de studii duplicate”
Studiile mici, inițiate de investigatori idependenți, care includ un număr redus de pacienți, ar putea explica această creștere semnificativă a studiilor din ultimii ani, dar și fragmentarea datelor obținute. Opinia CRI este că ar fi necesară o schimbare în designul studiilor clinice și încurajează colaborările dintre companiile biofarmaceutice și centrele de cercetare non-profit.
Pentru a organiza toată această colecție de date care apar continuu, este necesar ca un studiu să răspundă la cât mai multe întrebări. Apariția de substanțe terapeutice noi într-un ritm accelerat a crescut competiția în domeniul dezvoltării de medicamente. Trebuie să răspundem la cât mai multe întrebări cât mai repede.
KEYNOTE-001 este un bun exemplu. Cel mai mare studiu de fază I care a determinat două aprobări FDA – una pentru melanom și una pentru cancerul pulmonar non-microcelular. În plus, în același studiu a fost posibilă evaluarea și confirmarea biomarkerului PD-L1.
Care este viitorul cercetărilor în I-O?
Design-ul studiilor tradiționale are, evident, limitări. Studiile centrate pe un singur obiectiv și competiția dintre mai multe companii asupra unei singure ținte terapeutice, apariția unor rezultate din studii care se repetă – toate acestea indică nevoia acută de a pune accentul pe eficiență în lupta împotriva cancerului.
Într-o publicație realizată de FDA, s-a atras atenția asupra necesității unor studii care să poată răspundă la mai multe întrebări, studiile multicentrice fiind încurajate. Tipurile de studii clinice recomandate sunt de tip “umbrella” sau de tip “basket” sau platforme care să permită colaborarea dintre instituții și cercetători astfel încât inovația în tratarea cancerului să devină o realitate. 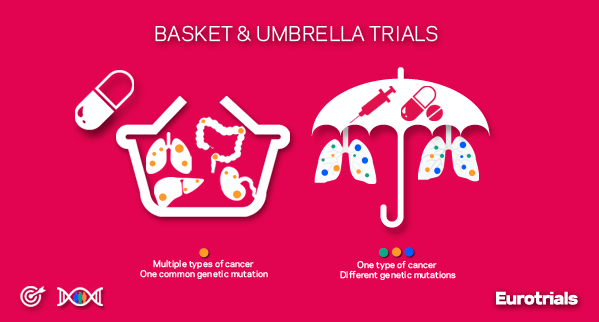
Sursa foto – EurotrialsAcest design este adoptat de multe companii farmaceutice însă medicamentele studiate sunt în general din producția proprie. Sectorul public și organizațiile non-profit ar putea avea un rol important în facilitarea colaborărilor.
De exemplu programul LUNG -MAP pentru studierea cancerului pulmonar reprezintă o colaborare a unor centre precum Friends of Cancer Research, Foundation for NIH, National Cancer Institute, the Southwest Oncology Group și multiple companii farmaceutice. Deși începutul a fost dificil, proiectul este acum un succes și un exemplu despre cum ar trebui să funcționeze colaborarea dintre instituții.

Articole similare
- ASCO: Terapia genică celulară CAR-T, cea mai importantă descoperire a anului 2017 în domeniul oncologiei
- Imuno-oncologia pentru toți: Despre folosirea imunoterapiilor pentru tratarea cancerului pulmonar în România
- #ESMO17. Prima biopsie lichidă care poate selecta pacienții ce răspund cel mai bine la imunoterapie
- Ghidul ASCO 2017 pentru cancerul pulmonar avansat: terapiile țintite și imunoterapia, noile standarde

