Bătălia #COVID19, în laborator. FDA: vaccinul Moderna a trecut în faza 2 de studiu clinic. În cât timp am putea avea un vaccin?
UPDATE 7 mai 2020: La data de 16 martie 2020, atât vaccinul Moderna Therapeutics (mRNA 1273), cât și vaccinul dezvoltat de CanSino Biological (Ad5-nCoV), începeau faza I de studii clinice pe oameni. La 10 aprilie, vaccinul CanSino intra în faza II de studiu clinic. Aproape o lună mai târziu, Moderna Therap. anunță că mRNA-1273 a primit aprobarea FDA (Food and Drug Administration) de începere a fazei II de studiu.
Conform comunicatului Moderna, se așteaptă ca faza II să înceapă în scurt timp, înrolând 600 de voluntari. Mai mult, compania finalizează protocolul pentru studiul de faza III, care urmează să înceapă la începutul acestei veri.
„Startul iminent al studiului de faza 2 este un pas crucial înainte, deoarece continuăm să avansăm dezvoltarea clinică a mRNA-1273, candidatul nostru pentru vaccinul SARS-CoV-2”, a declarat CEO-ul Moderna, Stéphane Bancel, într-un comunicat.
Bătălia #COVID19, în laborator. În cât timp am putea avea un vaccin? Vaccinul dezvoltat de BioNTech și Pfizer intră în studiu clinic pe oameni în Germania
UPDATE 22 aprilie: BioNTech și Pfizer au anunțat astăzi că autoritatea de reglementare germană, Paul-Ehrlich-Institut, a aprobat studiul clinic de faza 1/2 pentru vaccinul BNT162 pentru prevenirea infecției COVID-19. BioNTech și Pfizer au colaborat în dezvoltarea acestui vaccin. Este primul studiu clinic al unui vaccin anti COVID-19 care a început în Germania și face parte dintr-un program de dezvoltare globală. Pfizer și BioNTech vor desfășura, de asemenea, studii pentru BNT162 în Statele Unite, după aprobarea reglementării.
Pe 9 aprilie, Pfizer și BioNTech anunțau începerea studiilor umane spre finalul acestei luni. BioNTech colaborează și cu Fosun Pharma pentru dezvoltarea BNT162 în China.
La fel ca și primul vaccin care a intrat în studii umane, cel al Moderna Therapeutics, BNT162 este bazat pe ARN mesager, materialul genetic care este copiat din ADN și codifică proteinele.
Există patru formule ale BNT162, fiecare prezentând diferite formate ARNm și antigene țintă. Două dintre cele patru formule includ ARN ale cărui nucleozide sunt modificate chimic (modRNA), a treia include ARN care contine uridină (uRNA), iar a patra formulă utilizează ARNm auto-amplificator (saARN).
În prima parte a fazei 1/2 de studiu vor fi incluși aproximativ 200 de subiecți sănătoși cu vârste cuprinse între 18 și 55 de ani. Această fază are scopul de a determina doza optimă pentru studii ulterioare, precum și de a evalua siguranța și imunogenitatea vaccinului.
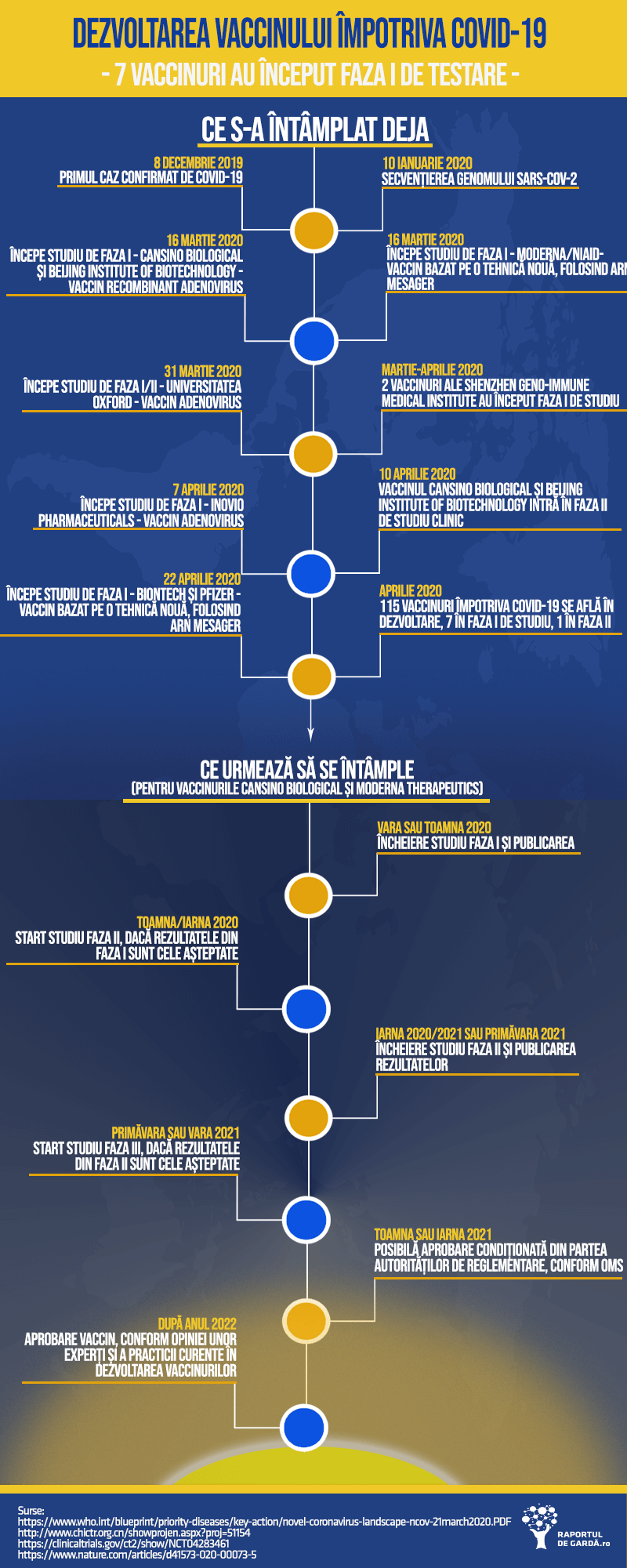
Bătălia #COVID19, în laborator. În cât timp am putea avea un vaccin? 6 vaccinuri se află în faza I de studiu pe oameni. Se așteaptă ca unul dintre ele să intre în faza II de studiu în curând
UPDATE 11 aprilie 2020: Conform unui articol din Nature, încă două noi vaccinuri împotriva COVID-19 se află în faza I de studiu pe oameni: LV-SMENP-DC al Shenzhen Geno-Immune Medical Institute și Pathogen-specific aAPC al aceluiași institut din Shenzhen.
Vaccinul LV-SMENP-DC (Lentiviral Minigene Vaccine), care conform clinicaltrials.gov a intrat în studiu clinic, cu aproximație, la data de 24 martie 2020 (pot exista variații ale acestei date), este un vaccin bazat pe celule dendritice modificate cu un vector lentiviral care exprimă minigene sintetice bazate pe domenii ale proteinelor virale selectate; administrat cu limfocite T citotoxice specifice antigenului.
Vaccinul Pathogen-specific aAPC, care conform clinicaltrials.gov a intrat în studiu clinic la data de 15 februarie (nu se specifică data începerii fazei I), este bazat pe celule prezentatoare de antigen artificiale (aAPC) modificate cu vector lentiviral care exprimă minigene sintetice bazate pe domenii de proteine virale selectate.
De asemenea, conform unui raport al CanSino Bio, vaccinul lor, Ad5-nCoV (vaccin recombinant adenovirus), urmează să intre „curând” în studiul de faza II, la doar 3 săptămâni de la începerea studiului de faza I (aproximativ 16 martie). Înscrierea virtuală în studiul de faza 2 a început deja, punând CanSino înaintea tuturor celorlalți candidați.
Toate cele trei vaccinuri menționate mai sus sunt de nouă generație, obținute prin tehnologii complexe. Conform aceluiași articol din Nature, o caracteristică importantă în peisajul de cercetări și dezvoltări ale vaccinurilor pentru COVID-19 este reprezentată de gama variată a platformelor tehnologice evaluate, incluzând acizii nucleici (ADN și ARN), particule asemănătoare virusului, peptide, vector viral (replicativ și non-replicativ), proteine recombinante, virusuri vii atenuate și virusuri inactivate. Multe dintre aceste platforme nu se numără în prezent printre bazele vaccinurilor deja autorizate, dar experiența în domenii precum oncologia încurajează dezvoltatorii să exploateze oportunitățile noi, pentru o viteză crescută de dezvoltare și fabricație.
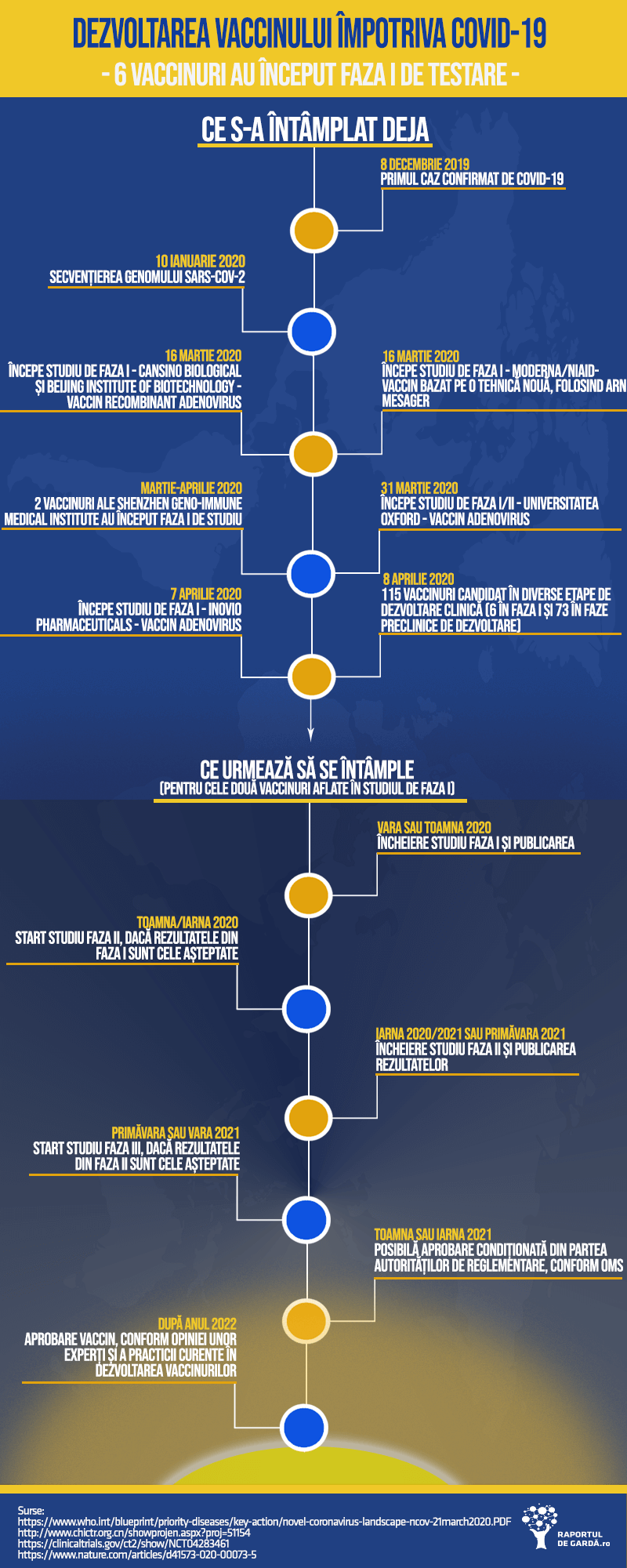
UPDATE 7 aprilie 2020: Bătălia #COVID19, în laborator. În cât timp am putea avea un vaccin? Al patrulea studiu de faza I pe oameni a început
Al patrulea vaccin pentru prevenirea infecției COVID-19 intră în faza I de testare umană – vaccinul INO-4800, candidatul Inovio Pharmaceuticals a primit aprobarea Food and Drug Administration pentru începerea demersurilor. Ieri, 6 aprilie, a început recrutarea voluntarilor sănătoși și a fost administrată prima doză de vaccin.
Studiul de faza I va înscrie până la 40 de voluntari adulți sănătoși din Philadelphia (care vor primi vaccinul în cadrul Facultății de Medicină Perelman, Universitatea din Pennsylvania) și Kansas City (care vor primi doza de vaccin la Centrul pentru Cercetări Farmaceutice). Fiecare participant va primi două doze de INO-4800 la interval de patru săptămâni, iar răspunsurile imune inițiale și datele de siguranță din studiu sunt așteptate până la sfârșitul verii. Datele preclinice au arătat rezultate promițătoare în ceea ce privește răspunsul imunitar pe mai multe modele animale.
De asemenea, rezultatele preclinice pentru vaccinul împotriva COVID-19 al INOVIO au fost în concordanță cu rezultatele studiului finalizat de faza 1 pentru vaccinul contra Sindromului respirator din Orientul Mijlociu (MERS), cauzat de un alt tip de coronavirus, în care vaccinul ADN al INOVIO a fost bine tolerat și a indus niveluri ridicate de răspuns la anticorpi în cazul a 95% dintre subiecți, generând răspunsuri mediate de celulele T la aproape 90% dintre participanții la studiu. Răspunsul de durată la anticorpi a fost menținut până la 60 de săptămâni în cazul vaccinului anti-MERS.
Printre principalii sponsori Inovio Pharmaceuticals se numără și Fundația Bill și Melinda Gates. Așadar, implicarea fundației în dezvoltarea unui vaccin există, însă de partea pozitivă a baricadei, deși teoriile conspirației acordau o altă implicare acestora.
UPDATE 1 aprilie 2020
Un nou vaccin împotriva COVID-19 intră în faza de testare umană – a început recrutarea primilor voluntari sănătoși. Vaccinul se numește ChAdOx1 nCoV-19 și va fi testat în cadrul unui studiu multicentric de fază I / II, randomizat, controlat placebo, pe un număr de 510 voluntari sănătoși din Marea Britanie, cu vârste cuprinse între 18 și 55 de ani. Studiul va fi condus de Institutul Jenner al Universității Oxford și Grupul de vaccinuri al acesteia. Oficial, faza I/II a studiului a început pe 31 martie 2020 și se va încheia în mai 2021.
Dezvoltat inițial pentru a viza MERS (Middle East Respiratory Syndrome), vaccinul se bazează pe un vector adenoviral și pe proteina S (Spike) a SARS-CoV-2. În prezent, acesta este fabricat în Departamentul de Biomanufacturare Clinică a Universității Oxford și va fi gata în câteva săptămâni pentru începerea testării propriu-zise.
Dezvoltat la Universitatea din Oxford, vaccinul este o versiune sigură a unui adenovirus. Acesta a fost modificat astfel încât să nu se poată reproduce în corp, fiindu-i adăugată secvența genetică necesară pentru codificarea proteinei Spike. Odată injectat (intramuscular) în organism, vaccinul va facilita formarea de anticorpi împotriva proteinei Spike.
27 martie 2020: Mobilizare fără precedent a comunității științifice și a autorităților de reglementare pentru a descoperi un vaccin sigur și eficace împotriva Covid-19, într-un timp cât mai scurt. Premisele sunt favorabile, startul a fost rapid, dar trebuie cu toții să știm că drumul poate fi mai lung decât ne-am dori, dar totuși mai scurt decât suntem obișnuiți. Unde suntem acum?
Genomul SARS-CoV-2, secvențiat rapid
Pe 8 decembrie 2019, în China era diagnosticat primul pacient cu o formă atipică de pneumonie, boală care avea să fie ulterior denumită drept COVID-19, de către Organizația Mondială a Sănătății. După o lună, pe 10 ianuarie 2020, agentul cauzal al bolii, virusul SARS-CoV-2, a fost descifrat, iar genomul său a fost publicat două zile mai târziu. Întreaga comunitate de cercetare, din Asia, SUA și Uniunea Europeană, a început să folosească informația genomică pentru a inventa și valida teste de diagnostic pentru boală, dar și pentru a realiza un vaccin sau pentru a identifica tratamentul potrivit.
În privința diagnosticului, lucrurile s-au mișcat foarte repede, iar în acest moment sunt sute de laboratoare publice și private, în întreaga lume, care au dezvoltat teste bazate pe determinarea prin tehnica numită real time PCR. Pentru dezvoltarea vaccinului și descoperirea unui tratament etiologic, avansul nu este însă la fel de mare, la acest moment. Dar avem totuși motive de optimism.
Primele două studii pe oameni, inițiate foarte repede
Și, totuși, am asistat deja la o premieră absolută din punctul de vedere al dezvoltării unui vaccin. În numai 42 de zile de la momentul publicării structurii genetice a SARS-CoV-2, primele două vaccinuri, unul în SUA și altul în China, au intrat în studii clinice de faza I pe oameni. Obiectivul acestor studii de faza I constă în evaluarea siguranței și a tolerabilității vaccinului, nu în studierea eficacității acestuia. Eficacitatea va fi evaluată în studiile de faza II și III, dacă rezultatele studiilor de faza I sunt favorabile. În afara acestor două vaccinuri, Organizația Mondială a Sănătății a contabilizat alte 48 de vaccinuri candidat, acestea din urmă aflându-se însă într-un stadiu de dezvoltare incipient, și anume faza pre-clinică, de laborator, care precede studiul de fază I pe oameni.
Cum se desfășoară un studiu clinic
Studiile clinice în cazul vaccinurilor au loc în 3 faze de cercetare:
- Faza I implică un număr mic de voluntari (20-50 de persoane) și are scopul de a evalua siguranța, a determina dozajul și de a identifica posibilele reacții adverse.
- Faza II a studiilor clinice implică un număr de 100-300 de voluntari, scopul fiind analizarea mai în detaliu a siguranței și imunogenității, a dozajului necesar și identificarea calendarului de administrare.
- Fază III a studiilor clinice include 3.000 – 50.000 de voluntari, fiind ultima fază pentru evaluarea siguranței și eficacității vaccinului la scară largă și analizarea administrării concomitent cu alte vaccinuri și tratamente.
După ce se încheie studiul de faza III, pe baza datelor colectate și analizate, vaccinurile trebuie aprobate de agențiile de reglementare, mai precis de Agenția Europeană a Medicamentului în Uniunea Europeană, după care vaccinul poate fi produs pe scară largă și astfel poate ajunge la populație, fiind recomandat pentru utilizare de către medici.
Durata medie de dezvoltare: 12-15 ani
Dezvoltarea unui vaccin este un proces complex și de durată, care diferă de dezvoltarea medicamentelor convenționale. În mod normal, perioada de dezvoltare a unui vaccin este de 12-15 ani. Vaccinurile sunt destinate utilizării la persoane sănătoase, cu scopul de a preveni apariția bolilor, în timp ce medicamentele convenționale sunt orientate către tratamentul unei afecțiuni. Studiile clinice pentru demonstrarea eficacității unui vaccin se concentrează pe demonstrarea capacității acestuia de a preveni boala, cu minimum de reacții adverse, ceea ce implică necesitatea înrolării unui număr mai mare de subiecți decât în cazul studiilor pentru medicamente tradiționale.
Cum am putea avea vaccinul mai repede?
Cu toate acestea, Organizația Mondială a Sănătății a avansat un termen extrem de ambițios pentru apariția primului vaccin aprobat: 18 luni. Estimările vin în urma experienței acumulate deja de companiile farmaceutice care dezvoltă astfel de vaccinuri, în lupta cu virusuri similare precum MERS, SARS, gripă sau Hepatită C. Una dintre cheile importante pentru scurtarea timpului necesar dezvoltării ține de avansul tehnologic și folosirea potențialului științelor omice, la care se adaugă colaborarea strânsă dintre dezvoltatorii vaccinului și autoritățile de reglementare, în cadrul unor programe dedicate de dezvoltare accelerată de soluții pentru COVID-19.
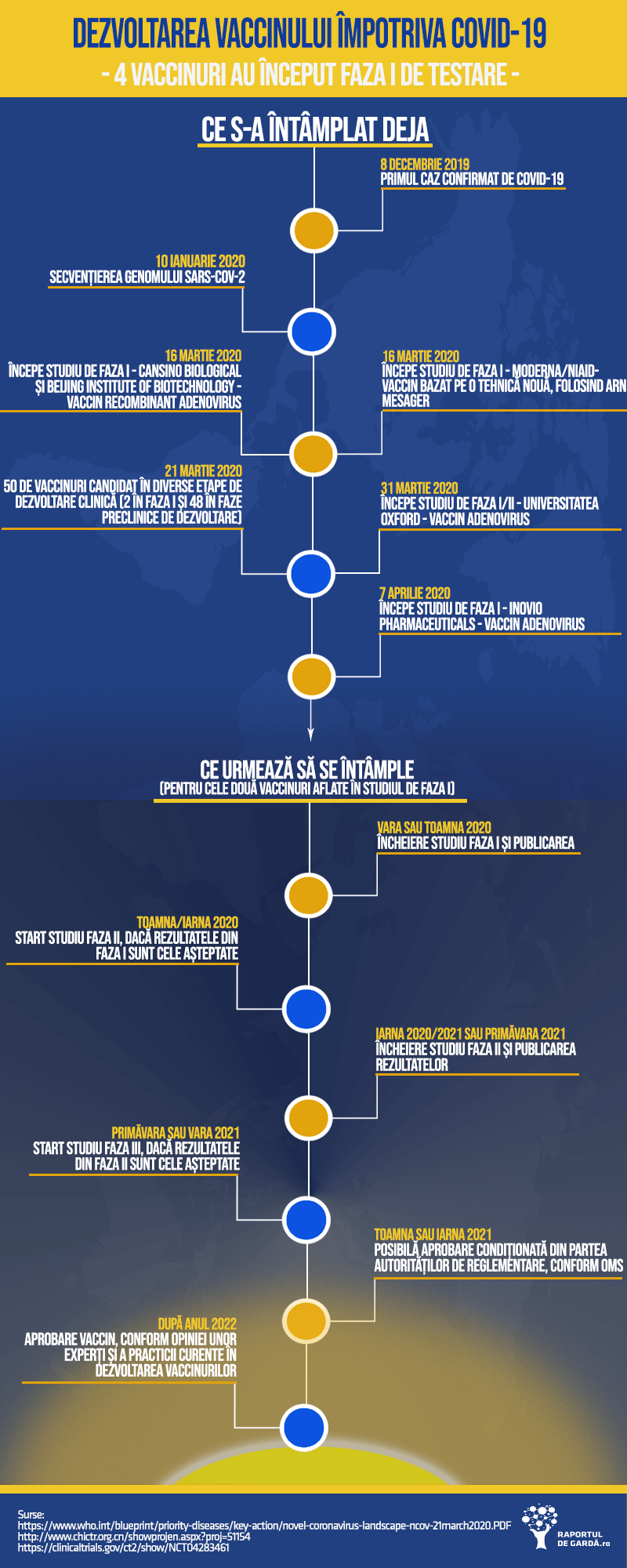
Sprijin pentru dezvoltarea vaccinurilor în UE
Comisia Europeană și Banca Europeană de Investiții au anunțat că vor sprijini financiar compania de vaccinuri CureVac pentru a extinde dezvoltarea și producerea unui vaccin împotriva coronavirusului. Sprijinul, sub forma unui împrumut de la BEI, cu o garanție din partea Comisiei Europene, va ajuta accelerarea programului de dezvoltare a vaccinurilor COVID-19, CureVac anunțând lansarea testelor clinice până în iunie 2020.
Există inițiative la nivel european, prin care toate resursele companiilor sunt puse împreună pentru a găsi cât mai repede soluții. Un exemplu practic al acestei colaborări este apelul 21, al Inițiativei privind Medicamentele Inovatoare (Innovative Medicines Initiative – IMI), care presupune o finanțare de 45 de milioane de euro pentru dezvoltare și cercetare de vaccinuri și medicamente împotriva COVID-19. 13 companii au răspuns până acum acestui apel și lucrează intens, la nivel european.
Articolul face parte din campania #NuNeOprim – Bătălia Covid-19 în laborator, realizată de Asociația Română a Producătorilor Internaționali de Medicamente în parteneriat cu RaportuldeGarda.ro.
Citește și:
- UPDATE 17 MARTIE. Vaccin împotriva COVID-19: A început faza I a studiului clinic pe oameni, cu două săptămâni înainte de data anunțată. Când ar putea fi disponibil pe scară largă? 37 de companii dezvoltă vaccinuri, în întreaga lume
- #COVID19. Taiwan controlează epidemia la numai 130 km de China continentală. Doar 216 de cazuri diagnosticate, în 3 luni. Cum a reușit?
- #COVID19. Analiza genomulului SARS-CoV-2: originea virusului și evoluția tulpinilor. Cum s-a transmis: liliac-pangolin-om




