ISTORIC. FDA aprobă prima terapie genică celulară (CAR-T) pentru leucemia limfoblastică acută cu precursori de celule B
FDA (Food and Drug Administration) a aprobat Kymriah (Tisagenlecleucel) pentru tratamentul pediatric și al tinerilor adulți (până la 25 de ani) care suferă de o formă de leucemie acută limfoblastică. Este primul medicament din categoria terapiilor CAR-T aprobat la nivel mondial.
„Deschidem o nouă etapă a inovației în domeniul medical, care are abilitatea de a reprograma propriile celule ale unui pacient pentru a ataca această formă de cancer mortală. Noile tehnologii ca terapiile genice și celulare au potențialul de a transforma complet medicina, oferindu-ne șansa de a trata sau chiar vindeca boli incurabile”, a declarat Comisarul FDA, Dr. Scott Gottlieb.
Kymriah este o terapie genică ce se bazează pe modificarea celulară și tratează pacienții de până la 25 de ani cu leucemie acută limfoblastică (ALL) cu precursori de celule B, țintind în primul rând cazurile care nu au răspuns la terapia inițială (15-20% dintre cazuri).
Siguranța și eficacitatea medicamentului au fost demonstrate într-un studiu multicentric, efectuat pe un număr de 63 de pacienți (copii sau tineri) cu leucemie limfocitară acută cu precursori de celule B, refractară sau recurentă. Procentul total de remisie la 3 luni a fost de 83%.
ALL este un tip de cancer în care corpul uman produce limfocite anormale. Boala progresează rapid și este cel mai comun tip de cancer întâlnit la copii în Statele Unite.
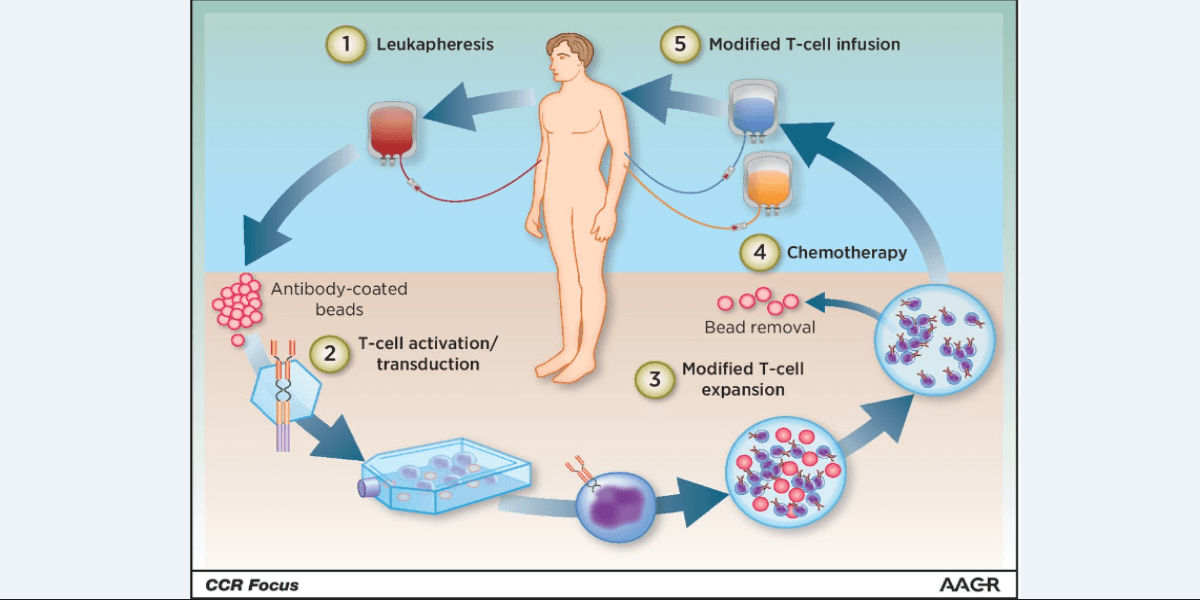
Fiecare doză de Kymriah reprezintă un tratament personalizat, creat pe baza propriilor celule T ale organismului pacientului. Celulele T sunt colectate și trimise într-un centru ultra-specializat, unde sunt modificate genetic prin includerea unor noi gene care conțin codificarea pentru proteine specifice (un receptor al antigenului chimeric – CAR), care direcționează celulele T pentru a ținti și elimina celulele leucemice care au pe suprafața lor antigenul CD19. Odată modificate, celulele CAR-T sunt introduse înapoi în organismul pacientului pentru a omorî celulele canceroase.
Tratamentul cu Kymriah poate produce efecte adverse grave, putând declanșa sindromul de eliberare a citokinei (CRS), care este un răspuns sistemic al organismului la proliferarea celulelor CAR-T (manifestările sunt asemenănătoare cu cele ale gripei) sau alte evenimente neurologice. Alte efecte adverse severe pot fi infecțiile, hipotensiunea, febra, cedarea rinichilor și hipoxie. Cele mai multe dintre simptome apar în primele 22 de zile de la administrare. Deoarece antigenul CD19 este de asemenea prezent pe suprafața celulelor B normale, iar Kymriah va distruge și aceste celule B care produc anticorpi, există riscul de infecții ale organismului pe o durată prelungită.
FDA a aprobat de asemenea și utilizarea medicamentului Actemra (tocilizumab) pentru tratarea pacienților cu vârste mai mari de 2 ani ce prezintă CRS potențial fatal. În teste clinice pe pacienți cu celule CAR-T, 69% dintre cazuri au avut parte de remisii totale la 2 săptămâni de la administrarea unei doze sau două de Actemra.
Din cauza riscurilor, prescrierea și administrarea de Kymriah sunt decise în urma unei proceduri speciale de evaluare a riscurilor și atenuare a daunelor (REMS). FDA obligă ca spitalele si clinicile implicate în dispensarea de Kymriah să dețină certificate speciale, iar personalul lor să fie instruit corespunzător, astfel încât să identifice cazurile de CRS și să reacționeze corect în fața lor. În plus, instituțiile trebuie să se asigure că pacienților li se administrează Kymriah doar după ce s-a asigurat existența în stoc a tocilizumab. Pacienții trebuie informați despre toxicitatea neurologică din urma administrării și trebuie instruiți să se întoarcă urgent la instituția unde s-a urmat tratamentul, în cazul apariției efectelor secundare.
În continuare, pentru a evalua pe termen lung siguranța medicamentului, compania farmaceutică producătoare – Novartis, este obligată să efectueze un studiu observațional care îi implică pe pacienții tratați cu Kymriah.
Mai multe despre terapia CAR-T, aici.

