Utilizarea tehnologiei de editare genomică CRISPR în strategia pentru combaterea SARS-CoV-2 și a virusurilor gripale
Încă din luna martie omenirea se confruntă cu pandemia cauzată de virusul SARS-CoV-2 și până la momentul actual nu există încă un vaccin sau tratament farmacologic eficient dovedit științific împotriva noului coronavirus. De aceea, studiile se îndreaptă asupra noilor tehnologii, în căutarea unei metode eficiente de a combate această infecție.
De curând, cercetătorii de la Universitatea Stanford, din California, au elaborat o strategie denumită PAC-MAN (Prophylactic Antiviral CRISPR in huMAN cells) pentru inhibiția virală. Această metodă poate degrada eficient ARN-ul provenit din secvențele SARS-CoV-2 și ale virusurilor vii influenza A (IAV) la nivelul celulelor epiteliale pulmonare umane.
În cadrul acestui studiu s-a utilizat metoda CRISPR-Cas13 care se bazează pe identificarea și distrugerea în mod specific a unor regiuni virale înalt conservate, vizând un spectru mai larg de amenințări virale, inclusiv toate tulpinile de coronavirus.
Pandemia COVID-19 cauzată de virusul SARS-CoV-2 subliniază necesitatea unei abordări antivirale care să poată ținti virusuri pentru care nu există încă vaccinuri sau tratamente farmacologice eficiente. În ultimele decenii, multiple variante ale coronavirusurilor, provenite din rezervoare animale, au reușit să infecteze omul, cauzând un număr semnificativ de decese. Coronavirusurile care determină COVID-19, SARS și MERS sunt capabile de transfer de la diverse animale (vectori virali) la oameni, astfel că o strategie care să combată chiar și alte coronavirusuri care pot apărea în viitor ar fi o resursă neprețuită.
Un raport recent a evidențiat două tulpini ale SARS-CoV-2, L și S, cu diferite secvențe genomice care au potențialul de a evolua. Acest fapt subliniază necesitatea identificării unei strategii direcționată împotriva coronavirusurilor. (Strategie denumită “pan-coronvirus targeting”)
Analiza bioinformatică a arătat cum doar un grup de șase ghiduri ARN CRISPR (crARN) pot recunoaște mai mult de 90% dintre toate coronavirusurile. Odată cu dezvoltarea unui sistem sigur și eficient de administrare la nivelul tractului respirator, PAC-MAN are potențialul de a deveni o strategie importantă împotriva coronavirusurilor.
Această abordare a redus încărcătura virală în celulele epiteliale respiratorii, limitând replicarea virală. S-a demonstrat abilitatea acestei strategii în clivarea fragmentelor SARS-CoV-2 și de a reduce cantitatea de ARN viral a virusurilor Influenza A în celule epiteliale pulmonare umane.
Noul coronavirus aparține unei familiei de virusuri ARN care are potențialul de a infecta tractul respirator superior și inferior și cauza efecte citotoxice, inducând gazdei o inflamație mediată de citokine.
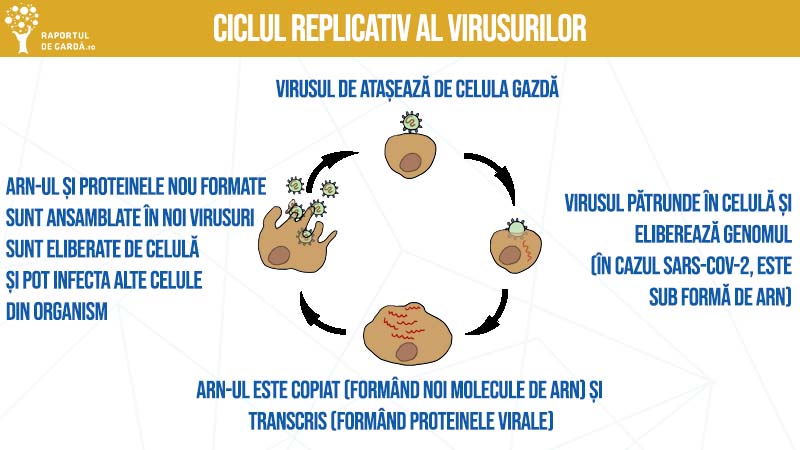
Ciclul de viață al SARS-CoV-2 este asemănător cu cel al altor coronavirusuri înrudite care cauzează SARS sau MERS. Astfel, virusul intră în celulă, eliberează genomul ARN în citoplasmă. Acesta va fi transcris în vederea producției de proteine virale și se va multiplica, iar catena ARN va servi ca matriță pentru sinteza de noi copii virale.
Cum funcționează CRISPR-Cas13 și sistemul PAC-MAN?
În timp ce majoritatea vaccinurilor se bazează pe pregătirea sistemului imun al individului în recunoașterea proteinelor virale și inhibiția pătrunderii acestora în celule, această alternativă antivirală folosește sistemul CRISPR-Cas13 pentru a recunoaște și degrada genomul viral intracelular. În plus, PAC-MAN diferă de studiile anterioare întrucât își propune să dezvolte o strategie pentru a ținti simultan mai multe specii ale acestei familii virale pentru a oferi o protecție largă (așa-numita “pan-coronavirus protection”).
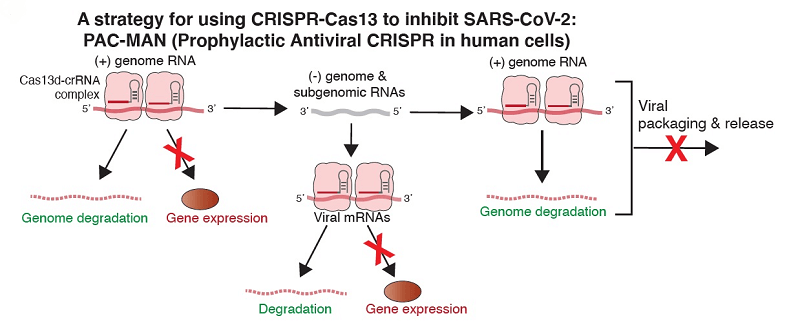
Strategia PAC-MAN este o formă de intervenție genetică cu scopul țintirii SARS-CoV-2, virusului Influenza A și cu potențial asupra tuturor coronavirusurilor. Aceasta a utilizat o tehnologie bioinformatică de înaltă performanță pentru a defini regiunile virale înalt conservate identificate în rândul genomurilor secvențiate și ulterior pentru a crea tehnologia de editare genomică CRISPR-Cas13 pentru degradarea secvențelor virale.
Sistemul CRISPR/Cas13 este alcătuit din două componente esențiale: o secvență scurtă de ARN ghid (crARN), complementar cu secvența țintă, care se va atașa specific la ARN-ul viral și o enzimă, Cas13 (endonuclează), capabilă de a “tăia” catena ARN de interes.
În încercarea de a inhiba virusurile în celulele umane s-a utilizat o endonuclează recent descoperită, Cas13d, care are dimensiuni mici, este înalt specifică și are o activitate catalitică puternică. Deși nu este prima dată când este folosită în studii în încercarea de a ținti secvențe virale în celulele umane, aceasta a fost aleasă datorită proprietăților sale.
Prin vizarea diferitelor regiuni virale a aceluiași virus sau a diferitelor tulpini de coronavirus, acest sistem ar putea oferi protecție împotriva unor viitoare virusuri patogenice înrudite.
CRISPR-Cas13 provine dintr-un sistem antiviral adaptativ puternic al bacteriilor, capabil să protejeze celulele gazda de infecția cu bacteriofagi. Această metodă a fost reinterpretată în cazul strategiei PAC-MAN și activitatea endonucleazei Cas13d ghidată împotriva țintelor virale la nivelul celulelor umane. S-a demonstrat că acest lucru se poate realiza cu succes (acest sistem poate ținti și cliva eficient secvențele ARN ale fragmentelor SARS-CoV2 și IAV cu ajutorul unor crARN realizate corespunzător).
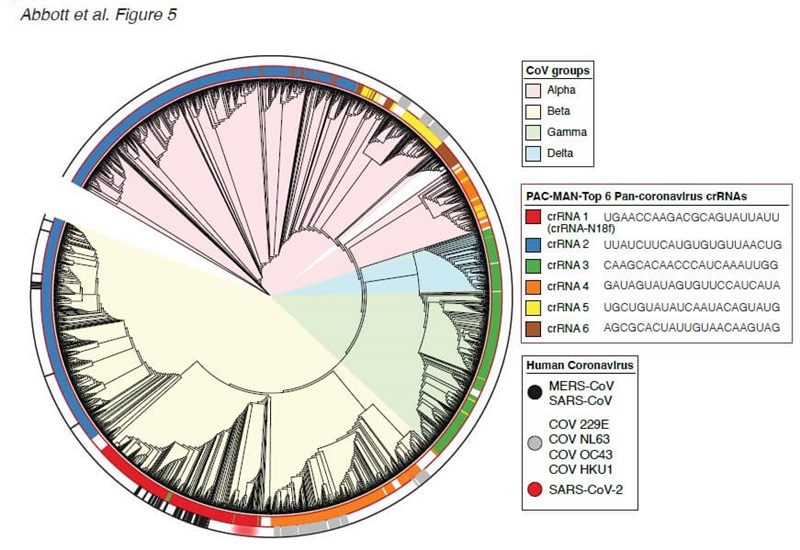
Astfel, au fost analizate toate genomurile cunoscute ale coronavirusurilor (peste 3000) pentru a identifica crARN posibile care ar putea ținti toate aceste genomuri virale. Din peste 6 miliaone de astfel de posibile instrumente, cu ajutorul unei analize bioinformatice, a fost selectat un număr minim de astfel de crARN care să poată ținti toate genomurile de coronavirus cunoscute.
S-a descoperit că doar două ghiduri crARN ținteau aproximativ jumătate din genomurile de coronavirus, inclusiv cele cauzatoare de COVID-19, SARS, MERS. De asemenea, 6 crARN au fost capabile să țintească 91% din genomuri, iar 22 de astfel de instrumente genomice acoperă toate coronavirusurile secvențiate.
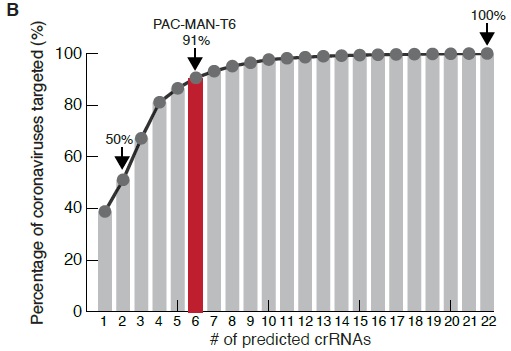
Abilitatea de a utiliza un număr mic de astfel de instrumente pentru a ținti pe larg majoritatea sau chiar toate coronavirusurile evidențiază unicitatea acestei metode în contrast cu abordările clasice farmacologice sau cu vaccinurile.
Deși există numeroase obstacole care trebuie depășite înainte ca această strategie să poată fi utilizată clinic, PAC-MAN are potențialul de a deveni o nouă strategie antivirală.
PAC-MAN – viitoare provocări
Este important de menționat faptul că PAC-MAN reprezintă o strategie antivirală care și-a dovedit capacitățile în laborator, dar că sunt necesari câțiva pași suplimentari importanți înainte de includerea acestuia în studii clinice.
De asemenea, din considerente ce țin de acces, nu a fost posibilă manipularea directă a virusului viu SARS-CoV-2, astfel încât s-a ales testarea strategiei PAC-MAN Cas13d asupra unei tulpini H1N1 a IAV, un virus ARN cu tropism similar pentru celulele epiteliale ale tractului respirator.
Următorul pas important este validarea eficienței și specificității secvențelor ghid crARN în inhibarea infecției celulelor respiratorii cu virusuri vii SARS-CoV-2.
În timpul testării strategiei PAC-MAN ca sistem profilactic a fost lansată ipoteza că PAC-MAN poate de asemenea să fie folosită pentru a reduce încărcătura virală după infecție, acest lucru fiind important de probat prin studii ulterioare.
Mai mult, după demonstrarea efectelor in vitro, cea mai importantă barieră în calea integrării clinice a PAC-MAN o reprezintă dezvoltarea unei metode eficiente și sigure de livrare a tratamentului in vivo către celulele pulmonare epiteliale umane.
În final PAC-MAN va necesita validarea în studii preclinice pe modele animale sau sisteme organoide pulmonare umane pentru testarea eficacității antivirale și a specificității.
Se estimează că acești pași importanți pot dura câțiva ani, astfel încât strategia PAC-MAN să nu poată interveni în controlul actualei pandemii, însă reprezintă un potențial enorm pentru viitoare amenințări virale.
Citește și:
- Bătălia #COVID19, în laborator. În cât timp am putea avea un vaccin? Vaccinul dezvoltat de BioNTech și Pfizer intră în studiu clinic pe oameni în Germania
- Bătălia #COVID19, în laborator. FDA: vaccinul Moderna a trecut în faza 2 de studiu clinic. În cât timp am putea avea un vaccin?
- Genomul coronavirusului SARS-CoV-2, secvențiat într-o lună de la apariția primului caz de boală. Ritmul cercetărilor este fără precedent – un vaccin ar putea fi dezvoltat în următoarele 3 luni

