Insuficiența cardiacă, un sindrom complex, multisistemic, nu doar o singură boală. Care sunt mecanismele implicate?
Modul în care este definită o boală stă la baza modului în care este gestionată de către medici și a modului în care sunt dezvoltate terapiile. Insuficiența cardiacă există de când au fost descrise primele boli și, știm de zeci de ani că nu este o singură boală. Mai degrabă, este un sindrom care cuprinde multe entități diferite; rezultă din multe etiologii și culminează cu incapacitatea inimii de a oferi un flux optim pentru a satisface nevoile metabolice ale organismului. În zilele noastre, insuficiența cardiacă (IC sau HF – heart failure) este una dintre cele mai frecvente cauze de spitalizare și deces, cu impact mare asupra resurselor sociale și economice (1).
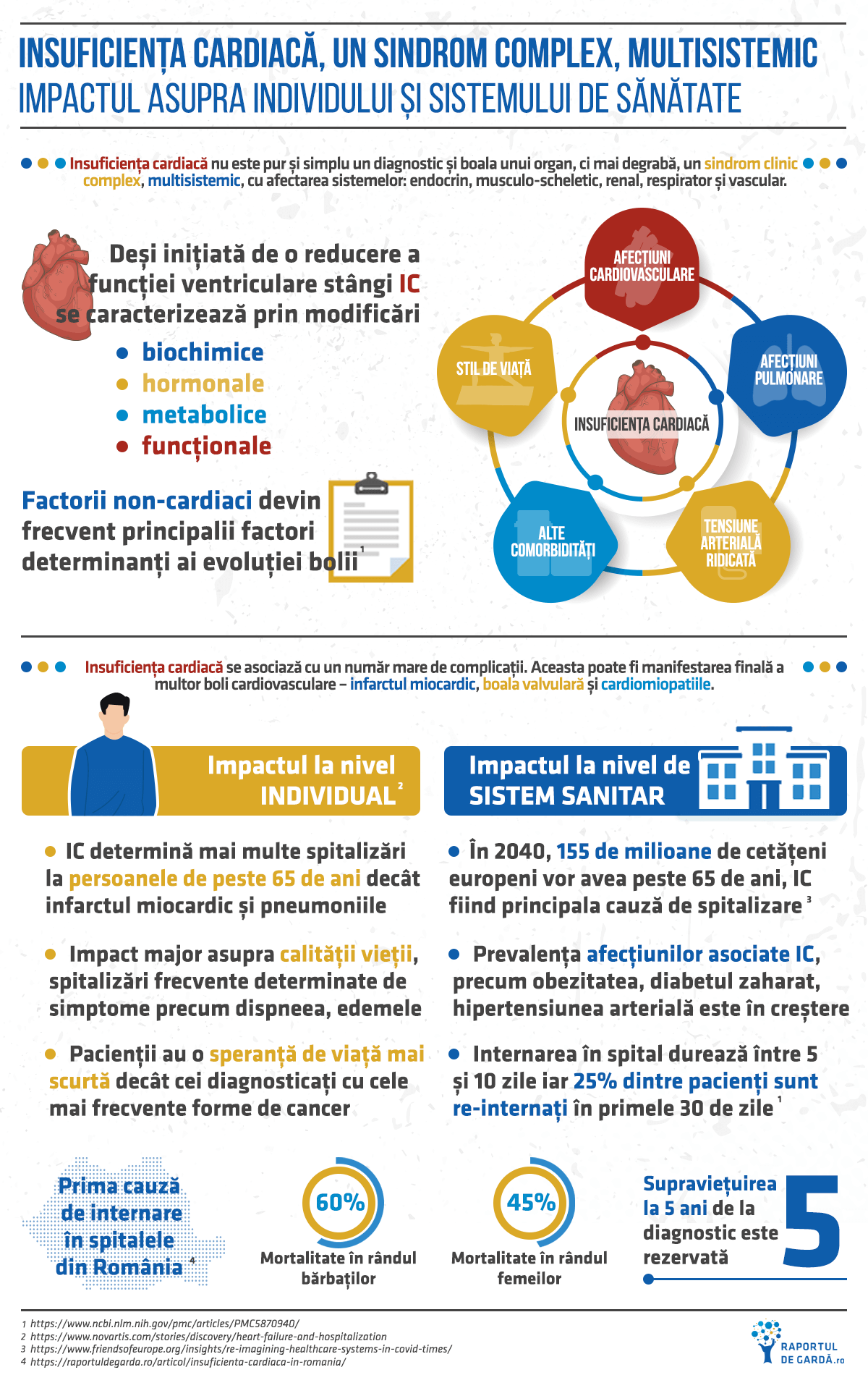
Sindromul insuficienței cardiace a fost descris pentru prima dată ca o epidemie emergentă în urmă cu aproximativ 25 de ani. Astăzi, din cauza creșterii și îmbătrânirii populației, numărul pacienților care suferă de IC este în creștere. Incidența s-a stabilizat și este chiar în scădere la unele populații, dar au fost observate tendințe opuse alarmante la persoanele relativ tinere, posibil legată de creșterea incidenței obezității. În plus, dovezile sugerează că numărul pacienților cu insuficiență cardiacă ar putea crește în țările cu venituri mici, care se luptă cu o povară dublă, a bolilor transmisibile și a afecțiunilor asociate cu un stil de viață de tip occidental. Aceste constatări, împreună cu observația că rata mortalității insuficienței cardiace scade mai puțin rapid decât în trecut, sugerează faptul că nu ne apropiem încă de sfârșitul epidemiei. Aproximativ un milion de persoane din România suferă de insuficiență cardiacă (4,7% din populație, conform studiilor). Îmbătrânirea populației și tratamentele noi au dus la creșterea duratei de viață, dar și la costuri mari legate de spitalizările repetate și de îngrijirea acestor bolnavi. Este prima cauză de internare în spitalele din România și continuă să aibă un impact foarte mare asupra sănătății, în ciuda progreselor terapeutice înregistrate în ultimele decenii. Supraviețuirea la 5 ani de la diagnostic este rezervată, cu o mortalitate de aproape 60% pentru bărbați și de 45% pentru femei (2).
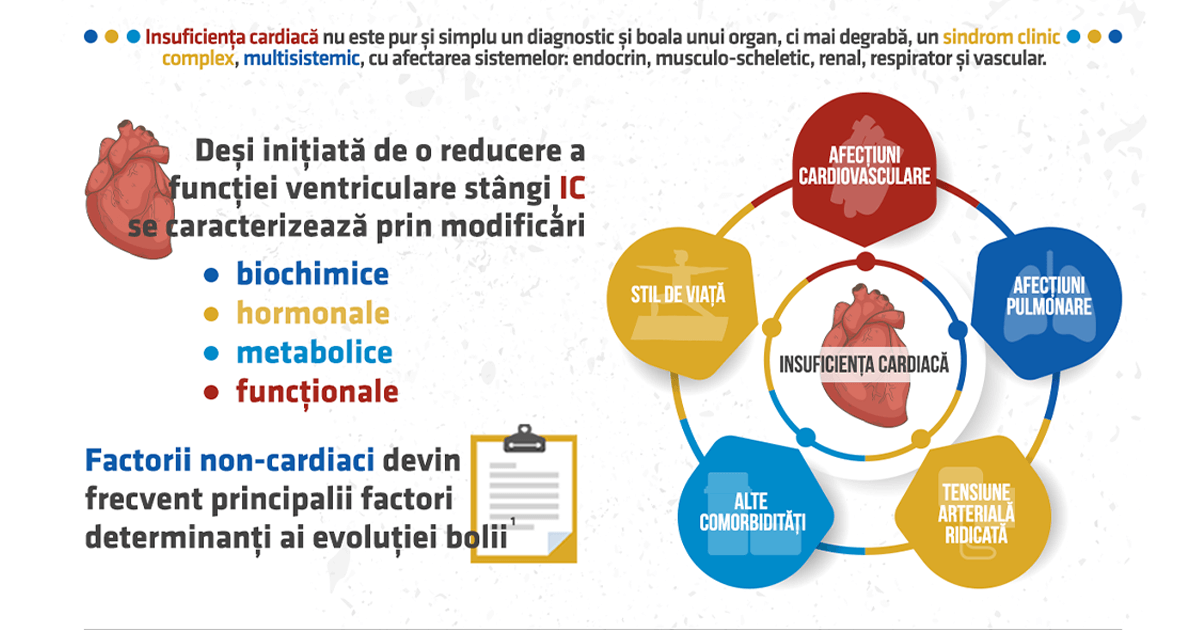
Dar insuficiența cardiacă nu este pur și simplu un diagnostic și boala unui organ, ci mai degrabă, un sindrom clinic complex, multisistemic, cu afectarea sistemelor: endocrin, musculo-scheletic, renal, respirator și vascular, cu impact variabil asupra morbidității și mortalității. Deși inițiată de o reducere a funcției ventriculare stângi, insuficiența cardiacă se caracterizează prin modificări substanțiale biochimice, hormonale, metabolice și funcționale. Factorii non-cardiaci devin frecvent principalii factori determinanți ai evoluției.
Clasificarea actuală insuficienței cardiace nu reflectă progresele științifice
În ultimele decenii, medicii s-au străduit să clasifice insuficiența cardiacă pentru a îmbunătăți înțelegerea acestui sindrom cu mai multe fețe și pentru a satisface cel mai bine nevoile pacienților. Plecând de la înțelegerea insuficienței cardiace ca o disfuncție mecanică a inimii, măsurarea funcției ventriculului stâng (VS) sub forma fracției de ejecție (FE) a fost considerat cel mai bun parametru pentru detectarea și gestionarea bolii. Insuficiența cardiacă a fost astfel clasificată inițial în două tipuri:
- IC cu fracție de ejecție redusă sub 40% (HFrEF);
- IC cu fracție de ejecție păstrată, mai mare de 50% (HFpEF), și un nivel crescut al peptidelor natriuretice (BNP>35 pg/ml și/sau NT-proBNP>125 pg/mL) și prezența fie a unei boli cardiace structurale (hipertrofie ventriculară stângă și/sau dilatație atrială stângă), fie a unei disfuncții diastolice.
Cele două au fost inițial considerate a fi entități opuse la două capete ale aceluiași spectru. Cu toate acestea, paradigma actuală consideră că dezvoltarea și progresia celor două forme de insuficiență cardiacă sunt distincte. Ghidul ESC din 2016 (3) a propus o a treia clasă, cu fracție de ejecție la nivel mediu (HFmrEF), pentru care FE este între 40-49% și însoțește aceleași două componente menționate mai sus ale HFpEF.
Chiar dacă știm că insuficiența cardiacă este mai complexă, continuăm să definim insuficiența cardiacă prin clasificări vechi de o sută de ani, cum ar fi sistemul de clasificare New York Heart Association (NYHA) sau ghidurile vechi bazate pe fracția de ejecție a ventriculului stâng. Niciunul dintre aceste elemente nu surprinde însă în mod adecvat riscul individual al pacientului sau diversitatea cauzelor bolii.
Tot mai multe dovezi au demonstrat capcanele acestei metode de clasificare și au sugerat că gestionarea insuficienței cardiace necesită o cunoaștere profundă a proceselor fiziopatologice și nu se poate baza doar pe evaluarea FEVS. Având în vedere limitarea acestui parametru și implicarea sistemică a insuficienței cardiace, clasificările insuficienței cardiace ar trebui înlocuite luând în considerare afectarea multiorganică. O stadializare integrată, optimă poate oferi o evaluare globală a caracteristicilor pacientului, permițând terapii țintite și un management personalizat al insuficienței cardiace.
Un exemplu este o analiză recentă, care a identificat trei variații ale entității clinice unice numită insuficiență cardiacă cu fracție de ejecție păstrată (4). Cele trei fenotipuri propuse, bazate pe markeri biochimici, indică diferite posibile strategii de management, dintre care una ar putea să nu implice neapărat medicamente. De altfel, identificarea fenotipurilor insuficienței cardiace, utile în practica medicală, a fost un obiectiv de cercetare de lungă durată tocmai pentru că fiecare fenotip ar putea răspunde mai bine la abordări distincte, proprii, de tratament.
Fiziopatologia complexă a bolii. Afectare multiorganică
Indiferent de cauză, starea fiziopatologică comună, care perpetuează progresia insuficienței cardiace, este extrem de complexă. Mecanismele compensatorii există la fiecare nivel de organizare, de la nivel subcelular până la interacțiunile dintre organe. Abia în momentul în care această rețea de modificări adaptative devine depășită, apare insuficiența cardiacă. Cele mai importante adaptări sunt următoarele:
- Mecanismul Frank-Starling – creșterea presarcinii ajută la susținerea performanței cardiace;
- Modificări regeneratorii ale miocitelor și moartea acestora;
- Hipertrofie miocardică cu/fără dilatarea cavității cardiace – creșterea masei țesutului contractil;
- Activarea sistemelor neuro-umorale, printre care SRAA (sistemul renină-angiotensină-aldosteron) și sistemele vasoactive, ce mențin tensiunea arterială și perfuzia țesuturilor.
Creșterea rezistenței vasculare periferice la pacienții cu insuficiență cardiacă cronică este legată de modificările controlului autonom, inclusiv tonusul simpatic crescut, activarea sistemului renină-angiotensină-aldosteron, concentrații crescute de endotelină și tulburarea eliberării de oxid nitric. Există dovezi care arată că funcția endotelială afectată în insuficiența cardiacă cronică poate fi îmbunătățită prin antrenamente fizice și tratament medicamentos, precum inhibitorii enzimei de conversie a angiotensinei.
Modificări periferice considerabile apar și la nivelul mușchilor scheletici ai acestor pacienți, inclusiv reducerea masei musculare și anomalii ale structurii, metabolismului și funcției musculare. Există, de asemenea, un flux sanguin redus către mușchii scheletici activi, care este legat de vasoconstricție și pierderea masei musculare. Toate aceste anomalii ale mușchilor scheletici, inclusiv asupra mușchilor respiratori, contribuie la simptomele de fatigabilitate, letargie și intoleranță la efort, care apar în insuficiența cardiacă cronică.
Inima și rinichii sunt strâns legate în sindromul clinic al insuficienței cardiace. Acum este clar că disfuncția renală apare frecvent în toate fenotipurile de IC și, atunci când este prezentă, se asociază cu mortalitate și morbiditate crescute (5). În timp ce fiziopatologia este multifactorială, cei mai importanți factori sunt perfuzia renală redusă și congestia venoasă. Interesul recent s-a concentrat asupra degradării funcției renale, puternic legată de mortalitate, dar care, aparent, apare doar atunci când se deteriorează statusul IC. Din păcate, până în prezent clinicienii nu sunt în măsură să identifice în mod specific acei pacienți cu prognostic sumbru după degradarea funcției renale. Deși s-au învățat multe despre interacțiunea cardiorenală în insuficiența cardiacă, încă au rămas fără răspuns mai multe întrebări.
Anomaliile funcției pulmonare atât în repaus, cât și în timpul exercițiilor fizice, sunt frecvent observate la pacienții cu insuficiență cardiacă cronică, de asemenea, în absența bolilor respiratorii de fond. Modificările mecanicii respiratorii și ale capacității de schimb gazos sunt strict legate de insuficiența cardiacă. Pacienții cu IC severă prezintă adesea un model respirator restrictiv, secundar dilatației inimii și a fluidelor pulmonare crescute, și afectarea difuziei gazelor, în principal datorită unei rezistențe crescute la difuzia moleculară prin membrana alveolo-capilară(6). Difuzia redusă a gazelor contribuie la intoleranța la efort și la un prognostic mai prost.
Conceptul inimii ca organ ce se poate auto-reînnoi este unul relativ recent (7). Această paradigmă privind biologia miocitelor a creat un întreg domeniu de cercetare care vizează în mod direct creșterea regenerării miocardice. S-a demonstrat că rata de turnover a miocitelor crește în perioadele de stres (8). În insuficiența cardiacă, acest mecanism de înlocuire devine copleșit de creșterea și mai rapidă a ratei de pierdere a miocitelor. La nivel celular, acest dezechilibru între hipertrofie și moarte celulară față de regenerare este calea comună finală pentru progresia remodelării și a insuficienței cardiace.
Perspective pentru reducerea poverii IC
Epidemia de insuficiență cardiacă se schimbă. Deși incidența ajustată în funcție de vârstă s-a stabilizat și pare să scadă, insuficiența cardiacă rămâne o problemă clinică și de sănătate publică serioasă, deoarece numărul total de pacienți care suferă de insuficiență cardiacă este în creștere, reflectând evoluția cronică a bolii, precum și creșterea populației și îmbătrânirea.
Sarcina factorilor de risc și a comorbidităților este mare și în creștere, în special la vârstnici. IM joacă un rol mai puțin important în etiologia insuficienței cardiace, în timp ce obezitatea este în creștere și se preconizează că va juca un rol din ce în ce mai important. Câștigurile potențiale ale reducerii factorilor de risc și îmbunătățirii prevenirii primare și a respectării tratamentului vor umbri probabil efectul oricărei noi strategii terapeutice. Programele de îngrijire ar trebui să se concentreze pe gestionarea multi-morbidității și cronicității, deoarece indivizii vor trăi cu insuficiență cardiacă mai mult decât oricând.
În era genomicii în care ne aflăm, noile tehnologii și informațiile pe care le generează au o gamă largă de aplicații potențiale pentru insuficiența cardiacă. Deși nu a existat o utilizare practică pe scară largă a informațiilor genomice în practica de zi cu zi, există multe exemple despre modul în care aceste informații încep să transforme modul în care privim bolile în termeni de diagnostic, prognostic și tratament. Experiența oncologiei și a altor domenii ajută la informarea despre utilizarea acestor informații în investigarea diagnosticului de insuficiență cardiacă, a prognosticului și a răspunsului la tratament, cât și a naturii reciproce a informațiilor. Datele pot fi utile din punct de vedere clinic (de exemplu, predicția bolii), precum și în cercetarea ulterioară de laborator (depistarea căilor biologice la pacienții care nu răspund la tratament poate constitui un punct central al descoperirii de noi medicamente) – aceasta este esența medicinei translaționale.
[1] Savarese, G., and Lund, L. H. (2017). Global public health burden of heart failure. Card Fail. Rev. 3, 7–11
[2] Insuficiența cardiacă în România, în fiecare oră: 12 internări, 5 cazuri noi, un deces
[3] Ponikowski, P., Voors, A. A., Anker, S. D., Bueno, H., Cleland, J. G., Coats, A. J., et al. (2016). 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: the task force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC). Developed with the special contribution of the Heart Failure Association (HFA) of the ESC. Eur. J. Heart Fail. 18, 891–975.
[4] STUDIU. Insuficiența cardiacă cu fracție de ejecție păstrată, clasificată în 3 fenotipuri care pot beneficia de abordări terapeutice distincte
[5] Damman K, Testani JM. The kidney in heart failure: an update. Eur Heart J. 2015;36(23):1437-1444. doi:10.1093/eurheartj/ehv010
[6] Anna Apostolo, Giuliano Giusti, Paola Gargiulo, Maurizio Bussotti, Piergiuseppe Agostoni, “Lungs in Heart Failure”, Pulmonary Medicine, vol. 2012, Article ID 952741,9 pages, 2012.
[7] Anversa P, Nadal-Ginard B. Myocyte renewal and ventricular remodelling. Nature. 2002 Jan 10. 415 (6868):240-3.
[8] Anversa P, Nadal-Ginard B. Myocyte renewal and ventricular remodelling. Nature. 2002 Jan 10. 415 (6868):240-3.

