Premiul Nobel pentru Medicină sau Fiziologie 2023: Katalin Karikó și Drew Weissman – vaccinurile ARNm împotriva COVID-19
Karolinska Institutet, 12:45. Premiul Nobel pentru Medicină și Fiziologie 2023 a fost acordat cercetătorilor Katalin Karikó și Drew Weissman pentru contribuțiile la dezvoltarea vaccinurilor ARNm împotriva COVID-19. Mai exact, „pentru descoperirile legate de modificările bazelor nucleozidice care au permis dezvoltarea de vaccinuri ARNm eficiente împotriva COVID-19”.
Prin descoperirile lor revoluționare, care au schimbat fundamental înțelegerea noastră despre modul în care ARNm interacționează cu sistemul imun, laureații au contribuit la ritmul fără precedent al dezvoltării vaccinurilor într-una dintre cele mai mari amenințări la adresa sănătății umane din vremurile moderne – pandemia COVID-19.
Karikó și Weissman au publicat rezultatele lor într-un articol din 2005 care a primit puțină atenție la acea vreme, dar care a schimbat cursul pandemiei COVID-19, conducând la obținerea a două vaccinuri cu o eficacitate fără precedent, într-un timp record. Versatilitatea tehnologiei ARNm și viteza cu care pot fi dezvoltate vaccinurile au facilitat extinderea aplicațiilor și pentru alte boli infecțioase. Tehnologia este explorată și pentru tratamentul unor tipuri de cancere.
Urmăriți LIVE acordarea premiului.
Câteva articole cheie legate de subiect:
- Cum funcționează tehnologia ARN mesager folosită în vaccinurile COVID-19?
- Cum a fost posibilă dezvoltarea atât de rapidă a vaccinurilor contra COVID-19?

O nouă generație de vaccinuri
Vaccinarea stimulează formarea unui răspuns imun împotriva unui agent patogen, oferind organismului „instrumentele” să lupte împotriva bolii în cazul unei expuneri ulterioare. Vaccinurile tradiționale folosesc virusuri inactivate sau atenuate, cum ar fi cele pentru poliomielită, rujeolă și febra galbenă. Max Theiler a primit Premiul Nobel pentru Fiziologie sau Medicină în 1951 pentru descoperiri care au contribuit la dezvoltarea vaccinului împotriva febrei galbene.
Progresele în biologia moleculară au condus la dezvoltarea vaccinurilor bazate pe componente specifice ale virusului, în locul întregului virus. Aceste componente codifică de obicei proteine găsite la suprafața virusului, stimulând producerea de anticorpi care pot neutraliza virusul. Exemple de astfel de vaccinuri sunt cele pentru virusul hepatitei B și HPV. De asemenea, secvențele codului genetic viral pot fi transferate către un virus purtător inofensiv, denumit “vector”. Această tehnică este utilizată în vaccinurile împotriva virusului Ebola. La injectare, vaccinurile bazate pe vectori virali determină celulele noastre să producă proteina virală aleasă, stimulând un răspuns imun îndreptat împotriva virusului.
Producerea vaccinurilor bazate pe virusuri întregi, proteine sau vectori necesită culturi celulare la scară largă. Acest proces limitează posibilitatea producerii rapide a vaccinurilor în caz de epidemii și pandemii. De aceea, comunitatea științifică a încercat de mult să dezvolte tehnologii de vaccinare independente de culturile celulare, ceea ce s-a dovedit dificil.
În celulele umane, informația genetică codificată în ADN este transferată în ARN mesager (ARNm), care este folosit ca matrice pentru producerea de proteine. În anii `80, au fost introduse metode eficiente pentru producerea ARNm fără culturi celulare, mecanism numit transcripție in vitro. Acest pas a accelerat dezvoltarea aplicațiilor biologiei moleculare în mai multe domenii.
Ideile privind utilizarea tehnologiilor ARNm în scopuri vaccinale și terapeutice au început să prindă contur, dar s-au ivit obstacole în cale. ARNm transcris in vitro era considerat instabil și dificil de livrat, fiind necesară dezvoltarea de sisteme sofisticate de lipide purtătoare pentru încapsularea ARNm. Mai mult, ARNm produs in vitro provoca reacții inflamatorii.
Cu toate acestea, biochimista maghiară Katalin Karikó și-a dedicat cariera dezvoltării metodelor de utilizare a ARNm în scop terapeutic. În timpul anilor ’90, când era profesor asistent la Universitatea din Pennsylvania, ea a lucrat intens la ideea de a dezvolta terapii pe bază de ARNm, în ciuda dificultăților întâmpinate în convingerea finanțatorilor de cercetare cu privire la importanța proiectului său.

Drew Weissman, imunolog, colegul lui Kariko era interesat de celulele dendritice, care au funcții importante în activarea răspunsurilor imune induse de vaccin. Cei doi au început să lucreze împreună pentru a înțelege modul în care diferite tipuri de ARN interacționează cu sistemul imunitar.
Karikó și Weissman au observat că celulele dendritice recunosc ARNm transcris in vitro ca o substanță străină, ceea ce duce la activarea lor și eliberarea de molecule de semnalizare inflamatorii. S-au întrebat de ce ARNm transcris in vitro era recunoscut ca străin în timp ce ARNm provenit din celulele mamiferelor nu provoca aceeași reacție. Karikó și Weissman au realizat că trebuie să existe anumite caracteristici care să facă diferența între tipurile diferite de ARNm.
Tehnologia ARNm a salvat milioane de vieți în contextul pandemiei COVID-19
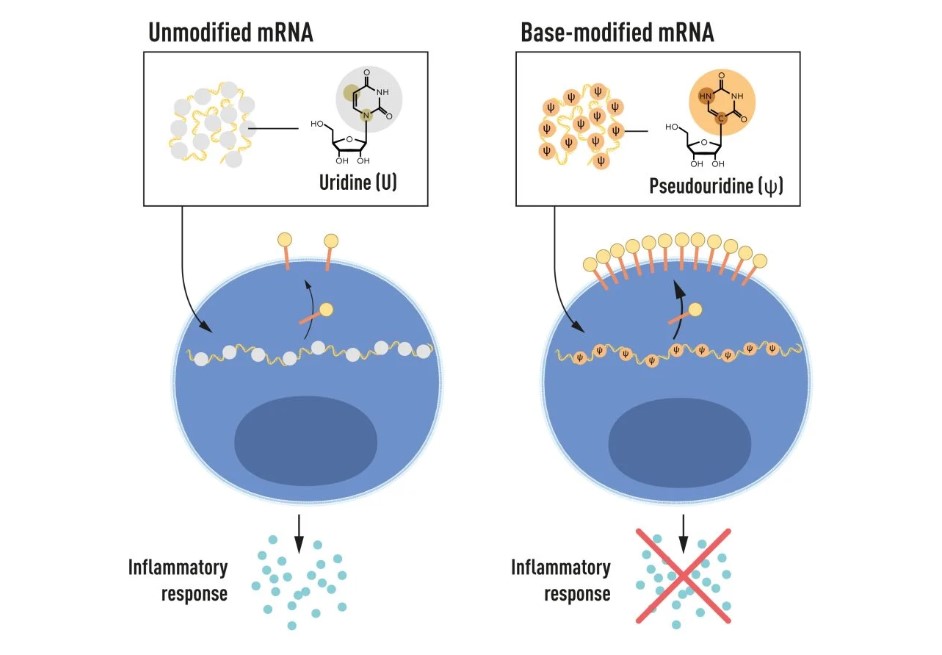
Unitatea de bază a ARN-ului conține baze azotate, care pot fi de 4 tipuri, abreviate A, U, G și C, corespondente cu A, T, G și C în ADN, literele codului genetic. Karikó și Weissman știau că bazele din ARN-ul provenit din celule sunt adesea modificate chimic, în timp ce ARNm transcris in vitro nu este. S-au întrebat dacă absența bazelor modificate în ARN-ul transcris in vitro ar putea explica reacția inflamatorie nedorită. Pentru a investiga acest lucru, au produs diferite variante de ARNm, fiecare cu modificări chimice specifice, pe care le-au livrat celulelor dendritice.
Rezultatele au fost remarcabile: Răspunsul inflamator a fost aproape abolit atunci când modificările bazelor au fost incluse în ARNm. Acest lucru a reprezentat o schimbare în înțelegerea modului în care celulele recunosc și răspund la diferite forme de ARN. Karikó și Weissman au înțeles imediat că descoperirea lor era relevantă pentru utilizarea ARN-ului mesager ca terapie. Aceste rezultate fundamentale au fost publicate în 2005, cu cincisprezece ani înainte de pandemia COVID-19.
Interesul pentru tehnologia ARNm a început să crească, iar în 2010, mai multe companii lucrau la dezvoltarea acestei metode și au fost obținute vaccinuri împotriva virusului Zika și a MERS-CoV. După izbucnirea pandemiei de COVID-19, au fost dezvoltate cu o viteză record două vaccinuri pe bază de ARNm modificate, codificând proteina de suprafață a SARS-CoV-2. Au fost raportate date de eficacitate de aproximativ 95%, iar ambele vaccinuri au fost aprobate încă din decembrie 2020.
Flexibilitatea impresionantă și viteza cu care pot fi dezvoltate vaccinurile ARNm deschid calea pentru utilizarea acestei noi platforme și pentru vaccinurile împotriva altor boli infecțioase. În viitor, tehnologia ar putea fi utilizată și pentru tratarea unor tipuri de cancer.
Mai multe alte vaccinuri împotriva SARS-CoV-2, bazate pe diferite metodologii, au fost, de asemenea, introduse rapid, iar în total, au fost administrate peste 13 miliarde de doze de vaccin împotriva COVID-19 la nivel global. Vaccinurile au salvat milioane de vieți și au prevenit boli severe în mult mai multe cazuri, permițând societăților să se redeschidă și să revină la condiții normale. Prin descoperirile lor fundamentale privind importanța modificărilor bazelor în ARNm, laureații Nobel de anul acesta au contribuit în mod critic la această dezvoltare transformatoare în timpul uneia dintre cele mai mari crize de sănătate ale timpurilor noastre.
Citește și:
- CE SPUN STUDIILE despre vaccinul Pfizer/BioNTech împotriva COVID-19. Momentele cheie care au condus la aprobarea condiționată din Uniunea Europeană
- #ReThinkHealth Podcast. Dan Staner, românul din spatele vaccinului Moderna. Ce produse pe baza tehnologiei ARNm se află în dezvoltare?

