CE SPUN STUDIILE despre vaccinul Pfizer/BioNTech împotriva COVID-19. Momentele cheie care au condus la aprobarea condiționată din Uniunea Europeană
Comirnaty, vaccinul produs de Pfizer și BioNTech este primul vaccin împotriva COVID-19 aprobat condiționat în Uniunea Europeană (la finalul lui decembrie 2020). De atunci, au mai fost aprobate încă 3 vaccinuri, iar România a atins pe 29 martie 2021 pragul de 1 milion de persoane vaccinate cu ambele doze (cifră valabilă pentru suma celor 3 vaccinuri distribuite pe teritoriul țării: Pfizer, Moderna și AstraZeneca). Însă ținta impusă de Comisia Europeană pentru primul trimestru al 2021 nu a fost atinsă de niciunul dintre statele UE.
Pe de altă parte, tabloul vaccinării a devenit și mai complex din cauza noilor variante virale circulante. Organismele internaționale recomandă supravegherea genomică și adaptarea vaccinurilor pentru a putea fi eficiente împotriva variantelor nou-apărute (diferite de tulpina inițială, detectată la finalul anului 2019). Citește și: PROPUNERE. Supravegherea prin secvențiere genomică a virusului SARS-CoV-2 în România: recomandările Centrului pentru Inovație în Medicină
În acest articol ne propunem o sumarizare a informațiilor științifice și a celor obținute în urma vaccinării cu vaccinul Comirnaty. Vaccinul dezvoltat de Pfizer și BioNTech este realizat prin tehnologia ARNm și conține informația genetică necesară pentru producția proteinei virale S (spike), care stimulează apariția unui răspuns imun protector contra COVID-19. La baza aprobării condiționate de punere pe piață a vaccinului s-a aflat un studiu clinic de fază 3, care a inclus aproape 44.000 de persoane. Mai multe detalii despre modul de funcționare a vaccinurilor de tip ARNm, în următorul articol: Cum funcționează tehnologia ARN mesager folosită în vaccinurile COVID-19?
Datele de eficacitate împotriva variantelor virale circulante
- Studiu din Israel (6 aprilie 2021): Protecția oferită de vaccinul Pfizer împotriva variantei B.1.351 (identificată prima dată în Africa de Sud) este mai scăzută
Un studiu recent care a evaluat vaccinul Pfizer provine din Israel și nu a fost încă supus expertizei specialiștilor – este disponibil în varianta preprint. Studiul a comparat aproape 400 de persoane care au primit un diagnostic de COVID-19 după minim 14 zile de la administrarea de una sau două doze de vaccin, față de același număr de persoane nevaccinate.
S-a constatat că B.1.351 reprezintă aproximativ 1% din cazurile de COVID-19 studiate. Dar printre pacienții care au primit două doze de vaccin, rata de prevalență a variantei a fost de opt ori mai mare decât la cei nevaccinați – 5,4% față de 0,7%. Acest lucru sugerează că vaccinul este mai puțin eficient împotriva variantei B.1.351, în comparație cu varianta originală și varianta B.1.1.7 (identificată pentru prima dată în Marea Britanie, care este majoritară în Israel). Limitarea studiului vine din numărul mic de persoane studiate, însă reprezintă un semnal de alarmă pentru studierea mai atentă a acestor cazuri. În plus, pare că momentan, prevalența acestei variante este scăzută.
Pe de altă parte, pe 1 aprilie, Pfizer anunța că în conformitate cu rezultatele studiului de fază III pe populația adultă, vaccinul BNT162b2 a demonstrat o eficacitate de 100% și în prevenirea bolii Covid19 cauzată de varianta B.1.351 a SARS-CoV-2 (au fost înregistrate 9 cazuri de Covid19, toate în grupul placebo, iar în urma secvențierii s-a constatat că 6 fuseseră determinate de B.1.351).
- Comunicat Pfizer (8 ianuarie 2021): Impactul variantei B.1.1.7. a SARS-CoV-2 asupra eficacității vaccinului Pfizer
La acea dată, varianta B.1.1.7. a SARS-CoV-2 era în vârful ascensiunii în întreaga lume, inclusiv în România. Dovezile indicau faptul că numeroasele mutații ale B.1.1.7, inclusiv opt la nivelul proteinei spike, sporesc transmisibilitatea – datele au fost confirmate la momentul redactării actualului articol, varianta fiind în mod curent majoritară în UE. În luna ianuarie 2021, informațiile disponibile indicau și o mortalitate mai mare cauzată de infecția cu B.1.1.7, însă un studiu publicat recent în The Lancet infirmă ipoteza conform căreia varianta B.1.1.7 se asociază cu o severitate și mortalitate mai ridicată a bolii COVID-19, în comparație cu celelalte variante virale.
Într-o declarație de la sfârșitul lunii decembrie, ECDC a avertizat că datele obținute prin secvențierea genomică a SARS-CoV-2 devin tot mai importante pe măsură ce vaccinurile și terapiile antivirale devin disponibile, pentru a monitoriza modul în care noile variante influențează eficacitatea vaccinului, precum și posibila apariție a rezistenței antivirale. ECDC avertizează că atunci când sunt raportate variante virale în zone geografice specifice, autoritățile ar trebui să se concentreze mai mult pe secvențierea cazurilor cu suspiciune de expunere la o astfel de variantă a SARS-CoV-2. Dacă sunt disponibile alte metode de identificare a acestor variante, acestea ar trebui considerate ca o completare a secvențierii.
FDA a alertat profesioniștii din domeniul sănătății că mutațiile SARS-CoV-2 pot declanșa rezultate fals negative la testele standard pentru COVID-19. Acuratețea poate avea de suferit dacă modificările apar în regiunea specifică a ARN-ului viral utilizată de testul diagnostic molecular pentru a determina un rezultat pozitiv, care poate varia de la un produs la altul. Testele care utilizează mai multe zone ale genomului viral pentru a stabili potrivirea, oferă mai multe șanse de a obține un rezultat precis.
Cercetătorii de la Universitatea din Texas și Pfizer au declarat că vaccinul a reușit să neutralizeze în laborator o versiune a coronavirusului cu mutații ale proteinei spike (mutația N501Y). Datele de atunci s-au dovedit a fi corecte, vaccinul oferind protecție și împotriva B.1.1.7.
Eficacitatea administrării unei singure doze de vaccin la persoanele care au trecut anterior prin infecție
- Studiu Nature (1 aprilie 2021): O singură doză din vaccinul Pfizer determină un răspuns imun optim la persoanele care au trecut prin infecție
Administrarea unei singure doze din vaccinul Pfizer la persoanele cu istoric de infecție COVID-19 determină un răspuns imun similar cu cel obținut în urma administrării a două doze la persoanele care nu au trecut prin boală. Datele provin dintr-un studiu publicat recent în Nature, care a inclus peste 1.000 de participanți.
Nivelul de anticorpi a fost măsurat înainte de prima doză, în intervalul de 7-21 de zile de la prima doză și la 21 de zile de la a doua doză. Datele susțin rezultatele unor studii anterioare mai mici, care indicau valori mai mari ale anticorpilor anti proteină S la persoanele cu istoric de COVID-19. A doua doză de vaccin nu aduce beneficii mai mari în ceea ce privește capacitate de a dezvolta anticorpi neutralizanți la această categorie de persoane. Sunt necesare studii suplimentare care să evalueze răspunsul imun pe termen lung pentru validarea unei astfel de strategii de vaccinare.
- Studiu The Lancet (18 februarie 2021): Eficacitate de peste 85% după o singură doză din vaccinul Pfizer contra COVID-19
Studiul arată că o singură doză din vaccinul ARNm produs de Pfizer determină o eficacitate de 85% contra infecției cu SARS-CoV-2. Analiza a inclus 7.214 persoane care lucrează în domeniul sanitar, în cadrul Sheba Medical Center din Israel. Reducerea totală a cazurilor de infecție, inclusiv cazuri asimptomatice, a fost de 75%. Cu toate acestea, persoanele incluse în studiu sunt majoritar tinere, cu vârste de sub 65 de ani.
Un alt studiu, publicat în New England Journal of Medicine, a analizat datele pe care Pfizer le-a furnizat către FDA și rezultatele arată o eficacitate de 92,6% după prima doză de vaccin. În studiile clinice care au condus la autorizarea vaccinului în UE este raportată o eficacitate de 52,4% după prima doză și de 95% după rapel.
Datele susțin fezabilitatea unei strategii prin care să se amâne a doua doză de vaccin, însă studiile nu au determinat cât timp durează protecția oferită de o singură doză și sunt așteptate date de follow-up.

Eficacitatea vaccinului la persoanele cu vârsta sub 16 ani
- Comunicat Pfizer (31 martie 2021): eficacitate 100% în prevenirea Covid-19 în grupa de vârstă 12-15 ani, cu sau fără infecție anterioară
Conform rezultatelor unui studiu de fază III efectuat în populația pediatrică, vaccinul împotriva Covid-19 produs de Pfizer și BioNTech (Comirnaty) este 100% eficace în prevenirea bolii la copiii cu vârste cuprinse între 12 și 15 ani. Studiul a cuprins peste 2.000 de adolescenți. De asemenea, evaluarea eficacității la copii cu vârste cuprinse între 6 luni și 11 ani a început săptămâna trecută și continuă.
Eficacitatea vaccinului la persoanele cu obezitate
Conform unui studiu recent (26 februarie 2021), eficacitatea Comirnaty ar putea fi scăzută la persoanele diagnosticate cu obezitate. Datele din studiu indică o corelație puternică între indicele de masă corporală (IMC, parametru utilizat în diagnosticarea obezității) și titrul de anticorpi post-vaccinare. Eficacitatea răspunsului umoral a fost semnificativ mai mare în rândul participanților cu greutate normală sau subponderali. Este prea devreme pentru a înțelege exact ce înseamnă acest lucru pentru eficacitatea vaccinului, dar rezultatele raportate ar putea implica faptul că o doză de rapel suplimentară ar putea fi necesară pentru imunizarea corespunzătoare a persoanelor cu obezitate.
Studiul a evaluat răspunsul imun (prin determinarea nivelului de anticorpi împotriva proteinei spike a SARS-CoV-2) în rândul a 248 de profesioniști din sănătate care au fost vaccinați cu două doze de vaccin Pfizer/BioNTech. La șapte zile de la administrarea rapelului, 99,5% dintre participanți au dezvoltat anticorpi, iar acest răspuns a fost mai mare decât cel înregistrat la persoanele care au trecut prin boală și s-au recuperat. Răspunsul imun a fost scăzut la persoanele care erau supraponderale și obeze. Studiul se află actual în revizuire de către specialiști.
Date EMA din viața reală: Profilul de siguranță al vaccinurilor de tip ARNm autorizate în UE, confirmat
Agenția Europeană a Medicamentului a emis pe 28 ianuarie un document care oferea noi date despre siguranța vaccinului Comirnaty. EMA publică în fiecare lună informări cu privire la siguranța tuturor vaccinurilor COVID-19 autorizate. De la obținerea autorizației condiționate de punere pe piață în UE, profilul de siguranță al vaccinului de tip ARNm a fost analizat constant. Rezultatele din cele mai recente analize provin din baza de date UE privind efectele secundare suspecte (EudraVigilance) și din rapoartele lunare ale companiei producătoare. Această evaluare a fost realizată de un comitet special din cadrul EMA (PRAC – Pharmacovigilance Risk Assessment Committee).
O analiză din SUA sugerează faptul că frecvența cazurilor de șoc anafilactic este de 11 cazuri la 1 milion de doze de Comirnaty administrate. De asemenea, au fost analizate cazurile de deces asociate vaccinării în rândul unei categorii vulnerabile de pacienți vârstnici, cazuri raportate de autoritățile din Norvegia. PRAC a ajuns la concluzia că acestea nu sunt cauzate de administrarea vaccinului Comirnaty, iar cazurile nu influențează profilul de siguranță al vaccinului.
Autorizarea și începerea vaccinării în România
- 27 decembrie 2020: începe vaccinarea împotriva COVID-19 în statele membre UE, inclusiv în România
În urma acordării autorizației condiționate de punere pe piață în UE pentru vaccinul contra COVID-19 produs de Pfizer/BioNTech (din data de 21 decembrie), vaccinarea a început pe 27 decembrie în majoritatea statelor din UE. Strategia de vaccinare împotriva COVID-19 în România a fost publicată încă de la începutul lunii decembrie și are scopul de a asigura accesul sigur, eficient și echitabil la vaccin.
Prima tranșă de 10.000 de doze de vaccinuri a sosit la Institutul Național de Cercetare-Dezvoltare Medico-Militar „Cantacuzino”. Campania de vaccinare contra COVID-19 din România a început pe 27 decembrie cu toate cele 10 spitale de boli infecțioase aflate în prima linie de luptă cu noul coronavirus.
- 21 decembrie 2020: Vaccinul Pfizer/BioNTech împotriva COVID-19 a primit autorizație condiționată de punere pe piață în UE
Comisia Europeană a acordat autorizația condiționată de punere pe piață pentru vaccinul BNT162b2 produs de Pfizer/BioNTech. Decizia a venit în urma recomandării Comitetului pentru Produse Medicale de Uz Uman (CHMP) din cadrul Agenției Europene a Medicamentului (EMA), care a ajuns la concluzia că beneficiile vaccinului depășesc riscurile.
În noiembrie 2020, cele două companii producătoare au ajuns la un acord cu Comisia Europeană pentru a distribui 200 milioane de doze de vaccin în 2020 și 2021 cu opțiunea de a produce încă 100 de milioane de doze adiționale – opțiune care s-a concretizat în aprilie 2021.
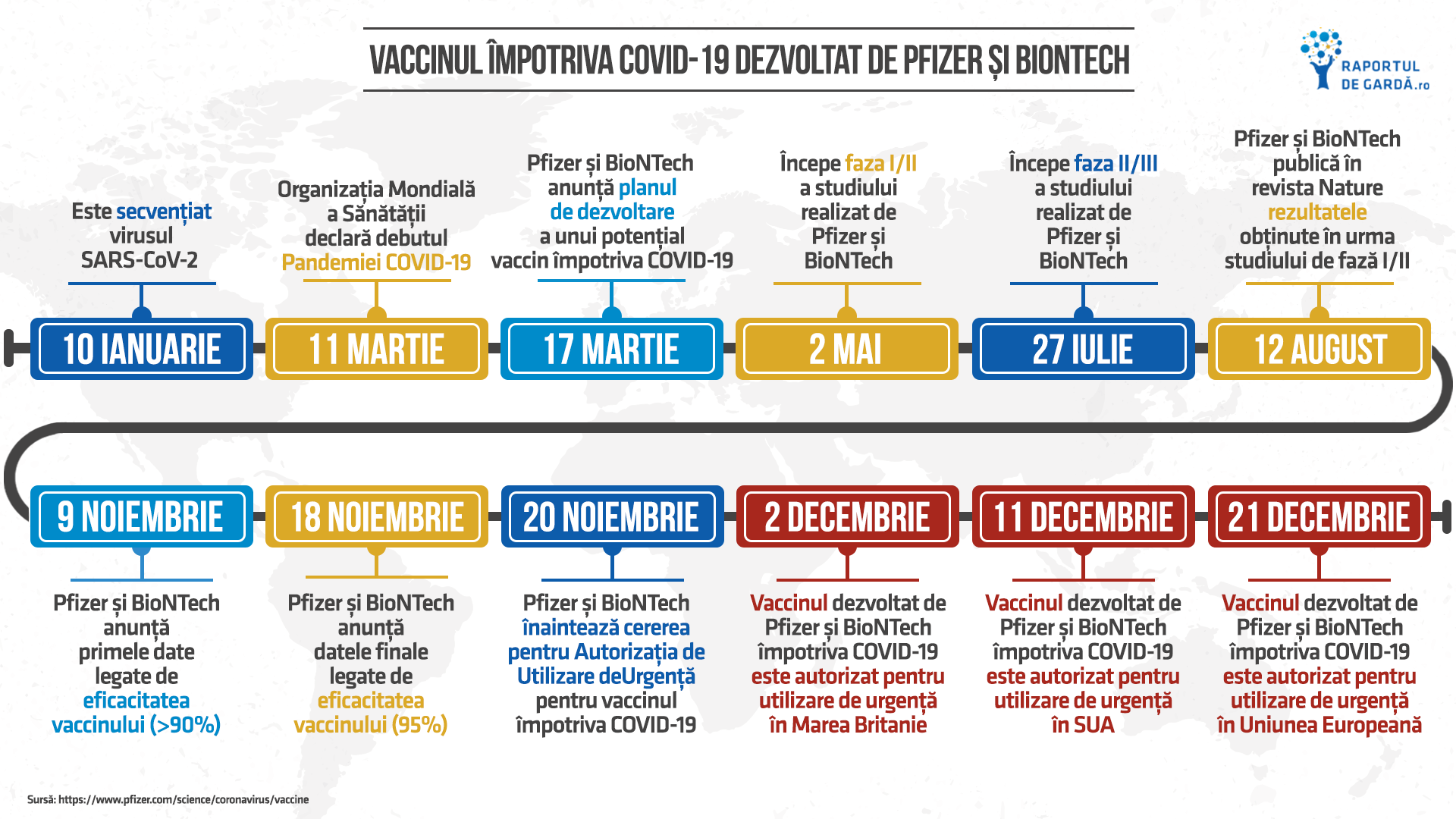
Alte momente importante care au condus la aprobarea condiționată a vaccinului:
- 11 decembrie 2020: FDA a autorizat vaccinul Pfizer/BioNTech pentru utilizare de urgență în SUA
- 2 decembrie 2020: Marea Britanie aprobă de urgență vaccinul Pfizer/BioNTech
- Săptămâna 16-22 noiembrie 2020: Pfizer a înaintat cererea pentru Autorizația de Utilizare de Urgență pentru vaccinul împotriva COVID-19 către FDA
- Săptămâna 9-15 noiembrie 2020: Vaccinul contra COVID-19: peste 90% eficiență, conform unei analize preliminare. Ce nu se știe încă?
- Iulie 2020: Pfizer și BioNTech au primit aprobarea FDA pentru accelerarea dezvoltării a două vaccinuri împotriva SARS-CoV-2
- Aprilie 2020: Pfizer și BioNTech primesc aprobarea autorității de reglementare germană, Paul-Ehrlich-Institut, pentru începerea studiului clinic de faza 1/2 pentru vaccinul BNT162
Citește și:
- Vaccinul Pfizer/BioNTech contra COVID-19 a primit autorizație condiționată de punere pe piață în UE
- Cum se acordă autorizarea condiționată de punere pe piață în Uniunea Europeană pentru vaccinurile împotriva COVID-19?
- Cum a fost posibilă dezvoltarea atât de rapidă a vaccinurilor contra COVID-19?

