STUDIU. Câte mutații genetice sunt necesare pentru apariția cancerului?
În anul 1859, era publicată teoria evoluționistă a lui Charles Darwin. 150 de ani mai târziu oamenii de știință de la Wellcome Trust Sanger Institute au pornit de la principiile selecției naturale pentru a elabora o metodă de cuantificare a anomaliilor genetice care determină dezvoltarea cancerului. Studiul realizat de aceștia a evaluat peste 7.500 de tumori, reprezentând 29 de tipuri de cancer, iar rezultatele au fost publicate luna aceasta în jurnalul medical Cell.
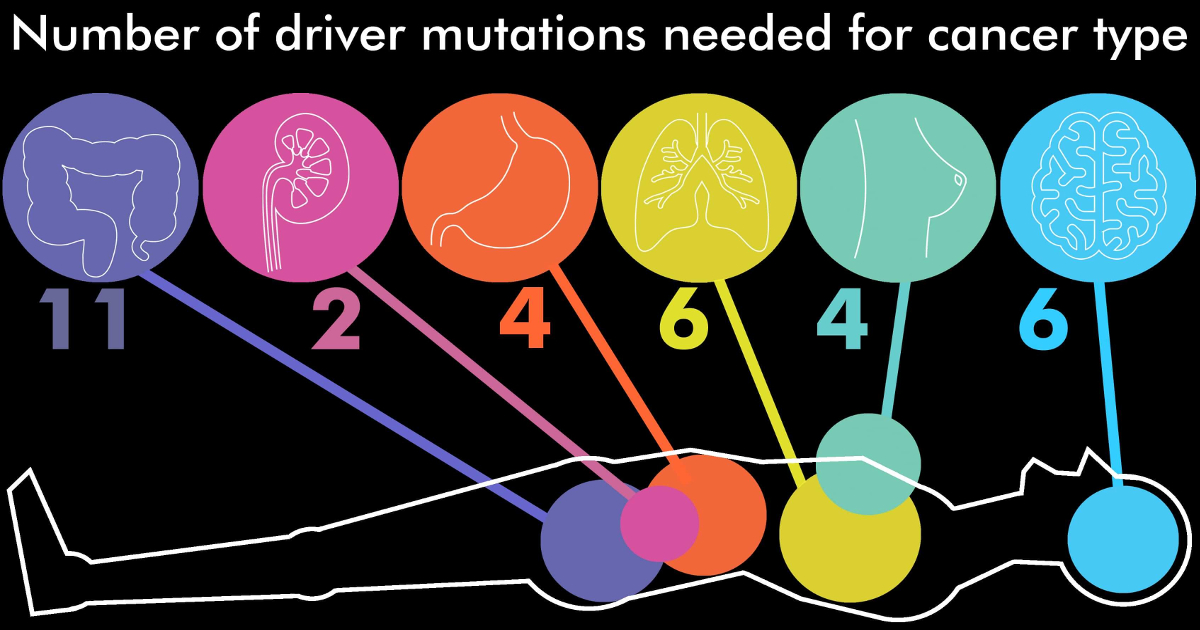
„Ne-am pus o întrebare pentru care se caută un răspuns încă din 1950. Câte mutații sunt necesare pentru ca o celulă normală să se transforme într-o celulă canceroasă? Răspunsul este – PUȚINE. De exemplu, în jur de 4 mutații per pacient sunt necesare în medie pentru declanșarea cancerului hepatic, pe când pentru cancerul colorectal aproximativ 10 mutații” – Dr. Peter Campbell, unul dintre autorii studiului
Studiul a arătat variabilitatea mutațiilor în cazul diferitelor tipuri de cancer. Observații esențiale din studiu:
- 99% dintre mutațiile codante identificate în cancer sunt inofensive și sunt tolerate de celule fără să le afecteze supraviețuirea. Doar câteva mutații specifice ar fi responsabile de apariția cancerului
- se înregistrează mai puțin de o mutație/tumoră în cazul cancerului testicular și tiroidian și mai mult de 10 mutații/tumoră în cazul cancerului endometrial și al celui colorectal
- aproximativ jumătate dintre mutațiile driver au fost identificate la nivelul unor gene care anterior nu erau asociate cancerului;
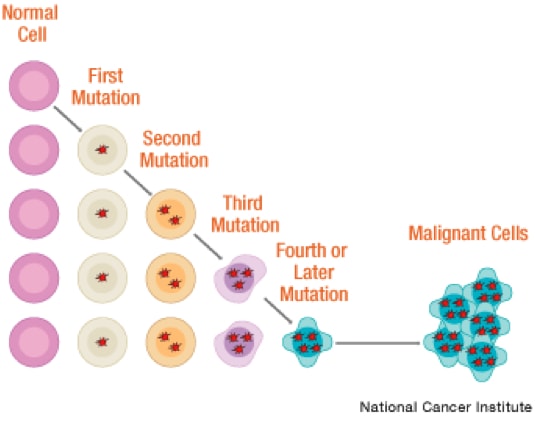
Mutațiile genetice – de la adaptare la boală
Toate procesele de evoluție la nivelul unui organism depind de variabilitatea genetică, un fenomen care explică modul în care organismele diferă unul de altul. Dacă ereditatea presupune transmiterea caractererelor între generații, variabilitatea desemnează acele elemente care conferă individualitate. De-a lungul timpului, apar constant mutații în ADN, mutațiile fiind cele care susțin adaptarea și evoluția în cadrul speciei. Cu toate acestea, există și mutații care pot declanșa boala.
Și în cazul cancerului apare un fenomen de selecție naturală, care dictează modul în care se exprimă mutațiile ce se acumulează la nivelul celulelor organismului. Cancerul apare ca urmare a mutațiilor somatice (care influențează celulele ce alcătuiesc țesuturile). Totuși, nu toate mutațiile de la nivelul genomului sunt responsabile de carcinogeneză. Mutațiile aleatorii care se acumulează constant, fără a avea un impact negativ asupra supraviețuirii celulei sunt mutații passenger. Acestea nu determină expansiunea clonală a unei celule transformate malign, nu promovează creșterea tumorală. Mutațiile driver, în schimb, determină oncogeneza.
Se consideră că mutațiile driver sunt aceleași pentru fiecare tip de tumoră, în timp ce mutațiile passenger sunt diferite de la pacient la pacient. Mutațiile passenger sunt considerate a fi neutre, fără implicare în oncogeneză.
Mutațiile care determină cancerul se manifestă la nivelul a două tipuri de gene: proto-oncogene, care au potențialul de a se transforma în gene care determină o neoplazie (oncogene) și gene care împiedică transformarea malignă a celulelor ( gene supresoare tumorale).
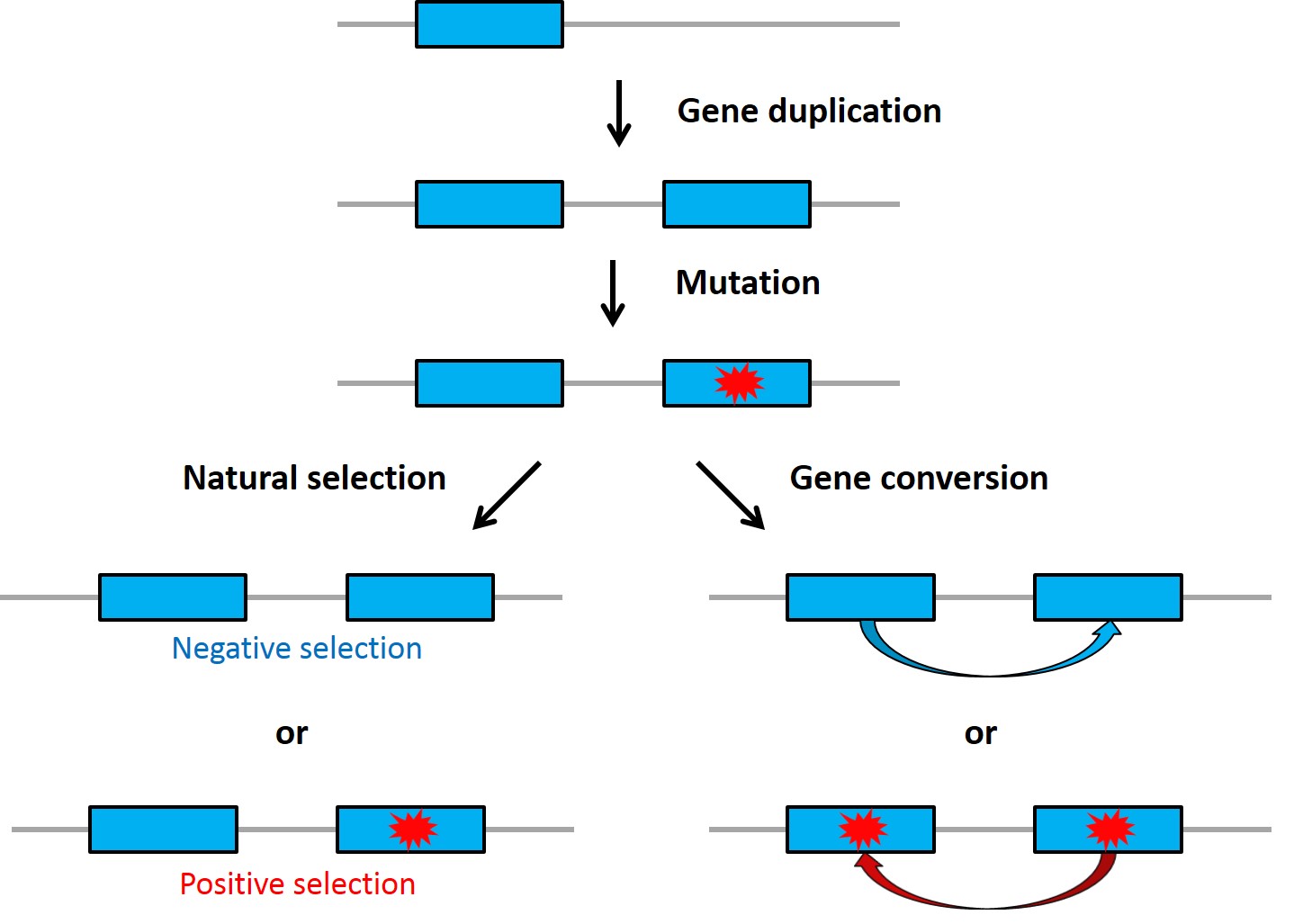
Selecția darwiniană și cancerul
Modificările „dăunătoare”, care reprezintă un dezavantaj pentru celulă sunt eliminate – selecție negativă (purifying selection), în timp ce mutațiile avantajoase care promovează supraviețuirea sau proliferarea celulei (mutații driver) persistă – selecție pozitivă (darwiniană). Selecția naturală care influențează mutațiile somatice se manifestă la nivel celular, spre deosebire de selecția care influențează linia germinală (afectând celulele sexuale), care manifestă la nivel de organism.
Cancerul este un proces al evoluției somatice în care se produce expansiunea clonală a unor celule ce prezintă mutații driver determinând proliferarea aberantă, invazivitatea la nivel tisular și diseminarea la alte organe. În cazul carcinogenezei este mai accentuată selecția pozitivă decât selecția negativă.
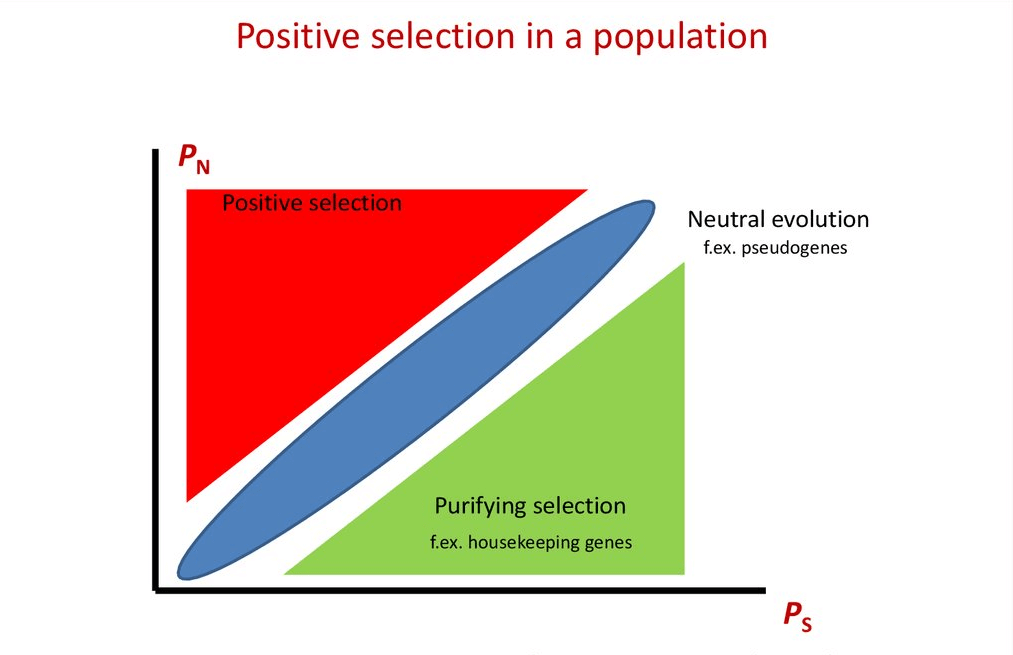
Subsetul de mutații care se menține, astfel încât să le putem identifica prin secvențiere genetică, se numesc substituții. Tipul de selecție se poate cuantifica prin examinarea tiparelor după care se realizează substituțiile. Una dintre metodele de cuantificare
folosite în studiu a fost dN/dS, care exprimă raportul dintre rata substituțiilor non-sinonime (mutațiile genetice care modifică aminoacizii rezultați) și rata substituțiilor sinonime (mutații care nu schimbă secvența de aminoacizi codificată).
Numărul de mutații driver necesare să genereze o tumoră reprezintă încă o provocare în oncologie. Secvențierea a mii de genomuri asociate cancerului nu a adus un răspuns acestei întrebări pentru că este greu de identificat care dintre mutațiile non-sinonime din genele canceroase sunt într-adevăr mutatii driver și pentru că există încă multe mutații driver nedescoperite. Luand în considerare impactul slab al selecției negative în carcinogeneză, se poate utiliza dN/dS pentru a se estima un numar mediu de mutații driver /tumoră.
Valorile estimate ale dN/dS pentru 369 de gene au variat semnificativ în funcție de tipul de cancer. De exemplu:
- 75% dintre mutatiile non-sinonime pentru gliom de grad mic sunt mutații driver
- în cazul melanomului, doar 25% dintre mutațiile non-sinonime sunt mutații driver
- pentru cancerul de cap si gât, valoarea este de doar 5%.
S-a putut observa că pentru sarcoame, cancer tiroidian, testicular sau mezoteliom există mai puțin de 1 mutație driver/pacient, în timp ce pentru cancerul de vezica urinară, cancerul endometrial și colorectal acestea ajung la 3-4 mutații/pacient.
Numarul mediu de substituții per tumoră care reprezintă mutații driver este mic, în medie de 4/tumoră, cu variații între 1 și 10, în funcție de tipul de neoplasm. Pentru o evaluare mai precisă, s-au estimat valorile dupa stadializarea tumorală. Nu s-a înregistrat o diferență între stadiul I și IV, în ceea ce privește numărul aproximativ de mutații driver.
O observație importantă ce a rezultat din studiu este că majoritatea mutațiilor asociate cancerului sunt bine tolerate de celulele organismului și scapă de sub selecția negativă. Aceasta este o descoperire surprinzătoare deoarece mutațiile care se transmit de la părinți sunt de obicei slab tolerate și se pierd de-a lungul timpului. În ceea ce privește cancerul, majoritatea mutațiilor rezistă fără a influența supraviețuirea celulei. Studiul a arătat că:
- 97-98% sunt gene neutre
- între 1-3,9% gene selectate pozitiv
- între 0,02 și 0,5% selectate negativ
Descifrarea mecanismelor selecției negative – calea spre identificarea noilor ținte pentru tratamentul cancerului?
O limitare în înțelegerea modului de evoluție a cancerului a fost reprezentată de imposibilitatea evaluării impactului selecției negative asupra modificării genomului asociat neoplaziilor. Detectarea mutațiilor supuse selecției negative este esențială deoarece poate facilita identificarea genelor cu rol cheie în proliferarea tumorală și a mecanismelor care determină întârzierea răspunsului la noii agenți terapeutici din oncologie.
Genele care ajung sub selecție negativă corespund proteinelor implicate în apariția adenocarcinoamelor – proteine din familia EGFR sau FGFR sau molecule de reparare a ADN-ului asociate melanomului, de exemplu. Evaluarea modului în care funcționează selecția negativă în apariția tumorilor ar putea avea un rol important în determinarea de noi ținte terapeutice.
Clonele celulare care poartă mutații aflate sub selecție negativă vor îmbătrâni sau vor muri. Acestui tip de de selecție îi corespunde un raport dN/dS mai mic de 1. Selecția negativă nu a fost încă bine studiată în ceea ce privește genomul cancerului, în mare parte din cauza faptului că din punct de vedere statistic, este dificil să se identifice un număr atât de mic de mutații fără a avea baze de date suficient de mari. Mai multe tipuri de analize genetice au fost realizate în acest studiu, iar concluzia a fost că impactul selecței negative este mult mai slab decât s-a crezut. Un rol important îl joaca și sistemul imun, care intervine spre eliminarea clonelor care poarta neo-antigene
Ce trebuie să mai descoperim despre genomul cancerului?
Se observă un interes crescut asupra studierii neoantigenelor create prin mutații somatice care modifică răspunsul imun față de cancer. Deși se cunosc multe gene care determină cancerul, încă nu este ușor de identificat exact mutațiile driver din genele respective sau câte alte mutații în alte gene ar putea fi implicate.
Pe măsură ce secvențierea genetică va intra în practica clinică, deciziile terapeutice pentru fiecare pacient se vor baza pe identificarea corectă a mutațiilor specifice tipului său de cancer. Majoritatea studiilor asupra mutațiilor somatice în cancer s-au concentrat pe identificarea mutațiilor de la nivelul genelor responsabile pentru apariția diferitelor tumori însă descoperirea genelor esențiale pentru creșterea tumorală, care nu au fost activate încă printr-o mutație, este încă o provocare.
„În acest studiu am demonstrat că aproximativ jumătate dintre mutațiile responsabile pentru apariția cancerului se exprimă la nivelul unor gene care nu au fost până acum asociate cu procesul de carcinogeneză. Există cercetări ample asupra celor mai importante gene implicate în apariția cancerului, dar există multe gene care nu au fost încă descoperite. Va fi nevoie să studiem mult mai multe tipuri de cancer prin secvențiere genetică pentru a identifica aceste gene” – Dr. Inigo Martincorena, autorul principal al studiului.
Cât de important este rolul factorilor genetici în apariția cancerului?
În deschiderea cărții „Gena Egoistă”, Richard Dawkins scrie că daca ființele superioare de pe alte planete ar vizita Pământul, pentru a ne verifica nivelul de civilizație prima întrebare ar fi: “Au ajuns să descopere evoluția?”.
„Astăzi înțelegem mai multe despre fotbal decât despre genetică și teoriile evoluției. Nimeni nu consideră că doar fundașii câștiga jocul la fotbal”- afirmă biologul Gregory Wray.
Genele joaca un rol important, într-adevar, în transformarea celulelor canceroase, dar trebuie privite în ansamblu. Ele fac parte dintr-un mecanism mult mai complicat care implică și stimuli externi, care țin de mediu, de stilul de viață, care influențează modul în care se exprimă materialul genetic. Un alt biolog care a studiat evoluționismul, Mary Jane West-Eberhard susține chiar că „genele nu conduc, ele urmează”.
Articole similare:
- #ESMO17: Secvențierea genomului poate ajuta la identificarea tratamentelor potrivite pentru unele cancere rare
- #ESMO17. Prima biopsie lichidă care poate selecta pacienții ce răspund cel mai bine la imunoterapie
- #ASCO2017: Testarea genomică de rutină este fezabilă, dar numai o parte a pacienților beneficiază de ea în mod curent

