FDA aprobă avelumab pentru tratamentul de întreținere în cancerul urotelial avansat
FDA (Food and Drug Administration) a aprobat avelumab (denumire comercială BAVENCIO) ca tratament de întreținere pentru cancerul urotelial avansat care nu a progresat în urma chimioterapiei cu un compus derivat de platină. Indicația de utilizare a inhibitorului de puncte de control, avelumab, a fost extinsă în urma rezultatelor studiului JAVELIN Bladder 100 , prezentate anul acesta în cadrul Întâlnirii Anuale a Societății de Oncologie Clinică din Statele Unite ASCO20.
Avelumab ca adjuvant în terapia de menținere în cancerul urotelial avansat, se administrează intravenos, într-o doză de 800 mg timp de 60 de minute, o dată la 2 săptămâni.
Cancerul de vezică avansat local sau cu metastaze la distanță implică administrarea de chimiotererapie din clasa derivaților de platină, precum cisplatinul. Pentru a reduce probabilitate de regresie a bolii, îngrijirea post-chimioterapie prin metode paleative este insuficientă. Continuarea tratamentului prin adăugarea unui agent biologic, precum avelumab, s-a dovedit a fi eficientă în prelungirea perioadei de supraviețuire la pacienții care nu prezintă un progres al procesului neoplazic post-chimioterapie.
Indicația terapiei cu avelumab a fost obținută în urma rezultatelor studiului clinic de fază III, multicentric, randomizat JAVELIN Bladder 100. Participanții incluși în studiu au fost diagnosticați cu cancer de vezică urinară avansat locat sau cu metastaze la distanță și au beneficiat în prealabil de chimioterapie. Criteriile de includere au fost următoarele:
- carcinom urotelial nerezecabil local sau cu metastaze la distanță;
- diagnosticul de carcinom urotelial în stadiul IV la inițierea primei cure de chimioterapie;
- între 4 și 6 cicluri de chimioterapie cu gemcitabină + cisplatin și/sau gemcitabină + carboplatin, administrate în prealabil.
Rezultatele studiului au dovedit eficiența tratamentului cu avelumab:
- perioada de supraviețuire a fost cu 7,1 luni, în medie, mai mare la lotul de pacienți care a primit avelumab și asistență medicală optimă, comparativ cu grupul de pacienți care au beneficiat doar de asistența medicală optimă;
- grupul de participanți care a primit avelumab și îngrijire medicală optimă a înregistrat o perioadă medie de supraviețuire fără progresia bolii de 21,4 luni, vs grupul de control, unde media a fost de 14,3 luni;
- la pacienții cu tumori care exprimă markerul PD-L1 (programmed death-ligand 1) administrarea de avelumab combinată cu îngrijirea medicală crește rata de supraviețuire.

Autorul studiului, Dr. Thomas Powels, profesor de oncologie genito-urinară și directorul Barts Cancer Centre din Londra, a explicat anul acesta în cadrul conferințelor online ASCO20, de ce aceste rezultate pot pune bazele unei schimbări majore în practica medicală:
“Perioada de menținere după chimioterapie este un prilej atractiv pentru inițierea tratamentului cu un inhibitor de puncte de control. De obicei, post-chimioterapie procesul neoplazic este sub control, însă, în cazul carcinomului urotelial, riscul de recidivă este foarte mare. Continuarea terapiei cu avelumab crește semnificativ rata de supraviețuire la acești pacienți. Noi credem că rezultatele studiului nostru vor influența major protocolul terapeutic pentru cancerul de vezică urinară.”
În ceea ce privește reacțiile adverse, mai mult de 20% dintre participanți au acuzat fatigabilitate, dureri musculoscheletale și infecții ale tractului urinar. Un singur deces s-a întregistrat, principala cauza fiind sepsisul. Aproape 28% dintre pacienți au prezentat reacții adverse severe.
Despre studiile JAVELIN și avelumab
Avelumab este un tratament inovator, dezvoltat de Merck în colaborare cu Pfizer, care ajută sistemul imun să lupte împotriva cancerului. Mecanismul său de acțiune presupune inhibarea PD-L1. PD-L1 este o proteină de pe suprafața celulelor tumorale și peritumorale, care interacționează cu proteina PD1 de pe suprafața celulelor imune și le inhibă, astfel, atacul împotriva tumorii.
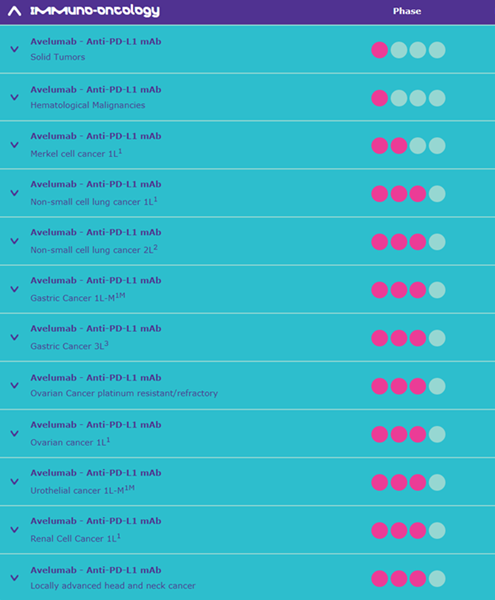
Primul studiu clinic care a implicat avelumab a demonstrat eficiența sa în tratamentul carcinomului cu celule Merkel, ceea ce a dus la aprobarea acestei imunoterapii în SUA și în UE. În continuare, pentru a obține extinderea indicației și în alte tipuri de cancer, au fost inițiate mai multe trialuri clinice, reunite în programul JAVELIN. Printre acestea se numără cancerul gastric, cancerul pulmonar, cancerul renal și cancerele de cap și gât.
Cancerul de vezică urinară are cea mai mare rată de recurență dintre neoplazii. Majoritatea pacienților pot fi tratați prin terapii care cruță vezica urinară (nu necesită excizia chirurgicală a acestui organ), însă în multe cazuri se înregistrează recurența sau progresia bolii. Pacienții diagnosticați cu tumori uroteliale avansate primesc diverse forme de chimioterapie, care reușesc să controleze boala în aproximativ 65-75% din cazuri. Cu toate acestea, perioada de supraviețuire fără progresul bolii este scurtă din cauza rezistenței la agenții terapeutici.
Cancerul urotelial are punct de plecare țesutul care căptușește tractul urinar inferior. Este a șasea cea mai frecventă formă de cancer în UE, cu 124.000 de pacienți diagnosticați în fiecare an și peste 40.000 de decese anual, și se află în top 10 al cancerelor cu cele mai înalte rate de deces în SUA. La nivel global, ocupă locul 5 ca incidență, și reprezentă 6.6% din totalul cazurilor de cancer la nivel mondial. Este de 5 ori mai frecvent la bărbați decât la femei iar riscul crește odată cu vârsta.
Citește și:
- FDA aprobă pembrolizumab pentru cancerul de vezică urinară incipient, care nu răspunde la tratamentul BCG
- #ASCO20. Pacienții oncologici, la risc în contextul infecției COVID-19. Chimioterapia și tratamentul cu hidroxiclorochină și azitromicină asociate riscului de deces
- Predicția asupra supraviețuirii pacienților cu cancer urotelial avansat tratați cu atezolizumab

