Larotrectinib, primul tratament „tumor-agnostic” recomandat spre aprobare în UE pentru cancerele solide care prezintă fuziuni NTRK
Comitetul pentru Produse Medicamentoase de Uz Uman (CHMP), din cadrul Agenției Europene a Medicamentului, a emis o recomandare pentru aprobarea de punere pe piață a medicamentului larotrectinib. Decizia finală din partea Comisiei Europene este așteptată în următoarele luni.
Larotrectinib este primul tratament independent de tipul histologic pentru tumori solide recomandat pentru aprobare în Uniunea Europeană. Medicamentul e deja aprobat în Statele Unite ale Americii precum și în Brazilia și Canada. Acesta este indicat este indicat atât adulților cât și copiilor cu tumori solide care prezintă fuziuni NTRK (Neurotrophic Tyrosine Receptor Kinase), local avansate sau metastatice, în cazul în care rezecția chirurgicală nu poate fi considerată o soluție și lipsesc alternativele terapeutice.
Înainte ca pacienții să primească tratamentul, mutația trebuie să fie confirmată cu ajutorul unor teste genetice valide, conform CHMP.
Oricât de frecvent auzim în ultimul timp în oncologie cuvinte precum „schimbare de paradigmă”, noua decizie legată de larotrectinib reprezintă unul dintre puținele cazuri în care descrierea chiar se potrivește. Dr. Noah Fedeman, unul dintre autorii studiilor care au stat la baza aprobării, a declarat pentru Medscape:
„Acesta este un pas foarte important pentru oncologie. În peste 10 ani de experiență în tratarea tumorilor solide la copii, adolescenți și adulți tineri la UCLA nu am văzut aceste răspunsuri pe care le obținem cu larotrectinib.” – Dr. Noah Fedeman, Jonsson Comprehensive Cancer Center, University of California at Los Angeles (UCLA)
Rate de răspuns ridicate în mai multe tipuri de neoplasme
Eficacitatea și siguranța tratamentului au fost evaluate în trei studii, care au inclus în total 102 pacienți: un studiu de fază I care a inclus pacienți adulți, studiul de fază II NAVIGATE care a inclus adulți și adolescenți și studiul de fază I/II SCOUT în care au participat pacienți pediatrici.
Recomandarea pentru aprobare condiționată se bazează pe date semnificative demonstrate de larotrectinib în aceste studii:
- 67% dintre pacienți au răspuns la tratamentul cu larotrectinib;
- în cazul a 88% dintre aceștia răspunsul a durat cel puțin 6 luni, iar în cazul a 75% a durat până la 1 an;
- s-au observat răspunsuri favorabile atât în cazul tumorilor rare precum fibrosarcomul infantil sau tumorile de glande salivare, precum și în afecțiuni mai frecvente precum cancerul de colon sau pulmonar;
Dr. David Hyman, autor principal al studiului NAVIGATE a prezentat primele date despre larotrectinib în 2017, care ulterior au fost publicate în New England Journal of Medicine. Acesta a explicat că în toate tipurile de cancere care prezintă fuziunea NTRK s-au obținut rate de răspuns similare la terapia cu larotrectinib.
„Rata generală de răspuns era de 76%, ceea ce este neobișnuit pentru o terapie țintită. La 12% dintre pacienții care prezentau cancere avansate s-au înregistrat răspunsuri complete, un rezultat de care aproape nu s-a mai auzit până acum.”
Acesta a adăugat că „datele garantează pentru SCREENINGUL pacienților de toate vârstele cu tumori solide avansate”
Cum funcționează larotrectinib?
Larotrectinib este indicat pacienților care prezintă NTRK drept biomarker. Fuziunile NTRK apar în cazul unor tipuri de cancere rare care afectează atât adulții cât și copiii. Există trei variante ale genei NTRK – NTRK 1, 2 și 3 – care codifică familia receptorilor TrK (tromomyosin receptor kinase), alcătuită din trei proteine transmembranare TrkA, TrkB și TrkC. Acești receptori tirozin-kinazici sunt exprimați în țesutul neuronal și au un rol important în funcționarea sistemului nervos prin intermediul neurotrofinelor, substanțe care contribuie la dezvoltarea neuronală. Receptorii se află și la nivelul altor celule din organism precum plămâni, pancreas, oase sau sistemul imun.
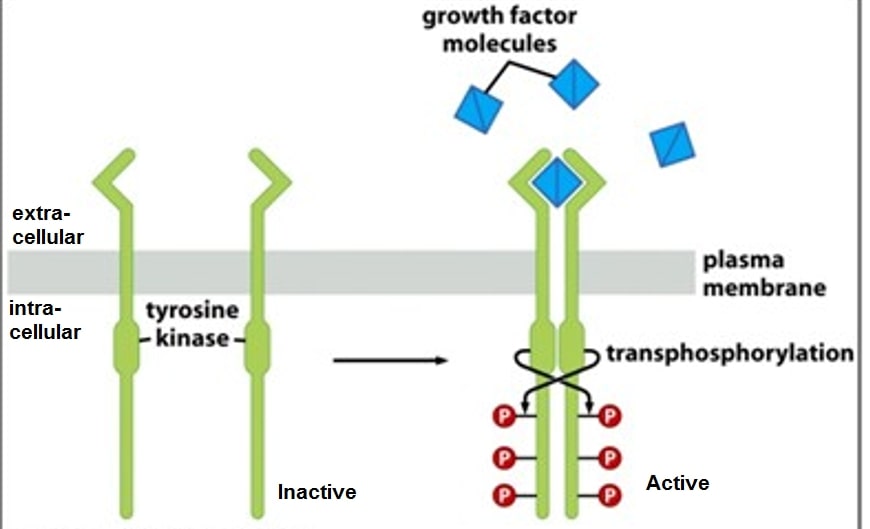
Genele NTRK pot fuziona într-un mod haotic cu alte gene, ceea ce va determina o amplificare a semnalelor de creștere activate prin Trk care pot induce carcinogeneza. Se cunosc peste 50 de tipuri de gene cu care se realizează această interacțiune.
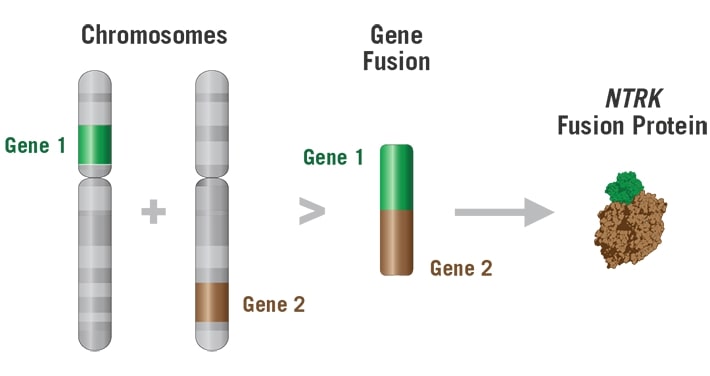
Fuziunea NTRK determină o semnalizare aberantă pe calea TRK și determină creșterea tumorală. Larotrectinib face parte din prima generație de inhibitori Trk, se leagă de receptori, ceea ce împiedică interacțiunea Trk – neurotrofine și determină apopotoza și inhibarea creșterii celulelor de la nivelul tumorilor care prezintă o supraexpresie a Trk.
Larotrectinib este singurul inhibitor pan-TRK selectiv, este considerat primul folosit într-adevăr într-o manieră „tumor-agnostic”, este prima terapie „tumor-agnostic” orală și este prima terapie dezvoltată simultan pentru adulți și copii.
Screeningul pacienților
Pentru ca pacienții cu aceste tipuri de mutații să fie tratați corespunzător, este necesar să fie și testați după noi standarde. Datele obținute din studii precum cele privitoare la larotrectinib susțin necesitatea testării genetice ca un standard de diagnostic.
Larotrectinib a fost aprobat în 2018 de FDA, fiind al doilea medicament din SUA aprobat pe baza profilului molecular și nu a subtipului histologic. Pembrolizumab a primit aprobare din partea FDA în 2017 pentru o indicație de tip tumor agnostic, în cazul tumorilor solide care prezintă instabilitate microsatelitară, însă acesta era deja aprobat pentru mai multe tipuri de cancere.
Însă, larotrectinib este primul medicament care are o indicație exclusiv de tip tumor agnostic și se adresează unei populații de pacienți despre care experții de la MD Anderson Cancer Center o descriu drept „acul în carul cu fân”, ceea ce ridică o serie de provocări în sistemul de sănătate. Accesul la testări genetice și la un diagnostic de precizie trebuie să fie pe lista de priorități.
Între 1-3 % dintre pacienții cu cancer pulmonar, cancer colorectal sau glioblastom prezintă această mutație. Însă, în cazul tumorilor rare, există tumori pentru care incidența mutației ajunge la 90%. Fuziunile NTRK apar la 91% dintre copiii cu fibrosarcom. Cancerul tiroidian se află pe locul 2 ca incidență a acestor anomalii genetice, fiind urmat de glioame. Cu toate acestea, este dificilă a estimare a numărului de pacienți care prezintă aceste anomalii genetice.
Dr. Noah C. Federman îndeamnă screeningul pacienților pentru fuziunea NTRK, mai ales în cazul tumorilor solide avansate sau metastatice.
Accesul la terapii de tip tumor-agnostic necesită schimbări majore în sistemele de sănătate
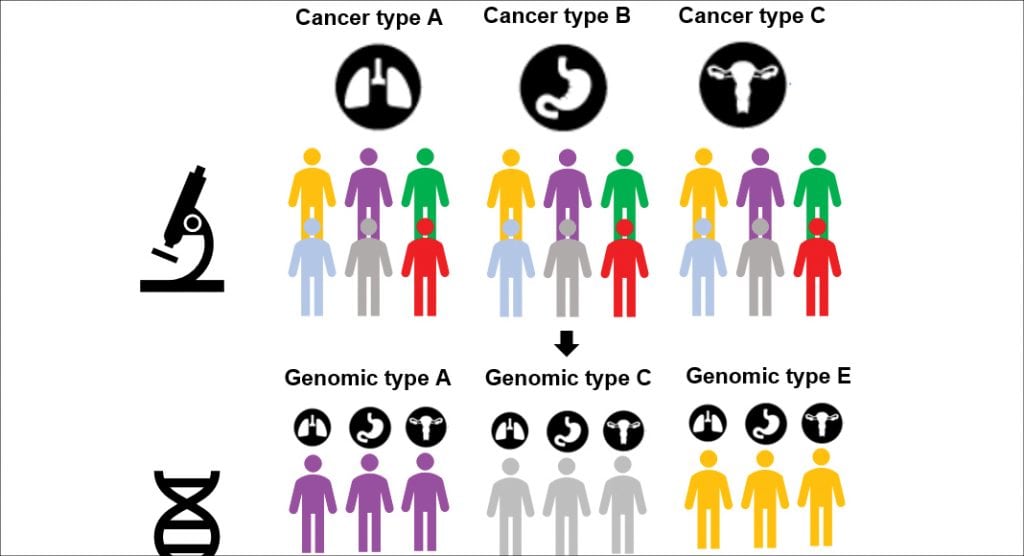
Cancerul începe să fie abordat ca o boală genomică iar obiectivele terapeutice se îndreaptă asupra descoperirii de noi mutații asupra cărora se poate acționa, identificarea de biomarkeri și selectarea populațiilor țintă care beneficiază cel mai mult de o anumită terapie.
Terapiile de tip tumor-agnostic care încep să intre pe piață determină și noi provocări pentru sistemul de sănătate – stabilirea valorii acestor terapii și modelul de rambursare pe de o parte și identificarea pacienților care ar beneficia de tratamente prin asigurarea accesului la noi metode de diagnostic, pe de altă parte.
„Pe măsură ce descoperim tot mai multe despre profilul genetic al tumorilor, devine din ce în ce mai important să asigurăm accesul la testări pe scară largă, astfel încât pacienții să beneficieze de medicina de precizie.” – Scott Fields, Directorul Departamentului de Oncologie de la Bayer
Țări precum Franța și Marea Britanie au stabilit deja bazele pentru dezvoltarea unei infrastructuri în sistemul medical pentru utilizarea NGS prin trasarea unor recomandări și obiective clare. În Germania se pregătesc ghiduri dedicate tratamentelor de tip tumor-agnostic. Conform unei analize realizate de A.T Kearney, defășurată în 5 țări europene și în Canada, o strategie care să permită accesul terapiilor de tip tumor agnostic trebuie să includă mai multe obiective precum:
- Medicina personalizată să fie considerată o prioritate – o înțelegere foarte bună din partea comunității științifice, stabilirea unor ghiduri pentru clinicieni care să includă noile terapii, existența unor programe guvernamentale dedicate terapiilor inovatoare și desigur existența unui plan național de control al cancerului;
- Stabilirea de noi mecanisme de rambursare și HTA;
- O schimbare de infrastructură în ceea ce privește diagnosticul și managementul datelor – crearea unor centre de excelență, investiții în tehnici precum NGS, WGS, etc
Citește și
- STUDIU: Larotrectinib, eficient în 17 tipuri de cancer în care este evidențiată fuziunea TRK. Se deschide era medicamentelor “tumor-agnostic” în terapia cancerului
- 5 inovații care vor schimba pentru totdeauna tratamentul cancerului, folosind sistemul imun al organismului
- BREAKING NEWS. Larotrectinib, terapia împotriva cancerului bazată pe tipul de mutație asociat, independent de localizare, a fost aprobată de FDA

