Olaparib, aprobat de FDA pentru tratamentul de menținere a cancerului pancreatic metastatic BRCA-pozitiv
Olaparib a fost aprobat de Administrația Alimentelor și Medicamentelor SUA (FDA) pentru tratamentul de menținere al cancerului pancreatic metastatic BRCA-pozitiv, care nu a progresat timp de minimum 16 săptămâni după un tratament chimioterapic pe bază de compuși de platină. În plus, FDA a aprobat și testul BRACAnalysis CDx de confirmare a prezenței mutației, obligatoriu pentru selecția pacienților eligibili pentru tratamentul cu olaparib.
„Olaparib ar trebui să devină un nou standard de tratament în cazul pacienților cu cancer pancreatic metastatic, BRCA-pozitiv”, afirmă Dr. Hedy L. Kindler, Universitatea din Chicago, cercetător principal în cadrul studiului.
Rezultatele studiului
Această aprobare vine în urma rezultatelor studiului POLO, care a demonstrat beneficiile olaparib în cancerul pancreatic metastatic BRCA-pozitiv.
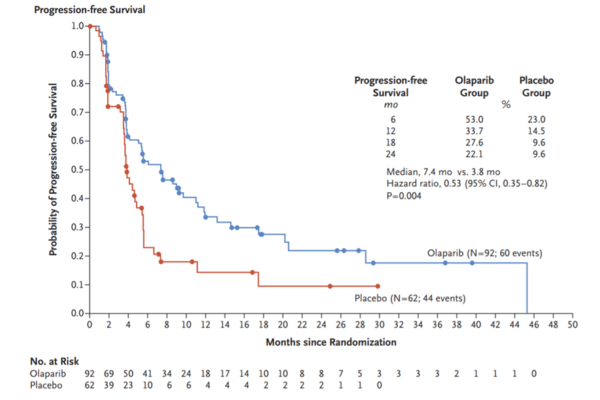
Sursa foto: NEJM
Studiul randomizat, dublu-orb, controlat cu placebo de fază III a inclus 154 de pacienți cu cancer pancreatic BRCA-pozitiv metastatic, care nu a evoluat sub chimioterapia de linia I (ce include compuși de platină). Astfel, 92 de pacienți au primit 300 mg olaparib oral de două ori pe zi, iar 62 au primit placebo. Rezultatele au fost semnificative:
- Supraviețuirea fără progresia bolii a fost de 7,4 luni în cazul tratamentului cu olaparib, față de 3,8 luni în cazul placebo;
- După 6 luni de la debutul studiului, de două ori mai mulți pacienți au supraviețuit fără progresia bolii în cazul olaparib, față de placebo (53%, față de 23%);
- În urma unei analize interimare a datelor, supraviețuirea globală a fost similară între cele două grupuri;
- Rata de răspuns a fost de 20% în cazul olaparib, față de 10% în grupul placebo;
- Grupul olaparib a suferit în proporție de 24% reacții adverse grave, față 15% în cazul grupului placebo.
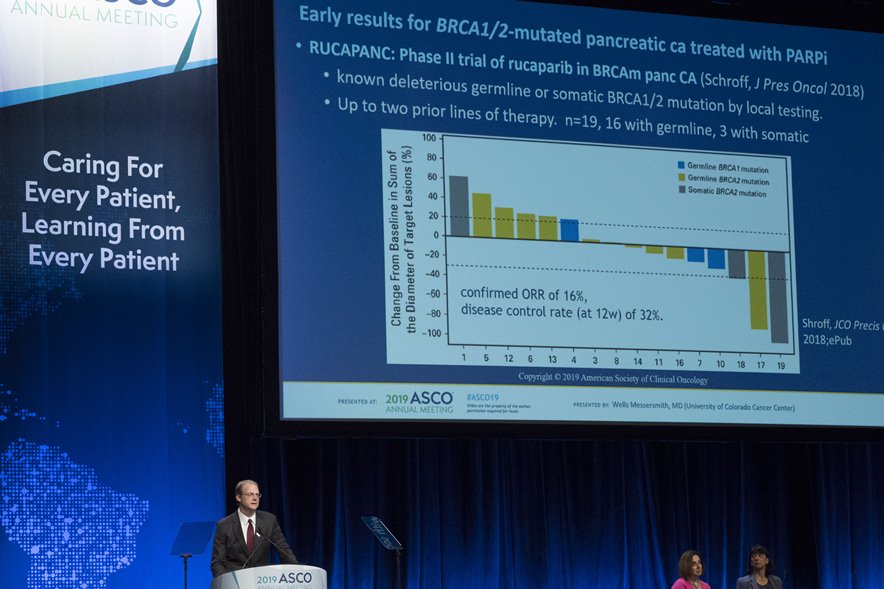
Sursa foto © ASCO/Phil McCarten 2019
Despre olaparib
Inhibitorul PARP, olaparib (denumire comercială Lynparza), este deja aprobat în cazul tumorilor BRCA-pozitive, localizate la nivel mamar sau ovarian. Celulele cu modificări metabolice cauzate de mutația BRCA sunt sensibile la acțiunea acestei clase terapeutice, prin intermediul unei enzime de reparare a ADN-ului, denumită PARP (poly-adenosine diphosphate–ribose polymerase). În cazul tumorilor BRCA-pozitive, celulele tumorale utilizează frecvent calea enzimatică PARP pentru a repara genomul și pentru a se multiplica. Astfel, prin inhibarea PARP, olaparib împiedică proliferarea tumorilor BRCA-pozitive.
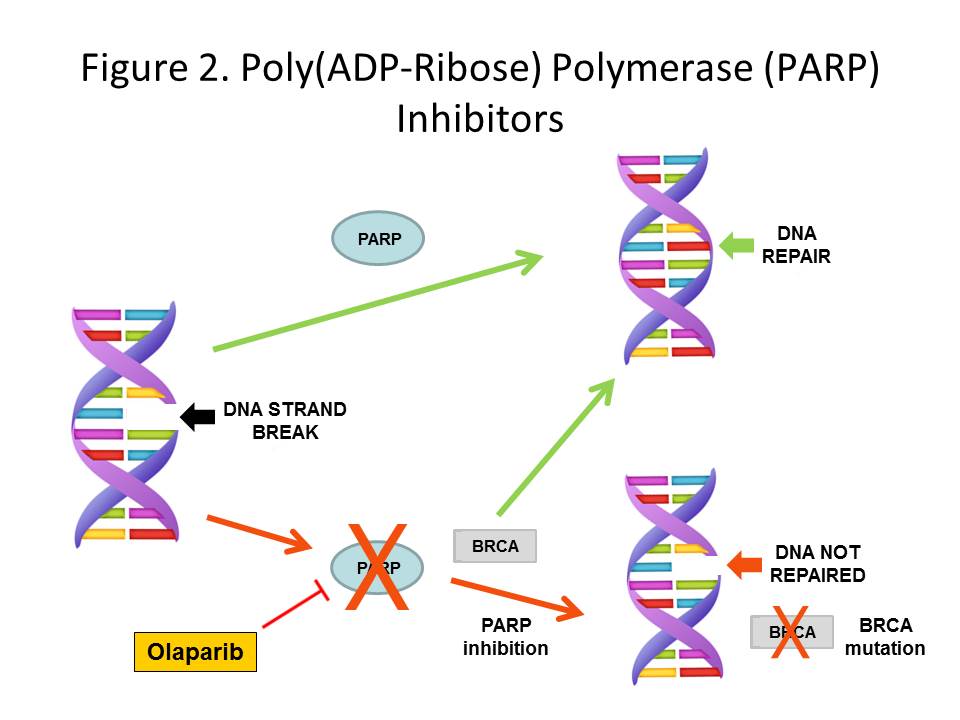
Tumorile pancreatice cu mutații la nivelul genelor BRCA1 sau BRCA2 reprezintă o proporție scăzută din totalul acestor tumori, de 4-7%. Tumorile pancreatice metastatice prezintă o agresivitate semnificativă: tratamentul actual conduce la o supraviețuire lipsită de progresie a bolii de aproximativ 6 luni, iar mai puțin de 10% dintre pacienți supraviețuiesc mai mult de 5 ani de la diagnostic.
Citește și:
- #ASCO19. Olaparib dublează numărul de pacienți în remisiune, în cazul cancerului pancreatic metastatic, BRCA-pozitiv
- STUDIU. Olaparib în cancerul ovarian avansat cu mutație BRCA: creștere a supraviețuirii fără progresia bolii când medicamentul este administrat în prima linie
- BREAKING NEWS. Olaparib, primul tratament pentru cancerul mamar BRCA pozitiv, aprobat de FDA

