BREAKING NEWS. Olaparib, primul tratament pentru cancerul mamar BRCA pozitiv, aprobat de FDA
FDA (Food and Drug Administration) a extins aprobarea medicamentului olaparib (Lynparza) pentru cancerul de sân metastatic, la persoanele care prezintă mutații la nivelul genelor BRCA. Olaparib este primul inhibitor PARP aprobat pentru tratarea cancerului mamar. Pentru identificarea corectă a pacienților cu mutațiile BRCA, FDA și-a dat acordul și pentru testul diagnostic BRCAnalysis CDx.
„Această aprobare demonstrează că tendința actuală este dezvoltarea de medicamente care țintesc cauzele genetice ale cancerului, adesea chiar între diferite tipuri de cancer.” – Dr. Richard Pazdur, Director al Centrului pentru Excelență în Oncologie din cadrul FDA
Informații cheie:
- FDA a aprobat medicamentul pe baza studiului randomizat de fază 3 OlympyiAD, care a arătat că neoplasmul mamar cu mutații la nivelul genelor BRCA1 și 2 este sensibil la terapii țintite
- olaparib determină o supraviețuire fără progresie a bolii mai mare decât chimioterapia
- ratele de răspuns au fost de 59,9% în favoarea olaparib, comparativ cu 28,8% în cazul chimioterapiei.
În 2014, olaparib a fost aprobat pentru cancerul ovarian BRCA pozitiv, la pacientele care au primit trei sau mai multe tratamente chimioterapice. La începutul acestui an, FDA a aprobat medicamentul și pentru cazurile de carcinom ovarian recidivat, cancer de trompe uterine sau cancer primar peritoneal, în cazul tumorilor care au răspuns total sau parțial la chimioterapie. Rucaparib (Rubraca) este un alt inhibitor PARP, aprobat pentru cancerul ovarian BRCA pozitiv. Niraparib (Zejula) este aprobat în cancerul ovarian indiferent de prezența mutației BRCA.
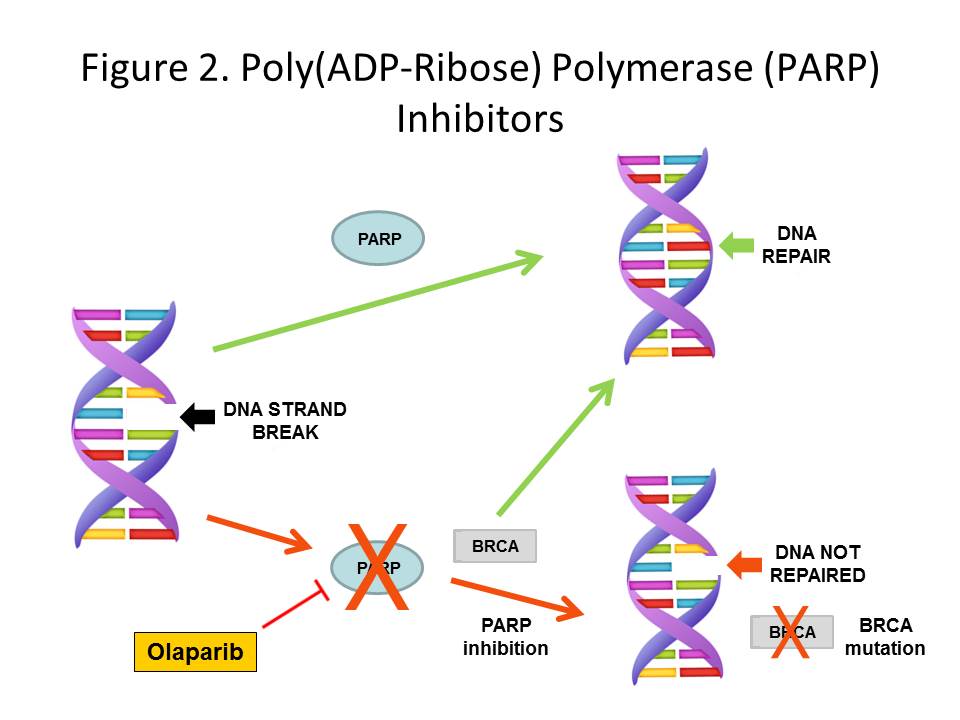
Între 10 și 15 % dintre cazurile de cancer mamar au o mutație BRCA. Olaparib funcționează prin inhibarea unei enzime implicate în repararea ADN-ului – PARP (poly-ADP-ribose polymerase) . Blocând această enzimă, ADN-ul celulelor canceroase nu mai poate fi reparat, ceea ce poate încetini sau stopa creșterea tumorală.
Profilul de siguranță și eficacitatea medicamentului au fost validate prin studiul OlympyiAD, prezentat în cadrul Congresului Societății Americane de Oncologie Clinică 2017 (ASCO). În acest studiu clinic randomizat au fost incluși 302 pacienți cu cancer de sân HER-2 negativ metastatic având mutația BRCA. Pacienții au primit fie 300 mg de olaparib de două ori pe zi sau chimioterapia standard care consta în 21 de cicluri de capecitabină sau vinorelbină sau eribulină.
Diferențele în ceea ce privește supraviețuirea fără progresia bolii au fost semnificative: 7 luni în cazul olaparib și 4.2 luni în cazul chimioterapiei. Ratele de răspuns au fost de 59,9% în favoarea olaparib, comparativ cu 28,8% în cazul chimioterapiei.
Olaparib a fost bine tolerat, mai puțin de 5% dintre participanți au întrerupt tratamentul din cauza toxicității.
Studiul dovedește faptul că neoplasmul mamar cu defecte la nivelul unei căi specifice de reparare a ADN-ului este sensibil la terapiile țintite.
Olaparib este produs de AstraZeneca. Pacienții care prezintă mutațiile BRCA pot fi identificați prin intermediul testului genetic aprobat de FDA și produs de Myriad Genetics, BRACAnalysis CDx.
În cazul femeilor cu o mutație BRCA, riscul de a dezvolta cancer de sân sau ovarian este mult crescut, 45-65% pentru cancerul de sân și 10-39% pentru cancerul ovarian, până la vârsta de 70 de ani. Bărbații cu mutații BRCA, în special BRCA2, au de asemenea un risc mare de a dezvolta cancer de sân.
Se estimează că în Statele Unite, din 155.000 de pacienți diagnosticați cu cancer de sân metastatic, 125.000 nu știu dacă prezintă o mutație BRCA.
BRCA 1 și 2 (BReast Cancer Associated) sunt gene cu rol de supresor al creşterii tumorale. Mutații la nivelul acestor gene determină sindromul cancerului ereditar de sân şi ovar.

Între 5 și 10% dintre cancerele de sân la femeie sunt atribuite mutațiilor BRCA1 și 2. La femeile cu o mutație BRCA, riscul de cancer de sân este de 5 ori mai mare decât în mod normal, iar riscul de cancer ovarian este de 10 până la 30 de ori mai mare. Mutațiile BRCA reprezintă 90% din cazurile de cancer de sân care au o influență genetică. Riscul de dezvoltare a cancerului apare la 60-80% dintre cei afectați.
Articole similare
- #ASCO2017: Olaparib încetinește progresia cancerului la sân metastatic, BRCA-pozitiv
- Dr. Mark Robson: olaparib vs. chimioterapie standard în tratarea cancerului la sân BRCA-pozitiv
- #ESMO17. 75% dintre pacientele cu cancer mamar sau ovarian nu și-au făcut testarea genetică, deși ar fi trebuit

