#SABCS2019. Trastuzumab deruxtecan crește ratele de răspuns în cancerul mamar HER2-pozitiv, avansat, la pacientele care au primit anterior multiple linii terapeutice
Trastuzumab deruxtecan a înregistrat o rată de răspuns de 61% în tratamentul femeilor cu cancer mamar HER2-pozitiv metastazat, care au primit anterior multiple linii terapeutice. Datele studiului clinic DESTINY-Breast01 de fază 2 au fost prezentate în cadrul San Antonio Breast Cancer Symposium (SABCS) 2019 și publicate în revista New England Journal of Medicine. Trastuzumab deruxtecan are potențialul de a deveni noul standard terapeutic pentru aceste paciente.
„Aceste rezultate sunt fantastice pentru pacientele tratate masiv dar fără rezultate”, a declarat Dr. Carlos Arteaga, co-directorul SABCS.
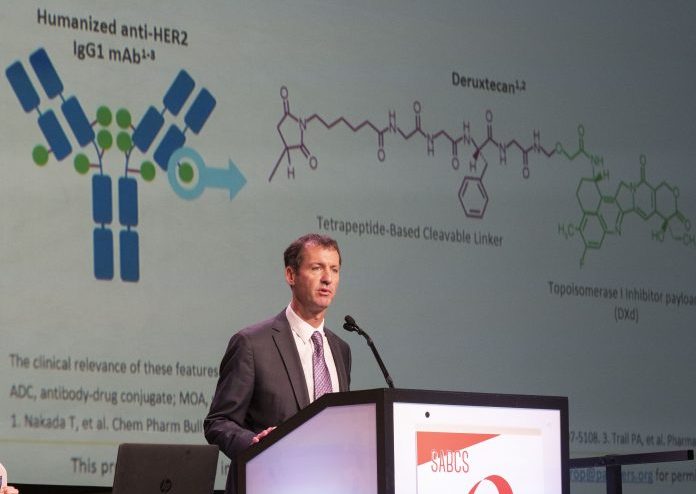
„Ratele de răspuns sunt duble sau triple față de ceea ce vedem în general în alte studii asupra pacientelor care se află la a treia sau a patra linie de tratament și la care supraviețuirea medie fără progresia bolii este în jur de 4-5 luni”, a afirmat Dr. Ian Krop, unul dintre principalii cercetători ai studiului, Division of Breast Oncology, Dana-Farber Cancer Institute, Boston.
Trastuzumab emtansine și trastuzumab deruxtecan sunt anticorpi monoclonali conjugați cu specificitate pentru HER2. Spre deosebire de trastuzumab emtansine care are un microtubul inhibitor în structură, trastuzumab deruxtecan conține un inhibitor de topoizomerază 1. În plus, are o rată mai mare medicament-anticorp (8 vs 3/4) și un profil farmacocinetic favorabil.
„Aceasta este o formă de terapie care nu se utilizează în mod tipic în cancerul de sân HER2-pozitiv, așa că este mai puțin probabil să existe deja rezistență la acest medicament” – Dr. Ian Krop.
Studiul DESTINY-Breast01
Studiul multicentric, de faza 2, a avut un singur grup de studiu care a inclus 184 de femei cu cancer mamar HER2-pozitiv metastazat și care mai fuseseră tratate anterior cu o medie de 6 linii terapeutice, inclusiv trastuzumab, trastuzumab emtansine, pertuzumab și alte terapii țintite. Li s-a administrat trastuzumab deruxtecan intravenos odată la 3 săptămâni.
Rezultatele studiului au fost următoarele:
- 60,9% din paciente au răspuns la tratament. 54,9% au înregistrat răspuns parțial iar 6%, răspuns complet. Rezultatele sunt în concordanță cu cele înregistrate în faza 1 a studiului, când s-a obținut o rată de răspuns de 59,5%.
- Activitatea terapeutică a fost asemănătoare în toate subgrupurile studiate, inclusiv în rândul pacientelor tratate deja cu pertuzumab, înregistrându-se rate de răspuns de 65%.
- Timpul mediu necesar pentru răspuns a fost de 1,6 luni.
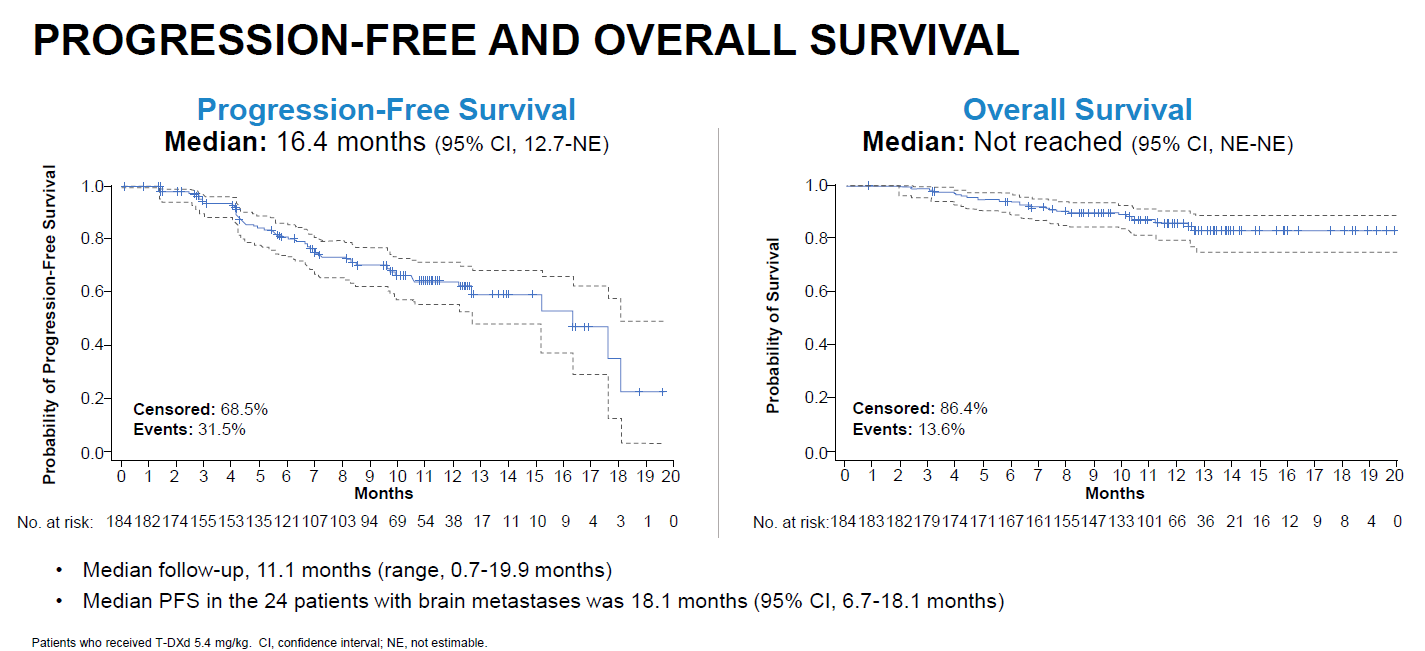
- Supraviețuirea medie fără progresia bolii (PFS) a fost de 16,4 luni. În subgrupul pacientelor cu metastaze cerebrale, durata medie a PFS a fost de 18,1 luni.
- Reacțiile adverse s-au înregistrat la 99,5% din paciente, 57% fiind de grad 3 sau mai mare: neutropenie, limfopenie, anemie, greață, fatigabilitate. Nu s-a observat toxicitate cardiacă, însă există risc potențial de boală pulmonară interstițiala.
„Răspunsurile semnificative clinic și durabile observate la paciente, sugerează potențialul trastuzumab deruxtecan de a deveni noul standard terapeutic. Rezultatele sunt impresionante având în vedere că pacientele cu forme avansate de cancer mamar au trecut deja prin multe terapii anterioare care vizează HER2” – José Baselga, vice-președinte executiv, Oncology R&D.
În prezent, trastuzumab deruxtecan este evaluat în mai multe studii clinice de faza 3. Trastuzumab deruxtecan a primit din partea FDA statutul prioritar (Priority Review), pe cel de medicament inovator (Breakthrough Therapy) și a intrat în procedura accelerată de aprobare (Fast Track), trei programe care cresc accesul la terapiile sunt considerate a aduce adevărate schimbări de paradigmă.

