Bavencio (avelumab): de la o descoperire de laborator la un tratament imuno-oncologic împotriva cancerului
Povestea imunoterapiei cu avelumab a început cu o informație importantă despre sistemul imun: acesta poate fi inhibat. Mai exact, limfocitele T („soldații” sistemului imun, care au rolul de a ataca și distruge celule străine corpului uman) prezintă un mecanism prin care pot fi inhibate, pentru a evita auto-imunitatea (atacarea celulelor proprii organismului). Acest mecanism este important pentru buna funcționare a imunității, dar s-a observat că diferite virusuri si celule tumorale pot profita, inhibând limfocitele T.
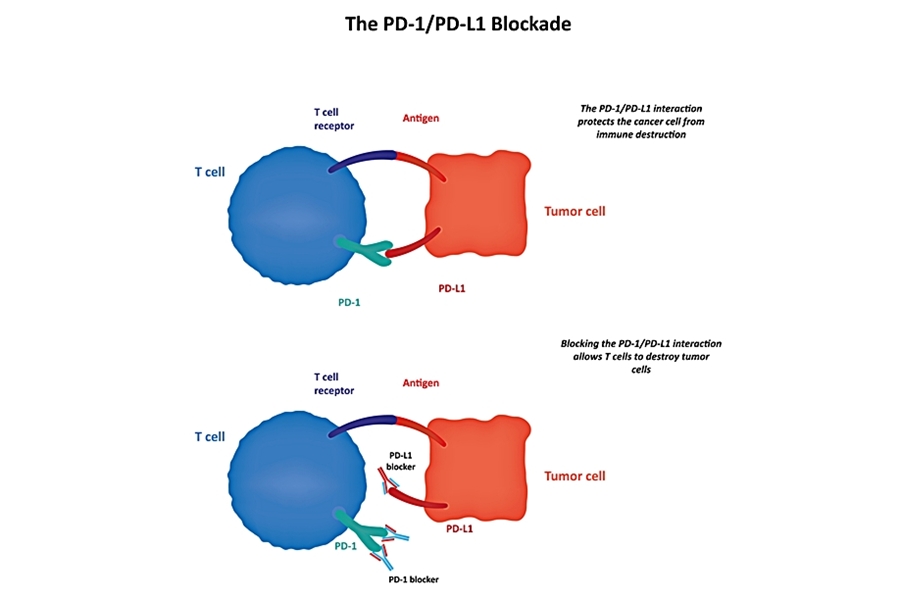
Unul dintre aceste mecanisme implică proteina PD1 (programmed-cell death receptor 1) de pe suprafața limfocitelor T. Această proteină este cunoscută din 1992, dar în 1999 a fost înțeles rolul de imunoinhibiție al acesteia (șoriceii cărora le lipsește PD1 dezvoltă numeroase boli autoimune).
Anumite tipuri de cancer prezintă pe suprafața celulelor PD-L1: o proteină care interacționează specific cu PD1, inhibând activitatea citotoxică a limfocitelor. La om, tumori care exprimă PD-L1 (mai rar PD-L2) includ cancerul urotelial, ovarian, mamar, cervical, de colon, pancreatic, gastric, pulmonar fără celule mici, diferite neoplazii ale sângelui și melanomul.
Potențialul terapeutic al acestei interacțiuni imunitate-cancer nu a rămas neexplorat: numeroase imunoterapii ce țintesc PD-1 sau PD-L1 sunt intens studiate în diferite boli tumorale.
Primele inhibitoare de PD-1 care au demonstrat beneficii clinice au fost nivolumab și pembrolizumab, ulterior aprobate în Statele Unite ale Americii pentru tratamentul melanomului și al altor neoplazii.
Inhibitorii de PD-L1 includ durvalumab, atezolizumab, și, recent aprobat în Europa: avelumab. Acesta a fost dezvoltat în laboratoarele companiei Merck și a demonstrat calități antitumorale încă din faza pre-clinică, în teste pe culturi de celule și pe șoricei.
La începutul anului 2013, primul pacient uman a primit avelumab, în cadrul unui trial clinic de fază I, iar rezultatele așteptate nu au întârziat să apară: răspunsuri complete și parțiale, în carcinomul cu celule Merkel.
O alianță care accelerează accesul pacienților la tratamente inovatoare

În noiembrie 2014, Merck a anunțat o colaborare strategică globală cu Pfizer, o altă companie farmaceutică care dezvoltă tratamente pentru cancer. Această alianță se concentrează pe avelumab și pe potențialul terapeutic al acestei molecule: implicarea acestuia în studii clinice pentru numeroase tipuri de cancer, în monoterapie sau în combinație cu alte produse create de Pfizer sau Merck.
Programul de dezvoltare pentru avelumab se numește JAVELIN, și la mai puțin de un an de la începutul colaborării Merck-Pfizer includea 6 trialuri clinice. Astăzi, 6.000 de pacienți, cu 15 tipuri diferite de cancer, primesc tratament cu avelumab, în cadrul a peste 30 de studii clinice.
“Această alianță permite Pfizer și Merck să își unească forțele, pentru binele pacienților cu diferite tipuri de cancer”, afirmă Albert Bourla, președinte Pfizer. “Imuno-oncologia reprezintă o prioritate importantă pentru Pfizer. Vom combina acest inhibitor de PD-L1 promițător cu numeroasele molecule dezvoltate de Pfizer: astfel putem extinde utilizarea imunoterapiilor în tratamentul pacienților cu cancer. Această alianță va accelera semnificativ dezvoltarea de noi studii și tratamente.”
Bavencio (avelumab): accesul pe piața europeană și nord-americană
Ultima etapă în procesul de dezvoltare a unui medicament îl reprezintă aprobarea și utilizarea efectivă ca tratament. În 2017, Bavencio (avelumab) a fost aprobat în Statele Unite ale Americii, Uniunea Europeană și în Japonia.
Primul pas a fost făcut în 2016, când FDA (Food and Drug Administration) a acordat avelumab titulatura de medicament-orfan pentru tratamentul carcinomului cu celule Merkel (o tumoră rară și deosebit de agresivă) și a accelerat procesul de aprobare. Ulterior, în 2017 FDA a aprobat Bavencio (avelumab) drept tratament pentru carcinomul cu celule Merkel în stadiu metastatic care nu răspunde la chimioterapie. În mai puțin de 2 luni, FDA a aprobat Bavencio (avelumab) și pentru tratamentul carcinomului urotelial avansat local sau metastatic, care nu răspunde la chimioterapie.
În Uniunea Europeană, Comitetul pentru Produse Medicale de Uz Uman (CHMP) al Agenției Europene a Medicamentului (EMA) a recomandat aprobarea punerii pe piață și, ulterior, Comisia Europeană aprobă Bavencio (avelumab) pentru tratamentul carcinomului cu celule Merkel în stadiu metastatic. Bavencio (avelumab) este aprobat și în Elveția, de către Agenția pentru Produse Terapeutice (Swissmedic), pentru carcinomul cu celule Merkel metastatic care nu răspunde la chimioterapie.
Cea mai recentă aprobare a venit din Japonia: Bavencio (avelumab) este primul și unicul tratament recomandat în carcinomul cu celule Merkel ce nu poate fi vindecat chirurgical.
Citește și:
Carcinomul cu celule Merkel: una dintre cele mai rare și agresive forme de cancer
Carcinomul cu celule Merkel: semnale de alarmă și metode de protecție împotriva bolii
Sistemul imunitar și apariția carcinomului cu celule Merkel. Ce rol are imunoterapia?

