Recomandare EMA de extinderea indicației pentru terapia CAR-T liso-cel: linia a II-a de tratament a limfoamelor non-Hodgkin cu celule B
Comitetul pentru Produse Medicale de Uz Uman (CHMP) din cadrul Agenției Europene a Medicamentului (EMA) a emis o opinie pozitivă cu privire la actualizarea aprobării de introducere pe piață a terapiei CAR-T lisocabtagene maraleucel (denumire comercială Breyanzi) pentru tratamentul adulților cu anumite limfoame cu celule B mari refractare sau recidivate, după administrarea unei linii anterioare de terapie. Aprobarea Comisiei Europene este așteptată în aproximativ 2 luni de la opinia favorabilă CHMP.
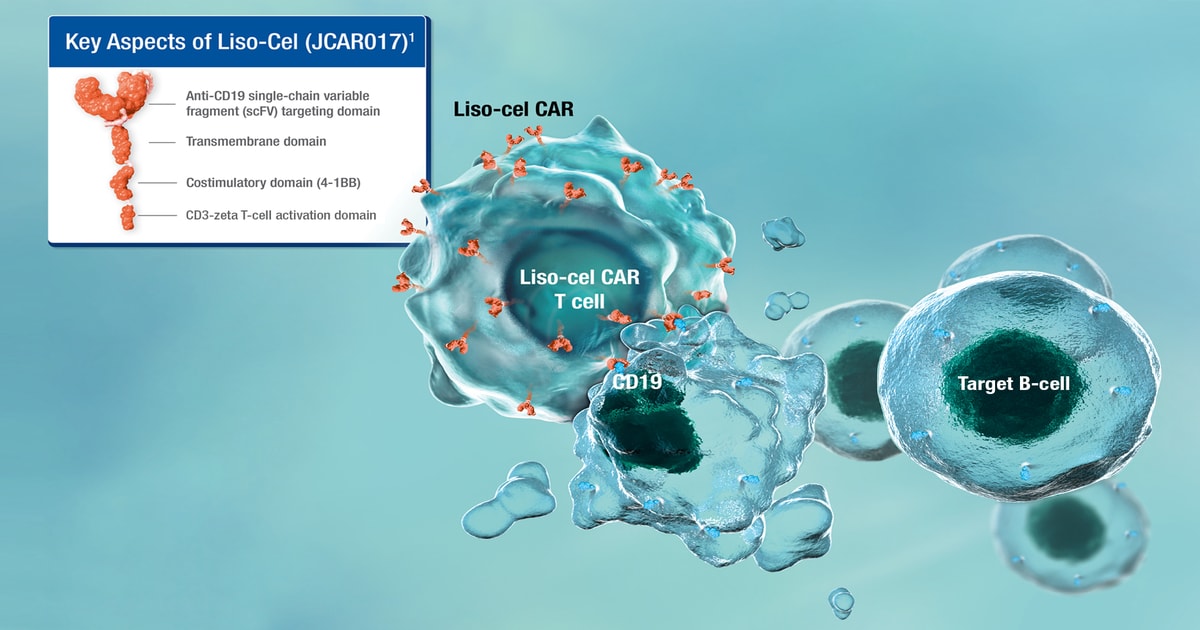
Mai exact, indicația este pentru pacienții cu limfom difuz cu celule B mari (DLBCL), limfom cu celule B de grad înalt (HGBCL), limfom mediastinal primar cu celule B mari (PMBCL) și limfom folicular de grad 3B (FL3B) a căror boală a recidivat în decurs de 12 luni de la finalizarea sau este refractară la chimio-imunoterapia de primă linie. În mod curent, liso-cel este aprobată în Uniunea Europeană pentru DLBCL, PMBCL și FL3B după două sau mai multe linii de terapie sistemică.
Pe lângă importanța clinică, extinderea indicației liso-cel reprezintă o bornă importantă în medicina de precizie în oncologie, devenind a doua terapie CAR-T care este indicată pentru linia a II-a de tratament în anumite limfoame non-Hodgkin cu celule B. Alte opțiuni terapeutice CAR-T pentru această clasă de cancere hematologice includ:
- Axicabtagene ciloleucel – pacienți adulți cu limfom cu celule B (HGBL, DLBCL, PMBCL, FL) refractar la prima linie de chimio-imunoterapie sau recidivant în primele 12 luni după prima linie de tratament (nu include limfomul primar al sistemului nervos central)
- Tisagenlecleucel – pacienți adulți cu limfom folicular refractar sau recidivant după cel puțin 2 linii anterioare de terapie sistemică (aprobată în UE în mai 2022)
Recomandarea are la bază rezultatele din studiul de fază III TRANSFORM, care a evaluat terapia ca tratament de linia a II-a, comparativ cu standardul de tratament. Liso-cel a condus la o îmbunătățire semnificativă a supraviețuirii generale, a ratelor de răspuns complet și a supraviețuirii fără progresie a bolii. La o urmărire mediană de 6,2 luni în ambele brațe de tratament, supraviețuirea mediană a fost de 10,1 luni cu liso-cel vs. 2,3 luni cu terapie standard. Rata de supraviețuire fără progresia bolii la o evaluare intermediară a fost de 14,8 luni cu liso-cel și doar 5,7 luni cu standardul de îngrijire. Mai multe detalii, aici.
Citiți mai multe informații despre studiile TRANSFORM (liso-cel), ZUMA-7 (axi-cel) și BELINDA (tisa-cel), care au evaluat terapii celulare CAR-T în limfoame non-Hodgkin cu celule B și susțin utilizarea acestora în linia a II-a de tratament, înlocuind standardul actual terapeutic în cazul DLBCL – transplantul autolog cu celule stem.
Citește și:
- #EHA2020. Terapia CAR-T Liso-Cel induce o rată generală de răspuns de 89% în limfomul non-Hodgkin cu celule B recidivant sau refractar
- FDA aprobă a treia terapie celulară CAR-T pentru limfomul cu celule B mari refractar sau recidivat

