FDA aprobă trastuzumab deruxtecan pentru tratamentul cancerului de sân HER2-pozitiv avansat
FDA (U.S. Food and Drug Administration) a aprobat Enhertu (fam-trastuzumab deruxtecan-nxki) pentru tratamentul adulților cu cancer mamar HER2-pozitiv, nerezecabil sau metastazat, care au primit anterior cel puțin două alte regimuri terapeutice în faza de metastazare.
”De la introducerea medicamentului Herceptin (trastuzumab) în anul 1998, s-a avansat mult în dezvoltarea terapiilor pentru cancerul de sân HER2-pozitiv. Aprobarea primita de Enhertu reprezintă cea mai nouă opțiune terapeutică pentru pacienții care au progresat urmând actualele terapii țintite anti-HER2”, a declarat Dr. Richard Pazdur, președintele Centrului de Excelență în Oncologie al FDA.
Enhertu este un anticorp monoclonal direcționat împotriva receptorului 2 al factorului uman de creștere epidermală (HER2). Astfel, medicamentul țintește modificările de la nivelul HER2 care favorizează creșterea, diviziunea și diseminarea celulelor canceroase. În plus, este conjugat cu un inhibitor de topoizomerază, care este toxic pentru celulele canceroase.
Trastuzumab deruxtecan a primit aprobare accelerată din partea FDA, care permite aprobarea medicamentelor indicate în afecțiuni severe în care există nevoi terapeutice neacoperite. În plus, trastuzumab deruxtecan a primit din partea FDA statutul prioritar (Priority Review) și pe cel de medicament inovator (Breakthrough Therapy). În continuare se vor derula studii clinice care vor verifica și descrie beneficiile clinice ale Enhertu.
”Dezvoltarea medicamentelor care fac parte din terapiile țintite se bazează pe înțelegerea noastră a bolilor maligne, nu numai a cancerului mamar” – Dr. Richard Pazdur.
Studiul clinic DESTINY-Breast01
Aprobarea Enhertu s-a bazat pe rezultatele studiului clinic de fază 2, care a înrolat 184 de femei cu cancer mamar HER2-pozitiv, nerezecabil și/sau metastazată. Aceste paciente primiseră anterior între 2 si 17 terapii țintite antiHER2 după ce boala metastazase, înainte de a primi Enhertu, care a fost administrat odată la fiecare 3 săpămâni. Evoluția terapeutică a fost urmărită prin investigații imagistice odată la 6 săptămâni.
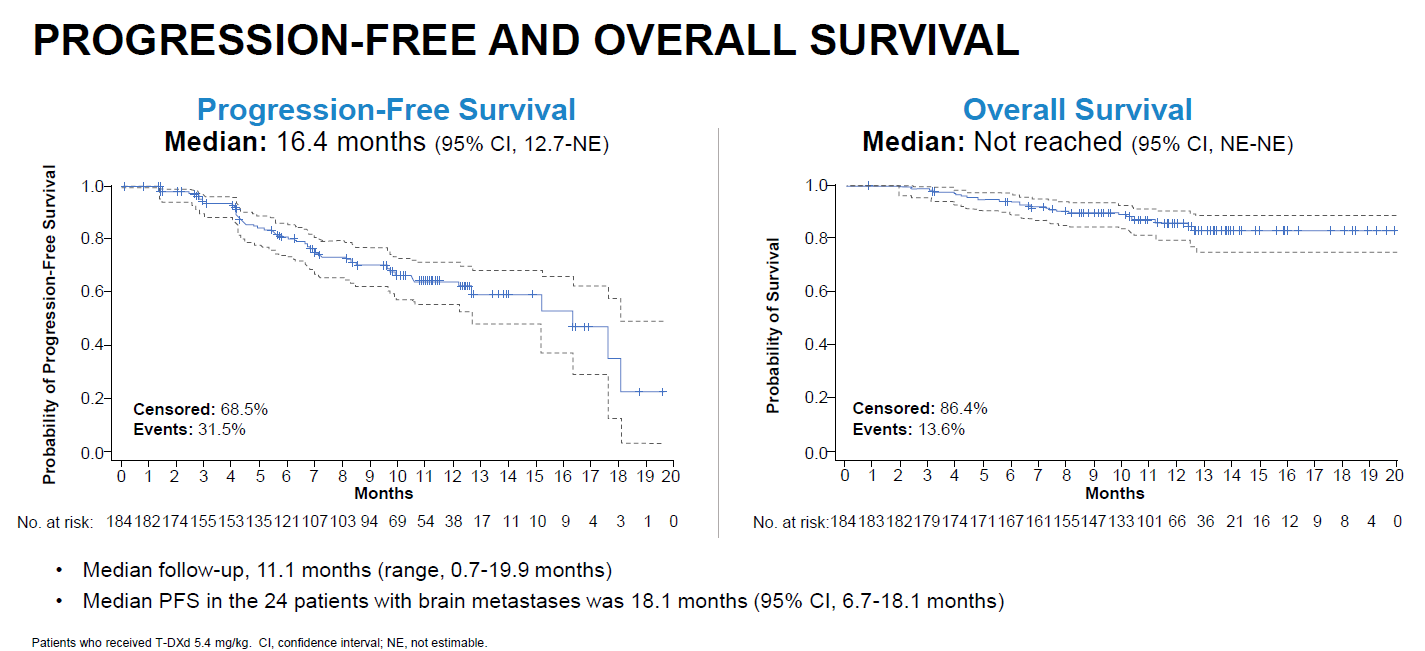
Rata generală de răspuns a fost de 60,3%, semnificând pacientele care au înregistrat scăderea dimensiunilor tumorale. Numai 4,3% din paciente au răspuns complet la tratament, restul de 56% au înregistrat răspuns parțial. Durata medie a răspunsului, de 14,8 luni, a fost demonstrată la începutul lunii august 2019. În plus, recent au fost prezentate rezultatele care au demonstrat o supraviețuire fără progresia bolii de 16,4 luni.
Enhertu se asociază cu risc de boală pulmonară interstițială și toxicitate embrio-fetală. Au fost raportate cazuri de pneumonie și/sau boală pulmonară interstițială (9% din paciente), inclusiv cazuri care au condus către deces (2,6%). Din acest motiv, este important ca medicii care prescriu medicamentul să monitorizeze semnele și simptomele sugestive, precum: tuse, dispnee (respirație dificilă), febră și agravarea altor simptome respiratorii. În cazul în care apar aceste semne și/sau simptome, se impune întreruperea temporară sau permanentă a administrării, sau reducerea dozelor. În plus, se interzice utilizarea medicamentului de către femeile însărcinate din cauza riscului de tulburări în dezvoltarea fătului și de complicații la naștere.
Cele mai frecvente reacții adverse asociate tratamentului cu Enhertu constau în: greață, vărsături, diaree, constipație, scăderea apetitului, fatigabilitate, alopecie, tuse, anemie, leucopenie, neutropenie, trombocitopenie. Pacienții prezintă risc crescut de a dezvolta disfuncție ventriculară stângă, problemă observată și în cazul altor terapii țintite anti-HER2.
Citește și:
- #SABCS2019. Trastuzumab deruxtecan crește ratele de răspuns în cancerul mamar HER2-pozitiv, avansat, la pacientele care au primit anterior multiple linii terapeutice
- #SABCS2019. Asocierea tucatinib la tratamentul cu trastuzumab și capecitabină crește supraviețuirea în cancerul mamar HER2-pozitiv metastazat
- #SABCS2019: Adăugarea capecitabinei la chimioterapia standard crește supraviețuirea în cancerul de sân triplu negativ, încă din stadiile timpurii ale bolii

