#WCLC2020. Combinația pembrolizumab – chimioterapie standard dublează supraviețuirea globală la 4 ani pentru pacienții cu cancer pulmonar non-microcelular metastatic, în linia I de tratament
Terapia cu pembrolizumab (Keytruda, Merck) și pemetrexed/chimioterapie cu derivați de platină dublează supraviețuirea la pacienții cu cancer pulmonar non-microcelular (NSCLC), subtipul non-scuamos, în comparație cu administrarea chimioterapiei standard, conform rezultatelor studiului Keynote-189. Rezultatele prezentate pe 28 ianuarie 2021 în cadrul Conferinței Mondiale despre Cancerul Pulmonar 2020 (WCLC2020,World Conference on Lung Cancer) provin din urmărirea pe parcursul a 4 ani a 160 de pacienți cu NSCLC în stadiu IV, netratați anterior.
Pembrolizumab reprezintă o imunoterapie care stimulează răspunsul imun împotriva celulelor maligne, prin blocarea PD-1 (programmed cell death protein 1). Keynote-189 este un studiu clinic de fază III care a început în 2016 și se află încă în curs de desfășurare.
Participanții la studiu au fost împărțiți în două brațe – un grup a primit terapie combinată (imunoterapie cu pembrolizumab + chimioterapie), iar celorlalți pacienți le-a fost administrată doar chimioterapie standard pentru NSCLC.
S-au obținut următoarele rezultate:
- După o perioadă mediană de urmărire de 46,3 luni, rata mediană de supraviețuire generală în grupul căruia i s-a administrat pembrolizumab și pemetrexed/chimioterapie cu derivați de platină a fost de 22 de luni, în comparație cu o supraviețuire generală de 10,6 luni în cazul grupului tratat doar cu chimioterapie;
- În ceea ce privește supraviețuirea fără progresia bolii (PFS), durata mediană a fost de 9 luni la pacienții cărora li s-a administrat combinația terapeutică, în comparație cu o PFS de 4,9 luni la pacienții care au primit doar chimioterapie.
La trei ani, rata supraviețuirii în urma terapiei cu pembrolizumab și chimioterapie a fost de 31,3%, față de 17,4% în grupul tratat doar cu chimioterapie, iar pentru PFS, rezultatele au fost 11,8% vs. 1,3%, în favoarea combinației imunoterapie-chimioterapie.
Rezultate favorabile au fost obținute și în pacienții ale căror tumori au avut o expresie scăzută a PD-L1 (programmed cell death ligand-1), măsurată prin PD-L1 TPS (PD-L1 tumor proportion score). Beneficiile administrării combinației pembrolizumab-chimioterapie asupra supraviețuirii generale și a supraviețuirii în lipsa progresiei au fost constatate indiferent de expresia PD-L1 la nivelul tumorii. Rata de răspuns general la terapie și durata răspunsului au fost îmbunătățite în urma terapiei cu pembrolizumab și chimioterapie, indiferent de expresia tumorală a PD-L1.
Rata de răspuns a fost de 87,5% la 56 de pacienți care au primit 35 de cicluri de terapie cu pembrolizumab, dintre care 10,7% au avut un răspuns complet, iar 76,8% un răspuns parțial la tratament.
Reacțiile adverse de grad 3-5 au fost asociate mai frecvent cu administrarea combinației imunoterapie-chimioterapie (52,1%) față de chimioterapie (42,1%). Evenimentele adverse de grad 3-5 de tip imun au fost constatate majoritar la participanții tratați cu pembrolizumab și chimioterapie (27,7%), în comparație cu chimioterapia (13,4%). Reacțiile adverse au determinat întreruperea terapiei în 27,4% dintre cazurile cărora le-a fost administrată combinația pembrolizumab-imunoterapie, față de 9,9% pentru participanții la studiu care au primit doar chimioterapie.
Când colectarea acestor date s-a finalizat, 45 de pacienți erau în viață, dintre care 28 nu au avut boală progresivă, iar 7 au început o nouă cură de terapie cu pembrolizumab.
Despre pembrolizumab
Pembrolizumab este o imunoterapie care funcționează prin blocarea PD-1 (programmed cell death protein 1), o proteină de pe suprafața limfocitelor T. Rezultatul este stimularea limfocitelor T să identifice și să elimine celulele maligne.
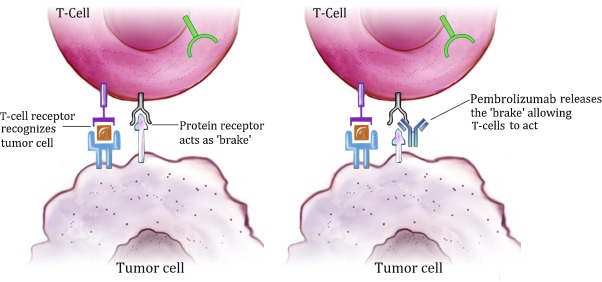
Sursa foto: ScienceDirect
Pembrolizumab reprezintă prima imunoterapie compensată în România, în asociere cu pemetrexed și chimioterapie pe bază de derivați de săruri de platină pentru tratamentul de primă linie al pacienților cu cancer pulmonar non-microcelular, non-scuamos, metastatic, la adulţi ale căror tumori nu prezintă mutații EGFR sau ALK pozitive. Imunoterapia cu pembrolizumab scade mortalitatea cu 50% dacă este administrată în combinație cu chimioterapia standard la pacienții cu NSCLC.
Citiți mai multe informații despre administrarea pembrolizumab în pacienții cu NSCLC.
Despre studiul clinic Keynote-189
Keynote-189 este un studiu clinic de fază III, randomizat, dublu orb care a debutat în ianuarie 2016 și se va încheia în martie 2022. Participanții la studiu sunt 616 cazuri avansate sau metastatice de cancer pulmonar non-microcelular, non-scuamos, care nu au primit anterior terapie sistemică pentru boală avansată. Studiul clinic Keynote-189 testează eficacitatea și siguranța pembrolizumabului administrat împreună cu pemetrexed/ chimioterapie cu derivați de platină, în comparație cu terapia doar cu pemetrexed/derivați de platină.
Principalele rezultate urmărite sunt: supraviețuirea fără progresia bolii (Progression-Free Survival, PFS) și supraviețuirea generală (Overall Survival, OS). PFS reprezintă timpul scurs de la debutul terapiei în cadrul studiului până la prima documentare a progresiei bolii sau până la decesul de orice cauză. Progresia bolii înseamnă o creștere cu minim 20% a leziunilor și cu 5 mm în valoare absolută sau apariția a una sau mai multe noi leziuni. OS reprezintă timpul scurs de la debutul administrării terapiei în cadrul studiului până la decesul de orice cauză.
Studiul a evaluat și rata de răspuns general la terapie (Overall Response Rate – ORR, procentul de participanți care au avut un răspuns complet sau parțial), durata răspunsului (Duration of Response – DOR, timpul scurs de la documentarea unui răspuns complet sau parțial până la progresia bolii sau deces), numărul participanților la studiu care au avut un eveniment advers, numărul participanților la studiu care au avut întreruperi în terapie din cauza unui eveniment advers.

