Terapiile CAR-T, o nouă dimensiune a personalizării tratamentului oncologic: cum diferă față de terapiile clasice și care sunt progresele în managementul cancerelor hematologice
În fenomenul de carcinogeneză sistemul imun joacă un rol esențial, iar limfocitele T reprezintă una dintre liniile principale de apărare. Răspunsul antitumoral al limfocitelor T devine însă insuficient din cauza mecanismelor de scăpare de sub detecția imună. Astăzi putem combina proprietățile naturale ale limfocitelor T cu metodele de inginerie genetică și biotehnologie.
Miliardele de celule T care circulă în organism pot recunoaște și elimina celule degradate, infectate de virusuri sau celule care se transformă malign. Deși pot recunoaște o varietate de ținte (antigene), în lupta împotriva cancerului, limfocitele T nu sunt instrumentele perfecte.
Pentru ca o celulă canceroasă să fie recunoscută de limfocitul T este important ca antigenele să fie exprimate pe suprafața ei. Dacă antigenul nu este exprimat pe suprafața celulei prin intermediul complexului major de histocompatibilitate (MHC), o componentă importantă a sistemului imun, celula nu va fi recunoscută de limfocitul T.
Limfocitele T pot fi modificate în laborator prin adăugarea unei porțiuni specifice a unor anticorpi – secvența de legare de antigen. CAR-T nu au această limitare a legării de antigen deoarece reprezintă structuri artificiale care pot avea ca țintă antigenele de pe suprafața celulelor canceroase chiar dacă acestea nu sunt exprimate cu ajutorul sistemului MHC.
Pentru exprimarea receptorilor CAR, ce țintesc antigene specifice este necesară introducerea unor instrucțiuni pentru limfocitele T. Aceasta se realizează prin reprogramarea lor genetică fie prin intermediul vectorilor virali, fie cu ajutorul editării genomice, o tehnică intens studiată.
Terapia celulară presupune transferul de celule pentru a înlocui sau a repara țesuturi afectate. Transplantul de celule stem hematopoietice reprezintă cea mai frecventă formă de terapie celulară, utilizată pentru tratarea cancerelor hematologice încă din anii `50. În ultimii 10 ani domeniul terapiilor celulare a cunoscut o expansiune rapidă.
Terapiile celulare reprezintă în prezent cel mai mare număr de agenți în dezvoltare în imuno-oncologie. La nivel global terapiile celulare includ peste 1000 de agenți activi, cu 250 mai mult decât acum un an. Dintre acestea, terapiile CAR-T au cunoscut cea mai mare dezvoltare, peste 560 de agenți terapeutici sunt studiați.
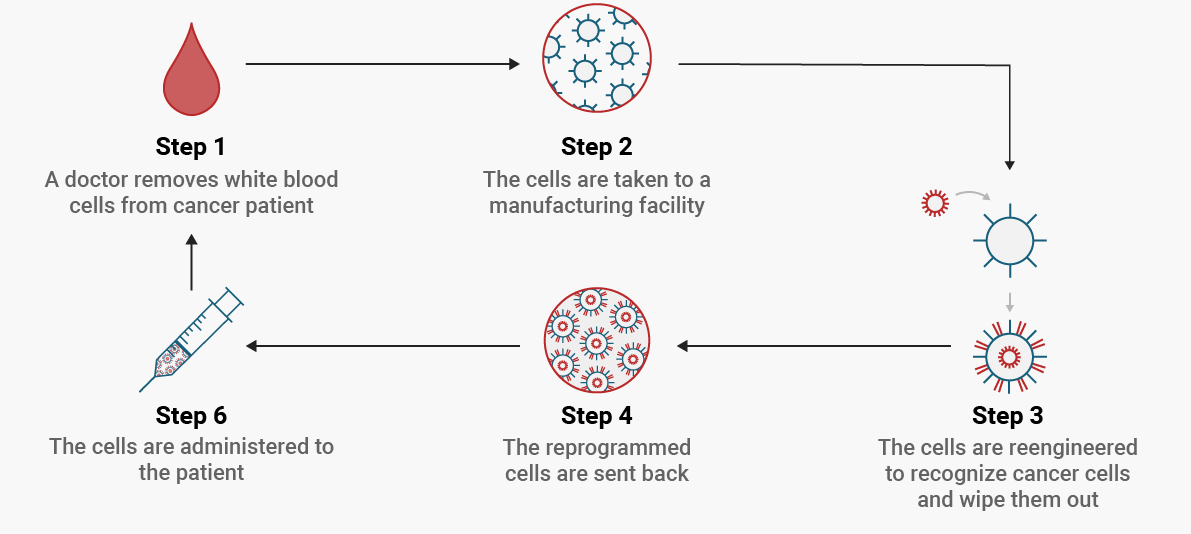
CAR-T reprezintă o schimbare radicală față de toate formele de tratament existente până în prezent. Aceasta presupune reprogramarea celulelor imune ale pacientului să lupte împotriva cancerului și este considerat un tratament cu potențial curativ. CAR-T reprezintă o nouă dimensiune a personalizării tratamentului în oncologie, reprezentând în același timp o terapie genică, terapie celulară și o imunoterapie.
Sursa foto: Business Insider
Limfocitele T sunt modificate prin biotehnologie astfel încât să exprime un receptor himeric (alcătuit din mai multe componente diferite) la suprafață. Domeniul extern al receptorului recunoaște anumite molecule de la nivelul celulelor tumorale și activează domeniul intern de semnalizare, astfel stimulând limfocitul T să atace celulele canceroase. Noile generații de receptori CAR prezintă domenii interne suplimentare care pot amplifica răspunsul imun împotriva unei anumite ținte.
Primele două terapii celulare CAR-T au primit aprobare din partea FDA în 2017. Tisagenlecleucel (Kymriah), cu indicație în leucemia acută limfoblastică și axicabtagen ciloleucel (Yescarta) pentru limfomul difuz cu celule B mari, cea mai frecventă formă de limfom non-Hodgkin.
Studiile clinice arătau că tratamentul cu Kymriah determină o rată de remisiune la 3 luni de aproximativ 82% în leucemia acută limfoblastică la pacienții care nu răspundeau la terapiile standard. Tratamentul cu Yescarta determină remisiunea la 72% dintre pacienții cu forme agresive de limfom non-Hodgkin.
În mai 2018, FDA extinde aprobarea pentru Kymriah și la pacienții cu limfom difuz cu celula mare de tip B refractar sau recidivat. În 2018, cele două terapii CAR-T sunt aprobate și în Uniunea Europeană, fiecare cu două indicații. Tisagenlecleucel este indicată la copii și tineri sub 25 de ani cu o formă refractară sau recidivată de leucemie acută limfoblastică și la adulții cu limfom difuz cu celule B mari. Axicabtagen ciloleucel a primit aprobare atât pentru limfomul difuz cu celulă B mare cât și pentru limfom mediastinal primar cu celule B mari. Societatea Americana de Oncologie Clinică (ASCO) a desemnat terapiile celulare CAR-T drept Inovația Anului 2018.
În cadrul Întâlnirii Anuale a Societății Americane de Hematologie, ASH 2019, două analize asupra datelor din practica medicală (real world experience) demonstrează eficacitatea tratamentului cu tisagenlecleucel pentru limfomul difuz cu celulă B mare (DLBCL) și leucemia acută limfoblastică (LAL).
Tratamentul este sigur și eficient pentru DLBCL, chiar și pentru categorii mai extinse de pacienți, pacienți vârstnici și cei tratați intensiv anterior. Mai mult decât atât, noile date din viața reală sugerează mai puține reacții adverse (sindromul de eliberare de citokine și reacții adverse neurologice) în cazul pacienților cu DLBCL, comparativ cu rezultatele din studiile clinice anterioare.
În cazul pacienților pediatrici și adulților tineri cu leucemie acută limfoblastică, recidivată sau refractară, eficacitatea tratamentului cu tisagenlecleucel confirmă datele obținute în studiul ELIANA. S-au înregistrat răspunsuri complete în 85% dintre cazuri, comparativ cu 82% în studiul ELIANA. Reacțiile adverse înregistrate au fost însă mult mai puține, conform analizei prezentate în cadrul ASH 2019.
Terapia CAR-T este complet diferită față de percepția convențională asupra unui medicament. Din clipa în care un medicament este administrat pacientului, acesta este degradat în organism și pacientul necesită o nouă doză. CAR-T este considerată o terapie „vie”, se regăsește în organism atâta timp cât există un antigen care poate fi țintit.
Pe lângă cele două tratamente aprobate, mai multe tipuri de terapii celulare CAR-T, atât de tip autolog cât și allogen sunt evaluate în studii clinice pentru diferite tipuri de neoplasme – alte tipuri de leucemii și limfoame dar și cancer de sân, cancer pulmonar, cerebral, mielom multiplu, cancer ovarian, etc.
CD19, antigenul exprimat mai ales pe suprafața limfocitelor B a reprezentat o țintă importantă pentru prima generație de terapii CAR-T. Cu toate acestea, atenția cercetătorilor se îndreaptă și asupra altor antigene tumorale cu scopul de a extinde utilizarea CAR-T dincolo de cancerele hematologice. BCMA (specifici pentru mielomul multiplu), CD123 (leucemia acută mieloidă) sau CD22 ( limfomul folicular) sunt doar câteva dintre țintele explorate în studii.
Tumorile solide cu siguranță ar reprezenta o piață mult mai largă pentru CAR-T însă tratamente eficiente sunt dificil de dezvoltat în prezent. Peste 30 de antigene asociate tumorilor solide sunt evaluate în studii care vizează terapiile celulare CAR-T.
Citește și:
- Noile generații de terapii CAR-T: cele mai importante studii prezentate la ASH 201
- State of Innovation 2019. Terapiile celulare CAR-T: momentul actual și direcții viitoare
- Terapiile CAR-T, eficiente și în cazul tumorilor solide: primele rezultate pozitive în studii de faza I

