State of Innovation 2019. Terapiile celulare CAR-T: momentul actual și direcții viitoare
Terapiile celulare CAR-T au reprezentat un moment de răscruce în oncologia modernă: această imunoterapie, care este în același timp terapie celulară și terapie genică a schimbat prognosticul într-o serie de cancere hematologice deosebit de agresive, iar rezultate promițătoare încep să apară și în cazul tumorilor solide.

Terapiile celulare CAR-T – un subiect important pe agenda evenimentului „Știința întâlnește Politicienii”, realizat de Centrul pentru Inovație în Medicină în parteneriat cu Comisia pentru Sănătate și Familie din Camera Deputaților și Comisia de Sănătate din Senat. Cu ocazia acestui eveniment a fost prezentat raportul anual State of Innovation, iar aplicațiile în domeniul oncologic au fost expuse pe larg în raport.
Ce înseamnă CAR-T și cum funcționează?
Terapia celulară CAR-T (Chimeric antigen receptor T cell – limfocit T cu receptor himeric pentru antigen) implică modificarea limfocitelor T, proprii pacientului, pentru a exprima receptori pentru antigenele specifice tumorale.
CAR-T face parte din clasa de tratamente numite imunoterapii – un segment în plină dezvoltare în cercetarea oncologică. Acestea funcționează apelând la o proprietate a cancerului puțin exploatată până acum, aceea de a se ascunde de sistemul imun și de a evita distrugerea.
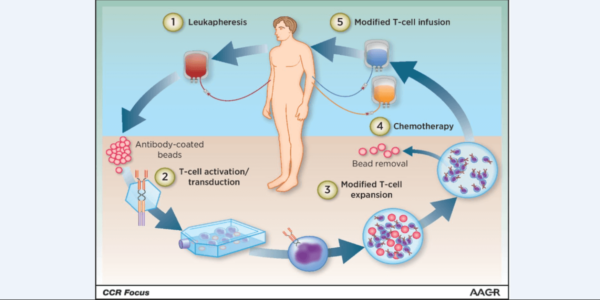
Terapiile CAR-T implică un proces de producție total diferit de medicamentele convenționale – întregul proces începe chiar cu pacientul. Dacă terapiile convenționale sunt produse în masă și ajung din laborator sau fabrică la pacient, pentru terapiile CAR-T există un circuit unic. Celulele imune (limfocitele T) sunt extrase cu ajutorul unui proces de leucafereză (separare a leucocitelor de alte celule sangvine) și trimise la laboratoare specializate, care utilizează tehnici de inginerie genetică pentru a echipa limfocitele cu „armele” necesare luptei contra cancerului. În acest scop se introduce un vector viral în celula imună, iar celula integrează în genomul propriu un fragment genetic, ceea ce o determină să exprime la suprafață anticorpi țintiți împotriva unor antigene specifice tumorii. În cazul celor două terapii CAR-T aprobate până în prezent, este vorba de anticorpi contra antigenului CD-19. Ulterior, limfocitele reprogramate sunt introduse în organism, fiind necesară o singură administrare, iar acestea își preiau rolul de distrugere a celulelor canceroase și rămân eficiente de-a lungul vieții pacientului.
Momentul actual în terapia celulară CAR-T
În acest moment, pacienții pot beneficia de două terapii CAR-T, Kymriah (tisagenlecleucel) și Yescarta (axicabtagene ciloleucel). Ambele au fost aprobate în Statele Unite (de către FDA) și în Uniunea Europeană (de către EMA).
Sursa foto: novartis.gcs-web.com
În 2017 au fost anunțate primele aprobări, în SUA: Kymriah a fost aprobat pentru tratamentul leucemiei limfocitare acute cu precursori de celule B, refractară sau recurentă, pentru pacienți cu vârsta sub 25 de ani. Această aprobare s-a bazat pe un studiu multicentric, care a observat o rată de remisiune la 3 luni, de 83%.

Ulterior, a fost aprobată Yescarta, pentru tratamentul adulților cu limfom non-Hodgkin difuz cu celule B mari, refractar sau recurent. În cadrul studiilor, Yescarta a condus la o rată de remisiune de 72%, cu o supraviețuire de 80% la 6 luni după administrarea tratamentului.
În 2018, Kymriah a primit a doua aprobare FDA, pentru aceeași indicație (limfom non-Hodgkin difuz cu celule B mari, refractar sau recurent).
Tot în 2018 au fost aprobate cele două terapii CAR-T și de către EMA, prin proceduri de aprobare accelerată.
Pe lângă terapiile deja aprobate, domeniul CAR-T este în plină dezvoltare: o analiză efectuată în 2018 descria un număr de 753 de terapii celulare în studiu, dintre care peste jumătate sunt terapii CAR-T.
Viitoarele provocări în utilizarea CAR-T
Pe lângă rezultatele excelente aduse de terapiile oncologice CAR-T, acestea aduc și o serie de provocări în sistemele de sănătate. Având în vedere procedeul complex de producere și administrare a terapiei, este necesară adaptarea circuitului pentru acest medicament și educarea personalului necesar.
Utilizarea terapiilor CAR-T poate fi mult limitată și datorită costurilor ridicate, datorează cauzate de procesul complex de producție și administrare, care implică modificări genetice induse de vectori virali, întregul proces durând mai mult de două săptămâni. Costurile tratamentului se ridică, în Statele Unite, la 300.000 – 400.000 de dolari, iar în țările membre UE are loc procesul de includere a terapiilor CAR-T în sistemul de rambursare.
Astfel, un sondaj în rândul hematologilor din 5 țări europene (Marea Britanie, Germania, Franța, Spania și Italia) a relevat principalele obstacole în administrarea CAR-T, în opinia acestora: costurile ridicate și procesul complicat de rambursare, numărul limitat de centre medicale capabile de administrare a tratamentului, nivelul insuficient de cunoștințe despre CAR-T al personalului medical și profilul de reacții adverse.
O altă provocare semnificativă în cadrul terapiilor CAR-T este reprezentată de extinderea utilizării acestora și la tumorile solide. Terapiile aprobate până în acest moment sunt utilizate împotriva unor cancere hematologice, cu o distribuție difuză în organism a celulelor tumorale, fără o localizare precisă a tumorii. Dacă în leucemia limfocitară cronică, celulele tumorale exprimă la nivelul limfocitelor B molecula CD19, în cazul tumorilor solide variabilitatea antigenelor exprimate este mult mai mare. Aceste tumori nu exprimă un antigen specific, ci un antigen asociat unui anumit tip tumoral. Această lipsă a specificității crește riscul de efecte off-target. Chiar și niveluri scăzute ale expresiei anumitor antigene în țesutul normal se poate asocia cu toxicități fatale. Astfel, aplicarea terapiilor CAR-T în tumorile solide reprezintă un domeniu intens studiat, care a adus deja o serie de rezultate promițătoare: studii de faza I descriu rate de răspuns de 72% în cazul mezoteliomului malign.

Este evident că adoptarea terapiilor CAR-T prezintă o serie de provocări fără precedent pentru sistemul medical din România. Raportul State of Innovation formulează recomandarea de înființare a unui grup de lucru, care să realizeze o strategie și un plan de acțiune pentru terapiile celulare CAR-T în România. Astfel, se încurajează adoptarea schimbărilor necesare în ceea ce privește infrastructura, formarea profesională, evaluarea noilor tehnologii medicale și compensarea terapiilor genice.
Citește și:
- O nouă terapie CAR-T eficientă în tratarea mielomului multiplu
- #ASH18: Inhibitorii punctelor de control asociați terapiei CAR-T pot crește răspunsul în leucemia acută limfoblastică recidivată
- CAR-T: terapie personalizată, celulară și imunoterapie. Cum se obține această terapie vie?

