UPDATE: Remdesivir este prima terapie aprobată de FDA, indicată în COVID-19. Care sunt tratamentele studiate și utilizate în protocolul terapeutic contra infecției cu SARS-CoV-2?
UPDATE 23 octombrie 2020. Administrația Alimentelor și Medicamentelor din Statele Unite ale Americii (FDA) a aprobat primul tratament indicat în infecția cu SARS-CoV-2. Molecula antivirală remdesivir (denumire comercială Veklury) poate fi administrată la pacienții cu COVID-19 confirmat, de vârstă adultă sau pediatrici (cu vârsta peste 12 ani și greutatea corporală peste 40 kilograme). Remdesivir este indicat în mod exclusiv formelor de infecție care necesită îngrijiri în cadrul unei instituții medicale, de exemplu, un spital.
Remdesivir a primit, în luna mai 2020, autorizație de urgență (EUA) pentru utilizarea în COVID-19, formele severe. Aprobarea actuală nu include cu exactitate toți pacienții, mai ales cei pediatrici. De aceea, reglementările EUA inițiale au fost modificate pentru a include copiii spitalizați, COVID-19 pozitivi sau suspecți, care au sub 12 ani și o greutate corporală între 3,5 kilograme și 40 de kilograme. În această grupă de pacienți, este necesară continuarea studiilor pentru a confirma beneficiile și siguranța remdesivir, pentru a se emite o aprobare definitivă.
Studiul ACTT, organizat de Institutul Național de Boli Alergice și Infecțioase din SUA (NIAID), este dublu-orb, randomizat, cu grup placebo, și a urmărit 1.062 de pacienți internați cu forme ușoare, moderate și severe de COVID-19, care au primit îngrijirile medicale standard, împreună cu remdesivir sau placebo:
- Recuperarea în urma infecției a fost definită drept externarea din spital sau întreruperea oxigenoterapiei sau tratamentului medical continuu;
- În medie, pacienții care au primit remdesivir s-au recuperat în 10 zile, semnificativ mai rapid decât grupul placebo, cu 15 zile;
- Proporția de pacienți recuperați în urma a 15 zile de spitalizare pentru COVID-19 a fost semnificativ mai mare în grupul de studiu.
Al doilea studiu, de fază III, a comparat administrarea remdesivir timp de cinci (191 pacienți) sau zece zile (193) cu administrarea de placebo (200), la pacienții cu forme moderate COVID-19. În ziua 11 de spitalizare:
- Cele mai bune rezultate au fost obținute în grupul care a primit cura de 5 zile;
- Rata de remisie a simptomatologiei este semnificativ mai mare în grupul remdesivir 5 zile, versus placebo.
Al treilea studiu, de fază III, open-label, multicentric, randomizat, a urmărit efectele remdesivir în formele severe COVID-19 la adulți, un grup primind 5 zile acest tratament antiviral (200 de pacienți), alt grup primind timp de 10 zile (197). În ziua 14 de spitalizare:
- Rata de remisie a simptomatologiei a fost similară în cele două grupuri;
- Rata de recuperare în urma infecției și de deces în urma infecției nu a variat în mod semnificativ între cele două grupuri.
„FDA este dedicat accelerării în dezvoltarea tratamentelor COVID-19, pentru a face față acestei urgențe de sănătate publică. Aprobarea de astăzi se bazează pe datele culese din numeroase studii clinice, atent analizate de FDA, considerate puncte de reper în desfășurarea pandemiei actuale. În cadrul Programului de Accelerare Terapeutică contra Coronavirusului, din cadrul FDA, vom continua eforturile de a oferi pacienților noile produse terapeutice, cât mai rapid posibil, luând în calcul, permanent, balanța risc-beneficiu,” a declarat Comisarul FDA dr. Stephen M. Hahn.
UPDATE 15 octombrie 2020: Studiul OMS pentru tratamentul COVID-19: date preliminare pentru remdesivir, hidroxiclorochină, lopinavir/ritonavir și interferon
Organizația Mondială a Sănătății a publicat date preliminare provenite din studiul SOLIDARITY, considerat cel mai mare studiu asupra terapiilor candidate COVID-19. Acest studiu randomizat, desfășurat în peste 30 de țări, are mai multe brațe de tratament, iar fiecare centru medical poate alege studierea anumitor tratamente din cele propuse de SOLIDARITY, în funcție de disponibilitatea la nivel local.
Până în acest moment, 11.266 de pacienți au fost alocați în mod aleatoriu în cele 4 brațe de tratament:
- 2.750 au primit remdesivir;
- 954 au primit hidroxiclorochină;
- 1.411 au primit lopinavir;
- 651 au primit lopinavir + interferon;
- 1.412 au primit interferon;
- 4.088 au fost îngrijiți conform standardelor locale, cu tratament suportiv, fără moleculele studiate;
În total, rezultatele nu au indicat avantajul uneia dintre aceste terapii:
- Au fost înregistrate 1.253 de decese, la aproximativ 8 zile de internare;
- Rata de mortalitate la 28 de zile este de 11,8%:
- 39% dintre pacienții ventilați au decedat;
- 10% din pacienții fără ventilație au decedat;
- În ceea ce privește vârsta: 20% dintre pacienții ≥ 70 de ani și 6% dintre cei < 50 de ani au decedat.
Impactul moleculelor studiate asupra ratei de deces a fost nesemnificativ;
- Remdesivir a condus la un risc relativ de 0,95, lipsit de semnificație statistică (CI 0.81-1.11, p=0.50; 301/2743 decese în grupul de studiu, 303/2708 decese în grupul de control);
- Hidroxiclorochina a condus la un risc relativ de 1,19, lipsit de semnificație statistică (CI 0.89-1.59, p=0.23; 104/947 decese în grupul de studiu, 84/906 decese în grupul de control);
- Lopinavir nu a modificat nivelul de risc (RR=1.00, CI 0.79-1.25, p=0.97);
- Interferonul a condus la un risc relativ de 1,196, lipsit de semnificație statistică (CI 0.96-1.39, p=0.11; 243/2050 decese în grupul de studiu, 216/2050 decese în grupul de control).
Niciunul dintre aceste tratamente nu a scăzut mortalitatea cauzată de infecția cu SARS-CoV-2, în mod global și în subgrupurile de studiu (ventilație mecanică), și nu a condus la o rată scăzută de ventilație mecanică sau de spitalizare pentru COVID-19.
În luna martie 2020, Organizația Mondială a demarat studiul SOLIDARITY, care își propune să studieze în mod riguros, însă flexibil, efectele terapiilor promițătoare în infecția cu noul coronavirus SARS-CoV-2. Astfel, primele molecule incluse au fost remdesivir, lopinavir/ritonavir, hidroxiclorochină și interferon. În urma primelor rezultate, OMS a decis în lunile iunie și iulie renunțarea la studierea hidroxiclorochinei și lopinavir, iar renunțarea la interferon va avea loc în octombrie. Pe de altă parte, se vor introduce noi molecule în protocolul de studiu, precum anticorpii monoclonali, imunomodulatoare sau alte molecule antivirale.
UPDATE 1 mai 2020. Administrația Alimentelor și Medicamentelor SUA (FDA) a autorizat utilizarea remdesivir în infecția cu noul coronavirus SARS-CoV-2, prin procedura specială de urgență (EUA – Emergency Use Authorisation). Această aprobare permite medicilor să administreze remdesivir pacienților cu infecție suspectată sau confirmată, formă severă (au saturația sangvină în oxigen SpO2 ≤ 94%, necesită oxigenoterapie, ventilație mecanică ori oxigenare extracorporală arterio-venoasă cu membrană/ECMO), chiar în afara studiilor clinice. Totuși, EUA nu reprezintă o aprobare completă, deoarece mai sunt necesare studii pentru a confirma eficacitatea acestui tratament.
Aprobarea de urgență survine în urma publicării unor rezultate încurajatoare, provenite din două studii care au implicat remdesivir:
- Studiul ACTT, organizat de Institutul Național de Boli Alergice și Infecțioase din SUA (NIAID):
- Fază III, randomizat, controlat cu grup placebo;
- 1.063 de pacienți incluși;
- Pacienții tratați cu remdesivir au prezentat ameliorare clinică după o perioadă cu 31% mai scurtă;
- Grupul de studiu a avut o durată mediană de recuperare de 11 zile, față de 15 zile în grupul de control;
- Grupul de studiu a avut o mortalitate de 8%, față de 11,6% în grupul de control.
- Studiul SIMPLE, organizat de Gilead (compania producătoare a remdesivir):
- Fază III, fără grup de control – pacienții primesc o cură de remdesivir de 5 sau 10 zile;
- Ameliorarea clinică a fost similară în cele două grupuri;
- Jumătate dintre pacienți au prezentat o ameliorare a bolii în primele 10 zile, în cazul tratamentului de 5 zile, și în primele 11 zile (tratamentul de 10 zile);
- După 14 zile, 60% dintre pacienții care au primit remdesivir timp de 5 zile au fost externați, și 52,3% dintre cei care au primit timp de 10 zile.
Plasma prelevată de la pacienții vindecați, potențial tratament în formele severe COVID-19
Tratamentul contra COVID-19 este în acest moment un subiect intens studiat, prin studii clinice randomizate. Candidații cei mai probabili includ antivirale (remdesivir, sau terapii anti-HIV precum ritonavir/lopinavir), antimalarice (hidroxiclorochina) sau imunomodulatoare (tocilizumab). O altă variantă care se dovedește promițătoare este utilizarea plasmei prelevate de la pacienții vindecați. Numărul de pacienți vindecați este în continuă creștere (se estimează că există peste 700.000 de persoane vindecate la nivel mondial, dintre care aproape 2.500 în România), iar aceștia sunt încurajați să doneze plasmă, pentru tratamentul experimental al pacienților COVID-19.

Această terapie se bazează pe capacitatea sistemului imunitar de a produce anticorpi, cu rol protectiv pe termen lung, împotriva unei infecții cu care s-a confruntat recent. Astfel, la pacienții vindecați de COVID-19, se regăsesc anticorpi anti-SARS-CoV-2 în sânge, iar prin centrifugarea acestuia, se obține plasma (lipsită de celule sanguine), care are o concentrație mare de anticorpi. Există cazuri în care această terapie a fost benefică în forme grave de infecție cu SARS sau MERS (coronavirusuri înrudite cu SARS-CoV-2). Beneficiul maxim poate fi obținut în primele 7-10 zile de infecție, când organismul încă nu a format proprii anticorpi protectori.
Mai multe țări au anunțat inițiative de a trata astfel pacienții spitalizați cu COVID-19, precum Statele Unite și Marea Britanie. În România, Centrele de Transfuzie Sangvină pot contacta pacienții vindecați, identificarea loc având loc prin colaborarea cu spitalele unde au fost tratați. Procedura de prelevare prioritară este plasmafereza, însă se poate utiliza și prelevarea de sânge integral, cu separarea ulterioară a plasmei din acesta. Plasma este testată pentru prezența virusurilor HIV, VHB și VHC, anticorpilor anti-HLA (la anumiți donatori), și administrată pacienților cu forme severe de COVID-19 (internați la ATI, cu progresie rapidă, de > 50% în 24-48 ore a afectării pulmonare, ventilați mecanic sau necesitând în curând ventilație mecanică, din cauza dispneei, tahipneei și saturației în oxigen scăzute).
În afară de utilizarea directă a plasmei de la pacienții vindecați, aceasta poate fi utilizată pentru a realiza un tratament compus din imunoglobulină hiperimună policlonală. Astfel de inițiative au fost anunțate de companii farmaceutice, cu scopul de a demara studii clinice și de a oferi pacienților această terapie.
Primii pacienți cu COVID-19 au fost incluși în studiul SOLIDARITY organizat de OMS
Studiul SOLIDARITY a înrolat primii pacienți, în Spania și Norvegia (Spitalul Universitar Oslo). Acest studiu este organizat de Organizația Mondială a Sănătății, cu scopul de a identifica cel mai eficient agent antiviral contra SARS-CoV-2, dintre lopinavir/ritonavir (cu sau fără interferon beta), remdesivir și clorochină (sau hidroxiclorochină).
Spania și Norvegia sunt primele țări care au administrat tratamentul, din cele 45 care au aderat la acest proiect, până la momentul de față. Componenta norvegiană a studiului SOLIDARITY este înregistrată pe platforma oficială Clinical Trials și aduce mai multe detalii despre desfășurarea studiului: primii pacienți incluși din Norvegia fac parte din cohorta propusă de 700 de pacienți, care vor fi alocați în trei subgrupuri de studiu, în mod aleator: remdesivir, hidroxiclorochină și tratamentul standard (suportiv). Conform indicațiilor OMS, obiectivele urmărite sunt mortalitatea, durata de spitalizare și proporția de pacienți care necesită suport medical intensiv, în cadrul secțiilor de Terapie Intensivă. În plus, medicii norvegieni vor urmări și viteza cu care virusul este eliminat din organism (clearence viral din probe sangvine și respiratorii) și markeri biologici ai impactului acestuia asupra organismului (inflamație, activare endotelială și plachetară).

Protocolul terapeutic contra COVID-19 este aprobat în România
UPDATE 24 martie. Astăzi Ministrul Sănătății a emis ordinul prin care se aprobă protocolul terapeutic al infecției cu virusul SARS-CoV-2. Toate terapiile antivirale recomandate sunt molecule cu potențial efect contra COVID-19, conform cercetărilor preclinice și rezultatelor preliminare ale studiilor în cadrul COVID-19.
Tratamentul antiviral se administrează pentru o perioadă de minimum 5 zile (în lipsa reacțiilor adverse). Administrarea hidroxiclorochinei impune urmărirea pacientului prin electrocardiogramă (există risc de aritmii de tip QT lung). În cazul în care este necesară adăungarea unui antiviral la hidroxiclorochină, se preferă darunavir/cobicistat la pacienții cu risc de aritmii. Dacă remdesivir nu este disponibil, se poate înlocui cu lopinavir/ritonavir.
Terapiile antivirale sunt combinate cu terapii simptomatice, în funcție de forma de boală și prezența factorilor de risc:
- Afectare ușoară, fără pneumonie:
- tratament simptomatic (paracetamol)
- Afectare ușoară, fără pneumonie sau prezența de factori de risc (>65 de ani, comorbidități: cardiovasculare, hepatice, pulmonare, diabet):
- Lopinavir/ritonavir SAU
- Hidroxiclorochină
- Afectare medie (pneumonie fără semne de gravitate):
- Hidroxiclorochină ȘI
- Lopinavir/ritonavir
- Afectare severă:
- Hidroxiclorochină ȘI
- Remdesivir
- Sindrom inflamator excesiv și disfuncție de organ: se adaugă tocilizumab
Criteriile de afectare severă sunt:
- Saturația sangvină în oxigen <93% (pacient în repaus, fără comorbidități respiratorii);
- Procalcitonina sangvină >0.5 ng/ml;
- Detresă respiratorie acută;
- Confuzie/comă;
- Sepsis;
- Insuficiență multiplă de organ.
Pacientul este declarat vindecat și este externat în momentul în care prezintă:
- Ameliorarea simptomelor și semnelor clinice și radiologice;
- Dispariția febrei;
- Două teste PCR de identificare a ARN-ului viral negative (recoltate la 24 de ore distanță între ele, după 3 zile de afebrilitate și 7 zile de la confirmarea PCR a diagnosticului).
UPDATE 22 MARTIE. Tocilizumab și hidroxiclorochina, candidați la tratamentul COVID-19, sunt incluse în studii de fază II și III
Un nou studiu pentru identificarea unui potențial tratamentul contra COVID-19 este demarat, substanța cercetată fiind tocilizumab, un anticorp monoclonal care inhibă receptorul interleukinei 6 și este utilizat în reumatologie. Studiul, denumit COVACTA, va fi un studiu randomizat, dublu-orb, cu braț de control placebo, de fază III, care va urmări beneficiile tocilizumab adăugat la standardul de îngrijire (suport ventilator). Studiul va include 330 de pacienți la nivel mondial și va urmări starea clinică a acestora, împreună cu proporția de pacienți care necesită terapie intensivă, ventilație mecanică sau care dezvoltă forme severe de COVID-19, care evoluează cu deces.
Acest studiu vine în urma unor studii de caz, în care s-a observat că tocilizumab ameliorează starea clinică în cazuri grave de COVID-19, cu inflamație pulmonară avansată. Această utilizare se bazează pe aprobarea tocilizumab drept tratament în sindromul de eliberare de citokine (CRS), o manifestare inflamatorie la nivelul întregului organism, care poate fi reacție adversă la imunoterapia cu celule CAR-T. În cazul COVID-19, pătrunderea SARS-CoV-2 în organism stimulează o reacție imună, cu eliberare de citokine (printre care și IL-6) care stimulează febra, inflamația și fibroza pulmonare. Studii asupra cazurilor COVID-19 au demonstrat că niveluri ridicate de IL-6 în serul pacienților se corelează în mod semnificativ statistic cu evoluția severă a infecției. Alte terapii imunomodulatoare sau antiinflamatoare sunt în studiu, precum sarilumab (un alt inhibitor de IL-6), fingolimod (imunomodulator utilizat în scleroza multiplă), și eculizumab (inhibitor în cascada complementului).
Este important de subliniat că nu există un tratament aprobat împotriva infecției cu SARS-CoV-2. Astfel, toate potențialele tratamente se administrează fie off-label, fie în cadrul studiilor clinice, fie prin programe de compassionate use (o moleculă aflată în studii dar neaprobată încă, care poate fi administrată în cazurile grave de boală pentru care este studiată, care nu reunesc criteriile de includere a studiului clinic). Gilead, compania producătoare a remdesivir, una dintre cele mai promițătoare molecule studiate în COVID-19, a anunțat că remdesivir este disponibil pentru tratamentul de urgență a formelor grave, fără alte opțiuni terapeutice, printr-un program de compassionate use.
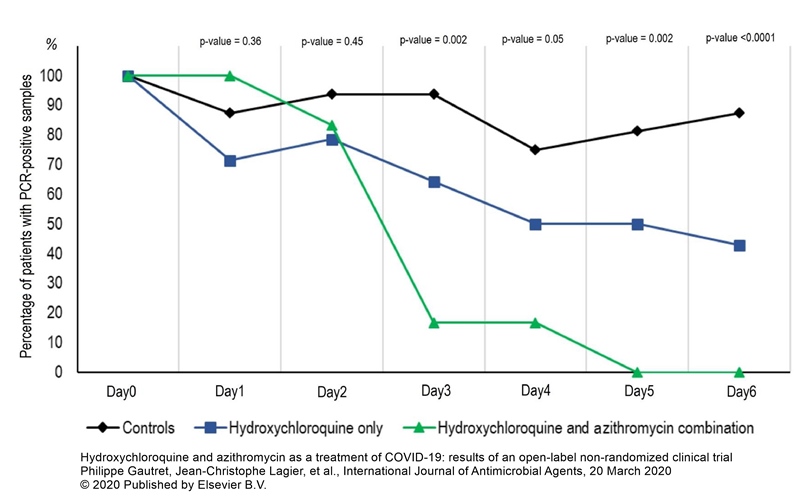
O altă moleculă cu potențial împotriva COVID-19, care a fost inclusă și în studiul SOLIDARITY, anunțat de OMS, este clorochina (sau derivatul acesteia cu profil de siguranță mai bun, hidroxiclorochina). Utilizată deja în tratamentul malariei și al unor boli autoimune și inflamatorii, aceasta acționează prin modificarea pH-ului intracelular, inhibarea glicozilării receptorilor celulari și a proteolizei virusului endocitat (ceea ce împiedică atașarea virusului de receptori și eliberarea ARN-ului). În plus, împiedică infecția și prin efectele sale imunomodulatorii – inhibă producția de citokine, procesul de autofagie și activitatea lizozomilor în celulele gazdă. Mai multe studii au fost demarate pentru a determina eficiența celor două molecule la pacienții infectați, împreună cu o altă utilizare – profilaxia infecției, la personalul medical expus noului coronavirus.
Studii de anvergură mai mică au condus deja la rezultate: un studiu cu 42 de pacienți a implicat administrarea hidroxiclorochinei, împreună cu azitromicina, și a condus la observația că aceasta scade încărcătura virală a pacienților după 6 zile de tratament, iar alte studii fără grup de control descriu ameliorarea manifestărilor radiologice ale bolii. Pe de altă parte, alte studii nu au observat diferențe notabile între pacienții care au primit hidroxiclorochină și cei care au primit placebo.
OMS demarează studiul SOLIDARITY, cel mai riguros studiu de identificare a tratamentui contra COVID-19
UPDATE 18 martie 2020. Organizația Mondială a Sănătății anunță cel mai mare studiu terapeutic centrat asupra coronavirusului SARS-CoV-2, denumit SOLIDARITY. În cadrul acestuia, mai multe molecule cu potențial terapeutic vor fi comparate între ele, pentru a alege cel mai eficient tratament împotriva COVID-19. Studiu va implica centre medicale din cel puțin 10 țări: Argentina, Bahrain, Canada, Franța, Iran, Norvegia, Africa de Sud, Spania, Elveția și Thailanda, iar procedura clară și simplă de intrare în studiu încurajează și alte țări să contribuie la descoperirea tratamentului.
Studiu va implica mai multe brațe de tratament, iar fiecare țară va putea alege liniile terapeutice testate, în funcție de tratamentele disponibile la nivel local. Aceste brațe de tratament sunt flexibile: molecule potențiale pot fi adăugate sau eliminate din comparație, pe măsură ce studiile aduc mai multe date. Standardul de îngrijire actual, care este reprezentat de suport respirator (oxigen), va fi comparat cu patru molecule/combinații de molecule: remdesivir, clorochina (sau hidroxiclorochina, mai ales în versiunea europeană a studiului), lopinavir/ritonavir, cu sau fără interferon-beta.
Obiectivele urmărite în studiul SOLIDARITY sunt rata de mortalitate generală a pacienților cu COVID-19, durata de spitalizare a acestora și proporția de pacienți care necesită suport medical intensiv, în cadrul secțiilor de Terapie Intensivă (cazuri severe de COVID-19).
În Europa, Institutul Național de Sănătate și Cercetare Medicală din Franța (Inserm) a anunțat studiul DISCOVERY, care va include aceleași molecule terapeutice și un total de 3.200 de pacienți din Belgia, Germania, Luxemburg, Olanda, Spania, Suedia, Marea Britanie. Mai multe centre medicale vor începe colectarea datelor, pe măsură ce apar noi cazuri, iar primele analize ale datelor vor fi realizate după 15 zile de tratament.

Coronavirusul SARS-CoV-2 reprezintă, la momentul actual, cel mai important subiect în cercetarea medicală: de la epidemiologie, până la posibile tratamente și vaccinuri, există numeroase necunoscute în această epidemie. În ceea ce privește tratamentul, există mai multe molecule cu potențial: de la remdesivir, un antiviral testat anterior în virusul Ebola, până la antiretrovirale utilizate contra HIV și antimalarice precum hidroxiclorochina. Totuși, un număr ridicat de studii de anvergură mică, cu metodologii diferite, nu pot identifica în mod adecvat cel mai eficient și sigur tratament. De aceea, proiectul SOLIDARITY are scopul de a oferi pacienților cu COVID-19 cel mai bun tratament, în cel mai scurt timp.
Tratament pentru infecția coronavirus SARS-CoV-2: peste 80 de studii clinice sunt în desfășurare. Remdesivir, medicamentul antiviral cu cel mai mare potențial terapeutic
Structura virusului a fost identificată într-un timp record, iar mecanismele infecției au fost descifrate în mare parte. Aceștia sunt primii pași pentru a dezvolta cele mai importante măsuri de control al infecției, pe lângă prevenție și igienă – o terapie țintită antivirală și un vaccin.De la începutul anului 2020, comunitatea medicală internațională își îndreaptă atenția asupra unui agent patogen emergent – o nouă tulpină de coronavirus, denumită de Organizația Mondială a Sănătății (OMS) Severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2 – datorită faptului că este un virus înrudit cu SARS, agentul cauzal al epidemiei din 2003). Infecția cu acest virus conduce la afectarea respiratorie, care poate evolua cu pneumonie sau afectarea întregului organism (boala fiind denumită, pe scurt, COVID-19). Virusul a apărut pentru prima oară în orașul Wuhan, provincia Hubei din China și s-a răspândit la nivel național și, într-o măsură mai mică, la nivel global.
Sursa foto: CDC
Conform Organizației Mondiale a Sănătății, tratamentul COVID-19 trebuie să țintească în mod prioritar dispariția rapidă a simptomatologiei, limitarea transmisiei interumane și ameliorarea formelor severe, cu risc de deces.
Interacțiunea coronavirus- organism uman. Cum are loc infecția?
Pentru a dezvolta tratamente care inhibă în mod țintit interacțiunea dintre virus și celulele corpului uman este important să înțelegem mai exact mecanismele infecției. Datorită secvențierii rapide a SARS-CoV-2, a cunoștințelor acumulate în domeniul coronaviridae (care infectează frecvent animale și includ cunoscutele virusuri SARS și MERS) și existenței de antivirale pentru alte infecții, dezvoltarea de medicamente contra SARS-CoV-2 este deja într-o fază avansată, mai mult de 80 de studii clinice fiind în desfășurare.
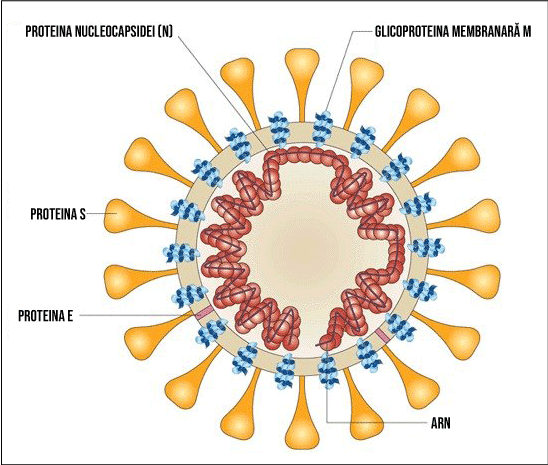
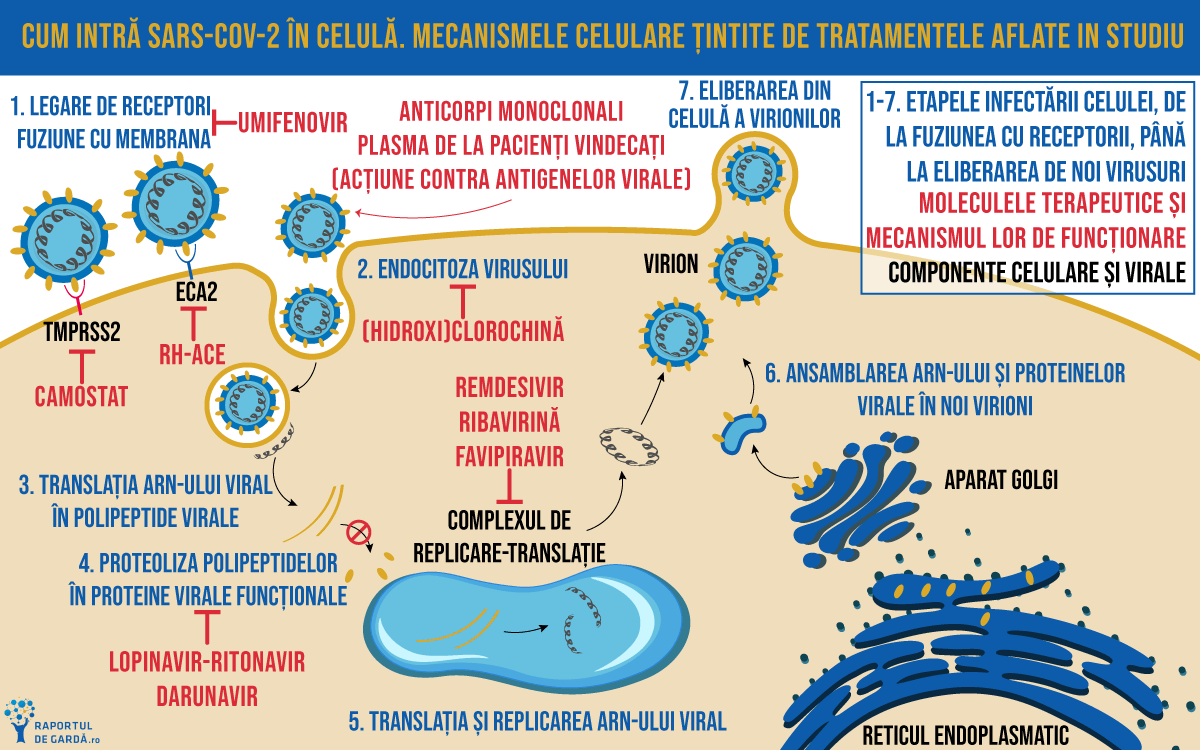
SARS-CoV-2 este un β-coronavirus cu anvelopă și informația genetică sub forma ARN. Proteinele non-structurale ale SARS-CoV-2 sunt polimeraza ARN, helicaza și proteazele similare 3-chemotripsinei și papainei, și ar putea constitui ținte terapeutice pentru antiviralele studiate. În jurul moleculei de ARN se află proteinele structurale virale, dintre care cea mai importantă este proteina S, care are funcția de legare de enzima de conversie a angiotensinogenului II (ECA2), cu rol de receptor în cazul virusurilor SARS-CoV-2 și SARS. În plus, proteina S este modificată de către TMPRSS2 (proteinaza transmembranară-serină 2), modificare care facilitează intrarea particulelor virale în celulă.
Descoperirea unui tratament eficient contra SAR-CoV-2 poate urma uneia dintre următoarele strategii:
- Inhibarea enzimelor sau proteinelor funcționale, esențiale în supraviețuirea virusului;
- Inhibarea proteinelor structurale virale, împiedicând interacțiunea cu celulele umane sau formarea de virioni;
- Stimularea imunității gazdei umane;
- Inhibarea proteinelor umane care acționează drept receptori pentru virus.
Tratamente posibile contra infecției coronavirus SARS-CoV-2
Există mai multe molecule care ar putea fi eficiente împotriva coronavirusului SARS-CoV-2, în testele pe culturi celulare, animale și teste incipiente la oameni. În baza de date oficială Chinese Clinical Trial Registry sunt înregistrate peste 150 de studii clinice asupra COVID-19, cele mai multe în faze inițiale 0-1 (pentru a evalua efectele a noi molecule) și în faza III (molecule cu efecte observate preclinic care pot fi deja testate în COVID-19).
Conform documentului OMS care vizează moleculele prioritate în studierea COVID-19, candidatul cel mai promițător este remdesivir, care a fost descris și de către Bruce Aylward, directorul general adjunct al OMS, drept tratamentul experimental cu cele mai mari șanse de reușită. Remdesivir este un analog nucleotidic, care acționează împotriva SARS-CoV-2 prin inhibarea ARN-polimerazei ARN-dependente și are următoarele avantaje:
- Spectru larg antiviral;
- Eficiență împotriva coronavirusurilor, atât în studiile in vitro, cât și in vivo;
- Profilul de siguranță demonstrat în studiile asupra virusului Ebola;
- Eficiență superioară combinației Lopinavir / Ritonavir / IFNbeta în studiile pe modele animale.
Pe 26 februarie au fost demarate două studii de faza III, în cadrul cărora remdesivir va fi administrat la 1.000 de pacienți: 400 de pacienți cu COVID19 forma severă vor primi timp de 5 sau 10 zile remdesivir, iar 600 de pacienți cu forme moderate vor primi tratamentul antiviral timp de 5 zile, timp de 10 zile, sau vor primi placebo. Obiectivul urmărit de studii este menținerea stării clinice normale, a unei temperaturi corporale (36,6 grade Celsius) și a unei saturații în oxigen normale (peste 94%), împreună cu proporția de pacienți externați după 14 zile de spitalizare. În studiile preclinice a demonstrat eficiență contra virusurilor Ebola, Marburg, MERS și SARS, iar fazele 1 și 2 au inclus pacienți infectați cu virusul Ebola. Studiile de fază 3 se va desfășura atât în spitale din China, cât și în Statele Unite.
În plus, Institutul Național de Sănătate din SUA (NIH) a demarat un studiu independent, dublu-orb, controlat cu placebo, de fază II, care urmărește efectele remdesivir într-o cohortă de 394 de pacienți cu forme severe COVID-19 asupra stării clinice, duratei de spitalizare, variabilelor biologice și proporției de decese.

Combinația inhibitorilor de protează lopinavir/ritonavir (comercializată sub denumirea Kaletra, pentru tratamentul infecției HIV), cu sau fără IFNβ, este un alt candidat viabil în lupta contra SARS-CoV-2. Este deja inclusă în studiul MIRACLE, contra virusului MERS, iar primul studiu în China contra SARS-CoV-2 a fost demarat. În plus, o echipă de experți din Wuhan (orașul în care a apărut infecția) a realizat un ghid de bune practici, în urma gestionării unui număr ridicat de pacienți. În afară de tratamentul suportiv, ghidul include utilizarea lopinavir+ritonavir+IFN, care este susținut, însă, de un nivel scăzut de certitudine științifică (recomandarea se bazează pe utilizarea în infecțiile SARS și MERS, înrudite, dar nu identice, cu SARS-CoV-2).
Lopinavir/ritonavir acționează prin inhibiția proteazei similare 3-chemotripsinei, din structura SARS, MERS și SARS-Cov-2. Studiile observaționale (în SARS-CoV-2 și SARS) susțin inițierea terapiei în primele 7-10 zile, altfel beneficiile clinice nu sunt regăsite la pacienți. În afară de combinația cu IFN, cei doi inhibitori de protează sunt administrați în cadrul studiilor și alături de ribavirină (analog de guanozină și inhibitor al sintezei ARN, care în cadrul COVID-19 ar putea inhiba proteinaza similară papainei), emtricitabină/tenofovir (alte terapii aprobate contra HIV, care inhibă enzima revers transcriptază) sau alături de umifenovir (inhibitor al fuziunii virale de membranele celulare umane, care inhibă interacțiunea dintre proteina S și receptorul ECA2).
În cazul umifenovir (un antiviral activ contra gripei, aprobat doar în China și Rusia), utilizarea sa în COVID-19 este promițătoare, conform studiilor din China, care sunt în desfășurare: acesta ar putea conduce la o rată de mortalitate mai mică. Un studiu randomizat a comparat umifenovir cu un alt antiviral promițător, favipiravir, iar acesta din urmă a condus la o rată de vindecare mai mare, după 7 zile de tratament, în cazurile moderate de COVID-19 (71,4% în grupul favipiravir, față de 55,9% în grupul umifenovir).
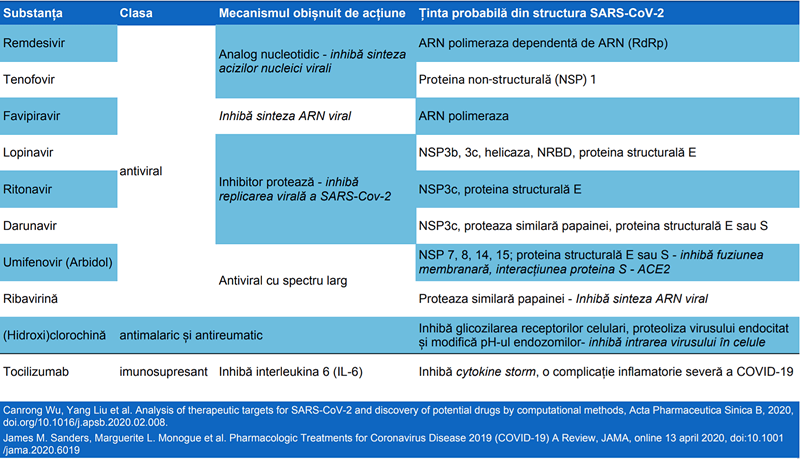
Alte opțiuni terapeutice, cu șanse mai mici de reușită – conform OMS – sunt anticorpii monoclonali sau policlonali, sau serul recoltat de la pacienții cu COVID-19, care conține anticorpi împotriva infecției. Cu toate acestea, a fost demarat un studiu care implică plasmă recoltată de la pacienții vindecați în urma COVID-19 și administrarea acesteia în cazurile severe de afectare pulmonară – situație în care au fost descrise câteva cazuri de remisiune clinică.
OMS a identificat și o serie de molecule a căror studiere este descurajată – ribavirina și imunosupresoarele, precum corticoizii (care ar putea fi totuși utili în afectarea pulmonară severă și ARDS), iar în cazul clorochinei nu există suficiente dovezi care să justifice studiile. Cu toate acestea, studii care includ aceste medicamente au fost demarate, pe baza dovezilor preclinice de acțiune contra virusului SARS-CoV-2. Ribavirina acționează prin inhibarea ARN-polimerazei ARN-dependentă, însă în cazul SARS și MERS nu a adus niciun beneficiu clinic.
Nu în ultimul rând, o serie de tratamente nonspecifice pot aduce îmbunătățiri clinice, precum statinele, heparina și vitamina C.
În afara moleculelor descrise de OMS, studiile preclinice sugerează și alte posibile tratamente contra SARS-CoV-2. Celulele stem mezenchimale sunt subiectul câtorva studii de faza I și II, derulate în cadrul infecției SARS-CoV-2. Ipoteza terapeutică este aceea că proprietățile imunomodulatoare și regenerative ale celulelor stem pot inhiba componenta inflamatorie a afectării pulmonare COVID-19 (care poate conduce la evoluția fatală a bolii).
Enzima de conversie a angiotensinei (ECA2) este o altă țintă terapeutică posibilă, datorită rolului de ligand viral. ECA2 este frecvent întâlnit la nivelul celulelor epiteliului și parenchimului pulmonar, fiind astfel o țintă accesibilă pentru coronavirus, care se transmite pe cale respiratorie. În acest sens, au fost identificate mai multe molecule care ar putea inhiba ECA2, dintre care ruxolitinib este inclus într-un studiu clinic, împreună cu celule stem mezenchimale.
O altă modalitate de a acționa asupra receptorului viral este cu ajutorul ECA2 recombinat uman (rhACE2), o moleculă studiată în cadrul sindromului de detresă respiratorie acută (ARDS), datorită nivelului pulmonar ridicat de ECA2. Studiul în cadrul COVID-19, demarat de compania Apeiron, urmărește efectele rhACE2 la pacienții cu COVID-19, care ar putea fi benefice atât prin scăderea viremiei (datorită legării limitate de receptorul ECA2) cât și prin protecția plămânului de ARDS, care este una dintre complicațiile COVID-19 cu consecințe adesea fatale.
Această strategie terapeutică, de a inhiba receptorii umani ai virusului, poate fi eficientă și împotriva celei de-a doua proteine cu rol în pătrunderea virusului în celule – proteinaza transmembranară TMPRSS2. Molecula camostat, aprobată în Japonia pentru afecțiunile pancreatice (care au, de asemenea, proteinaze drept elemente patogenice), a demonstrat efecte de inhibiție a TMPRSS2 în studiile pe culturi celulare și, implicit, de inhibiție a infecției virale.
Elemente din medicina tradițională chineză, precum preparatele vegetale sau acupunctura, sunt incluse în ghidul de bune practici realizat în Wuhan și constituie subiectul a mai multe studii clinice demarate în COVID-19.
De la culturi celulare, la pacient – mecanismul de studiere și aprobare a unei substanțe
Procesul de cercetare a unei noi molecule terapeutice este standardizat și deosebit de riguros, astfel încât, în momentul administrării la pacienți, medicii au toate informațiile asupra eficacității și siguranței. În medie, medicamentul parcurge „călătoria” dintre laborator și rafturile farmaciei în 10 ani, dintre care 6-7 ani sunt ocupați de studierea clinică efectivă. Fiecare medicament are costuri medii de 2,6 miliarde de dolari, ceea ce include numeroasele molecule dezvoltate care nu au trecut de etapa preclinică de cercetare. Din momentul demarării studiului clinic, pe pacienți, un medicament are o probabilitate de 12% de a fi aprobat.
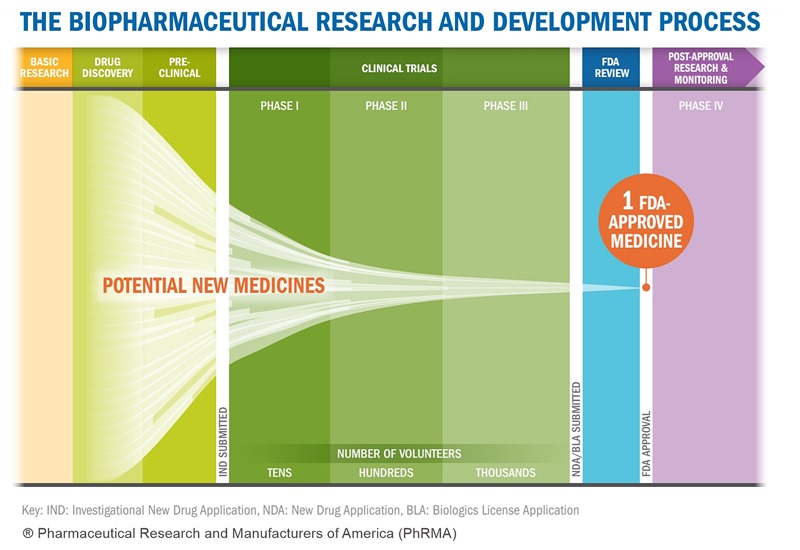
Sursa foto PhRMA
- Înțelegerea în detaliu a bolii și a potențialelor ținte terapeutice;
- Identificarea unei molecule care are potențialul de a interacționa în mod benefic cu ținta anterior descoperită;
- Cercetarea farmacodinamicii și farmacocineticii produsului, pe culturi celulare, modele animale (in vivo) și simulări digitale (in silico);
- Modificarea structurală a compusului, pentru a optimiza siguranța și eficacitatea;
- Dezvoltarea procesului de fabricație pe scară mai largă a moleculei.
- Faza I – înțelegerea mai exactă a profilului de siguranță, într-o cohortă de voluntari sănătoși;
- Faza II – evaluarea siguranței și eficacității, într-o cohortă de pacienți (prin compararea cu placebo sau terapia standard în acea boală) și identificarea dozelor optime;
- Faza III – evaluarea siguranței și eficacității, într-o cohortă mult mai mare de pacienți
- Aprobarea și fabricarea pe scară largă a substanței;
- Faza IV, sau studiile post-marketing – monitorizarea profilului de siguranță și identificarea de noi indicații a medicamentului (beneficii care nu au fost observate în studiile anterioare, combinații terapeutice, indicații în alte boli).
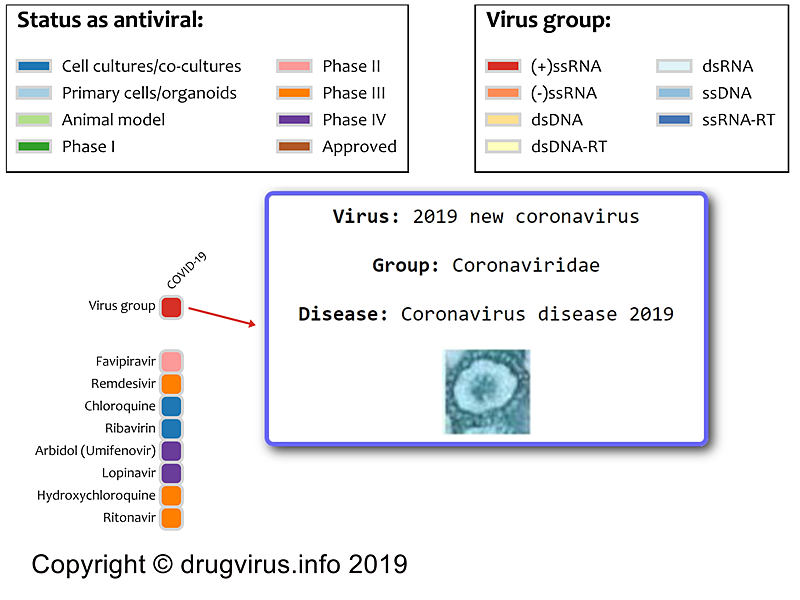
În cazul SARS-CoV-2 se utilizează o strategie care are avantajul de a conferi viteză procesului de cercetare – redirecționarea medicamentelor pentru alte boli decât cele pentru care au fost dezvoltate, studiate și aprobate inițial. În acest fel primele etape ale cercetării – sinteza chimică și procesul de fabricație, etapele preclinice pe culturi celulare și modele animale și etapele clinice precoce (fazele I și IIa) – sunt deja realizate, iar medicamentul poate fi direct administrat în cadrul studiilor de fază III – în boala-țintă, pentru a evalua eficacitatea. În acest fel, pot fi chiar utilizate molecule care nu au avut succes în cadrul altor boli (cum este cazul remdesivir în infecția cu virus Ebola).
Aprobarea de urgență
Pe lângă studierea moleculelor terapeutice în această infecție emergentă, o etapă importantă în gestionarea COVID-19 este aprobarea posibilelor tratamente. În acest sens, agențiile responsabile pentru evaluarea și aprobarea medicamentelor din SUA și UE – FDA și EMA – au adoptat măsuri prin care să încurajeze un proces rapid, dar eficient, în cazul coronavirusului SARS-CoV-2, situație care ar putea avea un impact benefic asupra evoluției epidemiei.
Administrația Alimentelor și Medicamentelor SUA (FDA) a aprobat pe 25 februarie primul studiul clinic asupra COVID-19 din SUA (cu antiviralul remdesivir), în urma unei evaluări mult mai rapide decât data stabilită de 30 de zile. FDA încurajează și cercetătorii altor molecule cu potențial anticoronavirus să apeleze la Programul de Consultări al Departamentului de Boli Infecțioase a FDA, anterior depunerii aplicației de studiu clinic (OID preIND Consultation Program).
Sursa foto: Deloitte
Agenția Europeană a Medicamentului (EMA) a demarat planul de gestionare a situațiilor de urgență în domeniul sănătății și, de asemenea, încurajează dezvoltatorii de potențiale terapii să discute cu reprezentanții EMA strategia de studiere a terapiei. În acest sens, există o serie de mecanisme de aprobare accelerată:
- Consultanță științifică – pentru identificarea metodelor de cercetare care conduc la cele mai mari șanse de reușită a studiului;
- Proiectul PRIME – care conferă prioritatea medicamentelor care se adresează unor boli fără alte opțiuni terapeutice, sau net inferioare celor studiate;
- Evaluarea accelerată a cererii de punere pe piață – în cazul terapiilor de interes public major, precum cele dedicate COVID-19;
- Autorizația condițională de punere pe piață – în cazul în care accesul imediat la medicament aduce beneficii mai importante decât acumularea de date pe termen lung asupra acestuia, situație care include și infecțiile emergente, care conduc la o stare de urgență, precum COVID-19.
Dezvoltarea de medicamente, împreună cu dezvoltarea de vaccinuri și cercetarea epidemiologică a infecției virale, reprezintă un element esențial în înțelegerea și controlul COVID-19. Rezultate interimare a studiilor clinice vor fi publicate în următoarele săptămâni, iar pacienții vor putea beneficia de rezultate finale și aprobări în următoarele luni, cu sprijinul autorităților în domeniu.

De asemenea, este important de menționat că Organizația Mondială a Sănătății a avertizat încă din 2018 asupra riscului apariției unei pandemii cu un patogen necunoscut la acel moment, prin introducerea pe lista de priorități, a Bolii X – un îndemn către cercetare și dezvoltare nu doar în aria medicală, ci și între diversele domenii care au rol în menținerea siguranței sănătății, o metodă în plus de prevenție pentru cazurile neașteptate de boli.
Pentru informațiile corecte și verificate, accesați stirioficiale.ro, primul website lansat de Code for Romania Task Force, în parteneriat cu Guvernul României prin Autoritatea pentru Digitalizarea României și Departamentul pentru Situații de Urgență.
Citește și:
- INFOGRAFIC. Care sunt măsurile recomandate de ECDC pentru controlul infecției determinate de coronavirusul Wuhan?
- UPDATE 24 februarie. Centrul European de Prevenire și Control al Bolilor declară risc scăzut spre moderat de transmitere a coronavirusului SARS-CoV-2 în Europa
- Coronavirusul SARS-CoV-2: Care este profilul persoanelor aflate la risc înalt de a dezvolta forme severe COVID19?

