FDA a aprobat tratamentul adjuvant cu atezolizumab pentru pacienții cu cancer pulmonar non-microcelular, în stadiile II-IIIA
Atezolizumab este prima imunoterapie aprobată de FDA (Food and Drug Administration) pentru tratamentul adjuvant al cancerului pulmonar non-microcelular (NSCLC), la pacienții cu stadiile II-IIIA și expresie PD-L1 ≥1%.
Rezultatele studiului IMpower010 demonstrează creșterea supraviețuirii fără semne de boală (disease free survival- DFS) și scăderea riscului de recurență la pacienții cu NSCLC în stadii mai puțin avansate și reprezintă un argument important pentru testarea precoce a biomarkerilor la persoanele la risc înalt. FDA a aprobat și testul Ventana PD-L1 (SP263) pentru selectarea pacienților eligibili pentru acest tratament.
În ultimii 10 ani, opțiunile terapeutice pentru stadiile NSCLC în stadii incpiente nu s-au schimbat semnificativ. Pacienții cu NSCLC rezecat primesc chimioterapie pe bază de platină, care determină o reducere modestă a riscului de recurență. Până la această imunoterapie, doar osimertinib, o terapie țintită, a primit aprobare pentru tratamentul adjuvant al NSCLC, în cazurile în care este prezentă mutația EGFR.
Atezolizumab este un anticorp monoclonal care se leagă de proteina PD-L1, exprimată pe celulele tumorale și pe celulele imune care pătrund în tumoră, blocând interacțiunile sale cu receptorii PD-1 și B7. Inhibarea PD-L1 determinară activarea limfocitelor T și induce un răspuns anti-tumoral.
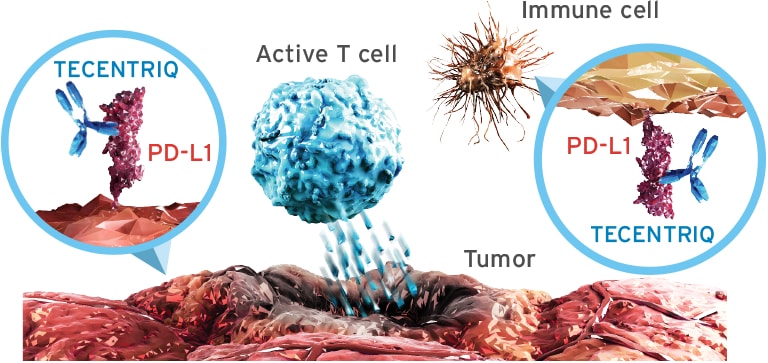
Sursa foto: Tecentriq.com
Aprobarea imunoterapiei atezolizumab pentru această indicație se bazează pe o analiză interimară a studiului de fază III IMpower010. 1.005 pacienți care au urmat intervenția chirurgicală pentru rezecarea tumorii și chimioterapie au fost randomizați pentru a primi atezolizumab la 3 săptămâni, 16 cicluri sau tratamentul standard. Obiectivul primar al studiului a fost supraviețuirea fără semne de boală (DFS) care a fost evaluat printr-o analiză asupra unui grup de 476 de pacienți cu stadiile II-IIIA de NSCLC, cu expresie PD-L1 ≥1%.
Rezultatele analizei interimare a studiului au fost prezentate în iunie 2021, la Întâlnirea Anuală a Societății Americane de Oncologie Clinică (ASCO).
- DFS mediană nu a fost atinsă în grupul care a primit atezolizumab și a fost de 35.5 luni în grupul care a primit standardul terapeutic (best supportive care);
- Datele de supraviețuire generală (overall survival – OS) nu erau disponibile la momentul analizei însă se observă o tendință de creștere a supraviețuirii în subgrupurile de pacienți la care se înregistrează o expresie PD-L1 crescută;
- Beneficiile clinice sunt importante mai ales la pacienții la care se înregistrează expresia PD-L la nivelul a cel puțin 50% din celulele tumorale;
- Nu s-au observat evenimente adverse noi, față de alte indicații ale imunoterapiei;
- Tratamentul cu atezolizumab la pacienții care au urmat excizia chirurgicală și chimioterapie pe bază de platină a determinat și o reducere a riscului de recurență a bolii cu 34%, comparativ cu tratamentul standard.
Aceasta este a 6-a indicație aprobată de FDA pentru atezolizumab în cancerul pulmonar. Atezolizumab este prima imunoterapie aprobată pentru tratamentul de linia I în cancerul pulmonar microcelular, în combinație cu chimioterapie. În 2020, atezolizumab a primit aprobare din partea FDA pentru tratamentul pacienților diagnosticați cu NSCLC metastatic, în cazul tumorilor care prezintă o expresie ridicată a PD-L1. În mai 2021, Agenția Europeană a Medicamentului a aprobat imunoterapia în linia I de tratament pentru NSCLC metastatic, pe baza studiului de fază III IMpower110.
Fiecare nou tratament aprobat pentru cancerul pulmonar necesită testarea biomarkerilor
Cancerul pulmonar non-microcelular a devenit un exemplu al succesului medicinei de precizie în managementul cancerelor solide. Prin punerea în evidență a biomarkerilor, se realizează un diagnostic de precizie al cancerului, care poate sta la baza administrării tratamentului potrivit pentru pacientul potrivit, la momentul potrivit, și încă de la început.
Centrul pentru Inovație în Medicină a publicat recent Carta Albă a biomarkerilor în cancerul pulmonar non-microcelular, un document care descrie evoluția testării moleculare în cancerul pulmonar non-microcelular (NSCLC). Pe măsură ce terapiile oncologice avansează și devin din ce în ce mai precise, și tehnicile de testare utilizate trebuie adaptate și adoptate de către fiecare sistem medical.
Un raport publicat la începutul anului demonstra că deși în România au intrat pe piață și au fost rambursate tot mai multe terapii inovatoare, lipsa accesului la diagnosticul de precizie a făcut ca această disponibilitate a terapiilor să nu se reflecte în supraviețuirea pacienților.
Citește și:
- #ASCO21. Adăugarea atezolizumab la chimioterapia adjuvantă crește supraviețuirea fără progresia bolii în stadiile incipiente ale cancerului pulmonar non-microcelular
- FDA aprobă atezolizumab ca primă linie de tratament în cancerul pulmonar non-microcelular metastazat cu expresie PD-L1 ridicată

