FDA aprobă pembrolizumab în prima linie de tratament pentru cancerul de cap și gât avansat
Pembrolizumab a fost aprobat de către FDA în tratamentul de primă line a cancerului scuamos de cap și gât, metastatic sau nonrezecabil. Acesta era deja aprobat în tratamentul de linie a doua. Extinderea indicația s-a făcut pe baza rezultatelor studiului de fază 3 KEYNOTE-048, prezentate recent în cadrul întâlnirii anuale a Societății Americane de Oncologie Clinică – ASCO 2019.
„Această aprobare este un moment de hotar în tratamentul cancerului de cap și cât. Prin oferirea de noi opțiuni terapeutice are potențialul de a transforma felul în care tratăm pacienții cu această boală debilitantă”- Dr. Barbara Burtness, cercetător principal al studiului KEYNOTE-048, Prof. Yale School of Medicine.
Pembrolizumab poate fi folosit ca tratament de primă linie fie ca monoterapie la pacienții cu cancer scuamos de cap și gât, cu expresie PD-L1, fie în combinație cu chimioterapice pe bază de platină și 5-fluoro-uracil (5-FU), la toți pacienții cu acest tip de cancer, indiferent de expresia PD-L1.
Față de regimul EXTREME (cetuximab+chimioterapie pe bază de platină+5-FU), standardul de îngrijire în această condiție, ambele regimuri terapeutice au crescut supraviețuirea globală:
-
pentru toată populația de pacienți, supraviețuirea globală mediană a celor tratați cu pembrolizumab+chimioterapie a fost de 13 luni, față de 10,7 luni în cadrul EXTREME;
-
pentru populația de pacienți cu expresie tumorală de PD-L1 (scor combinat pozitiv PDL-1 >1%), reprezentând 44% din întreaga populație de pacienți, supraviețuirea mediană a pembrolizumab+chimioterapie a fost de 12,3 luni, față de 10,3 luni în cadrul EXTREME;
-
pembrolizumab în monoterapie nu a fost superior chimioterapiei în monoterapie;
-
nu a fost înregistrată o îmbunătățire a perioadei fără progresie a bolii față de regimul EXTREME, nici prin monoterapie cu pembrolizumab nici prin combinație pembrolizumab+chimioterapie.
Reacțiile adverse întălnite la >20% din pacienții cu monoterapie pembrolizumab au fost oboseala, constipația și rashul. Reacțiile adverse întălnite la >20% din pacienții cu pembrolizumab+chimioterapie au fost greața, oboseala, constipația, vărsături, inflamații ale mucoaselor, diaree, scăderea apetitului, stomatită și tuse.
Pentru diagnosticul pacienților cu scor combinat pozitiv PDL-1 >1% se poate utiliza kitul PD-L1 IHC 22C3 pharmDx. FDA a extins indicația acestuia pentru a include folosirea acestui ca dispozitiv de diagnostic pentru selectarea pacienților cu cancer scuamos de cap și gât pentru monoterapie pembrolizumab.
Despre pembrolizumab
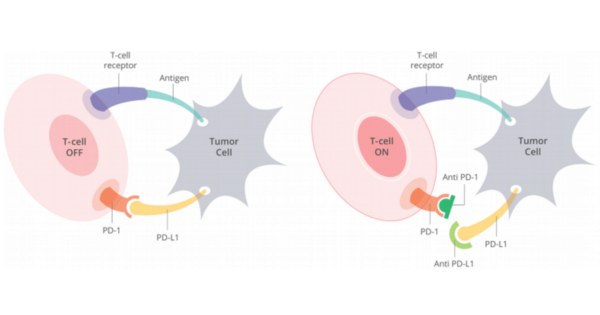
Pembrolizumab este un anticorp monoclonal ce blochează interacțiunea PD-L1 cu PD-1 și CD80. Fiziologic, interacțiunea dintre PD-L1 și PD-1 are rolul de a inhiba limfocitele T, menținând activitatea sistemului imun în limite normale, prevenind distrugeri tisulare sau fenomene autoimune. Unele tipuri de cancer se folosesc de această cale, pentru a inhiba răspunsul imun. Inhibitorii PD-L1 și PD-1 împiedică acest mecanism adaptativ al celulelor maligne.
- #ASCO19. Imunoterapia de primă linie cu pembrolizumab, alternativă promițătoare la chimioterapie pentru formele avansate de cancer gastric
- Pembrolizumab, disponibil în România, în regim compensat, pentru pacienții cu cancer pulmonar metastatic și melanom
- #ILC2019. Nivolumab și pembrolizumab, eficiente și sigure pentru tratamentul carcinomului hepatocelular, conform studiilor din viața reală

