Contribuție românească. Studiul CheckMate -9LA: nivolumab + ipilimumab combinate cu chimioterapie, cresc supraviețuirea în prima linie de tratament a cancerului pulmonar non-microcelular metastazat, indiferent de expresia PD-L1
Rezultatele studiului CheckMate -9LA demonstrează beneficiul combinării a două imunoterapii cu chimioterapia limitată pentru pacienții cu cancer pulmonar non-microcelular (NSCLC), indiferent de statusul PD-L1. La realizarea acestuia au contribuit și experți români în oncologie: Prof. Dr. Tudor-Eliade Ciuleanu, de la Institutul Oncologic Prof. Dr. Ion Chiricuta din Cluj Napoca, Conf. Dr. Michael Schenker, de la Centrul Oncologic „Sf. Nectarie” din Craiova și Dr. Aurelia Alexandru de la Institutul Oncologic București.
Pe 26 mai FDA a aprobat această combinație terapeutică și rezultatele studiului CheckMate -9LA au fost prezentate în cadrul Întâlnirii Anuale a Societății Americane de Oncologie Clinică 2020 (ASCO).
Dubla imunoterapie Opdivo (nivolumab) plus Yervoy (ipilimumab) administrată împreună cu două cicluri de chimioterapie dublă cu săruri de platină, a primit aprobare în SUA din partea FDA (Food and Drug Administration) pentru tratamentul de primă linie al pacienților adulți cu NSCLC metastazat sau recurent, fără aberații tumorale EGFR sau ALK. Terapia este aprobată pentru pacienții cu boală scuamoasă sau non-scuamoasă și indiferent de expresia PD-L1.
Această aprobare marchează a șasea indicație pentru combinațiile pe bază de Opdivo + Yervoy, în cinci tipuri de cancere. Două combinații pe bază de Opdivo + Yervoy sunt acum aprobate în tratamentul de primă linie al cancerului pulmonar.
Aprobarea pentru Opdivo + Yervoy și chimioterapie limitată se bazează pe analiza intermediară din studiul de fază III CheckMate -9LA, în care combinația celor două imunoterapii cu două cicluri de chimioterapie dublă cu săruri de platină a demonstrat rezultate superioare privind supraviețuirea globală, supraviețuirea fără progresia bolii și rata globală de răspuns față de chimioterapia simplă, indiferent de expresia PD-L1 sau histologia tumorală.
„Am parcurs un drum lung în înțelegerea rolului abordărilor duble bazate pe imunoterapie în cancer și posibilul impact asupra rezultatelor pe termen lung ale pacienților”, a declarat Prof. Dr. David P. Carbone, autor principal al studiului CheckMate-9LA, director al James Thoracic Oncology Center la Ohio State University. „Odată cu aprobarea aceasta, mai mulți pacienți au acum acces la o opțiune bazată pe Opdivo + Yervoy și o șansă la o viață mai lungă.”
Studiul clinic CheckMate -9LA
CheckMate -9LA este un studiu multicentric, randomizat, de fază III, care evaluează Opdivo (360 mg) + Yervoy (1 mg/kg) combinat cu două cicluri de chimioterapie dublă cu săruri de platină comparativ cu chimioterapia dublă, bazată pe sărurile de platină (patru cicluri, urmate de terapie opțională de menținere cu pemetrexed în cazul NSCLC non-scuamos). Tratamentul a fost evaluat ca primă linie la pacienții cu NSCLC metastazat sau recurent, indiferent de expresia PD-L1 și histologia tumorală.
Pacienții au fost stratificați în funcție de expresia PD-L1 (<1% vs ≥ 1%), sex și histologia tumorii (scuamoase vs. non-scuamoase). Pacienții înrolați în studiu au fost împărțiți în două grupuri de aproximativ 350 de pacienți, care au primit cele două regimuri terapeutice.
Obiectivul principal al studiului a fost supraviețuirea globală (OS). Obiectivele suplimentare privind eficacitatea au inclus supraviețuirea fără progresia bolii (PFS), rata globală de răspuns (ORR) și durata răspunsului.
La o analiză intermediară după o urmărire medie de 8,1 luni, Opdivo plus Yervoy combinate cu două cicluri de chimioterapie au redus riscul de deces cu 31%, comparativ cu chimioterapia singură. În plus, după o monitorizare mai lungă (minimum 12,7 luni), combinația a continuat să arate îmbunătățiri ale supraviețuirii globale comparatuv cu chimioterapia (supraviețuire globală medie de 15,6 luni față de 10,9 luni); Opdivo plus Yervoy și chimioterapia limitată au îmbunătățit supraviețuirea, indiferent de nivelurile de expresie PD-L1, reducând riscul de deces cu 38% la pacienții cu PD-L1 <1% și cu 36% la pacienții cu PD-L1 ≥1%.
Combinația de imunoterapie dublă și chimioterapie a demonstrat o rată de supraviețuire fără progresia bolii la un an de 33% față de 18% pentru chimioterapie.
La un an, 63% dintre pacienți tratați cu Opdivo + Yervoy + chimioterapie limitată erau în viață, comparativ cu 47% dintre cei tratați cu chimioterapie.
Rata globală de răspuns (ORR) a fost de 38% pentru pacienții tratați cu Opdivo + Yervoy cu chimioterapie limitată și 25% pentru pacienții tratați cu chimioterapie.
Cele mai frecvente reacții adverse au fost fatigabilitate, dureri musculo-scheletale, diaree, scăderea apetitului, erupții cutanate. Reacțiile adverse grave au apărut la 57% dintre pacienți. Nivolumab plus ipilimumab în combinație cu chimioterapia dublă cu săruri de platină au fost întrerupte din cauza evenimentelor adverse la 24% dintre pacienți. Cele mai frecvente reacții adverse grave au fost pneumonia și insuficiența respiratorie, neutropenia febrilă, anemia, leziunile renale acute. În plus, evenimentele adverse fatale au apărut la 7 (2%) pacienți.
Imunoterapia dublă cu nivolumab și ipilimumab – 6 indicații în 5 forme de cancer
Nivolumab este un anticorp monoclonal care inhibă PD-1. Acesta funcționează ca un inhibitor de punct de control (checkpoint inhibitor) al reacției imune: limfocitele T nu mai sunt inhibate de receptorul PD-1 de pe suprafața lor, astfel pot ataca mai eficient celulele tumorale.
Ipilimumab este un anticorp monoclonal, care acționează de asemenea prin blocarea punctelor de control. Acesta inhibă proteina CTLA-4 de pe suprafața limfocitului T, astfel acesta este mai eficient în atacarea celulelor tumorale.
Opdivo + Yervoy este o combinație unică de doi inhibitori ai punctelor de control cu un mecanism de acțiune potențial sinergic, care vizează două puncte de control diferite (PD-1 și CTLA-4) pentru a ajuta la distrugerea celulelor tumorale, astfel:
- nivolumab ajută la activarea și proliferarea celulelor T;
- ipilimumab ajută celulele T existente să descopere tumora.
Unele dintre celulele T stimulate de ipilimumab pot deveni celule T de memorie, ceea ce poate permite un răspuns imun pe termen lung. Poate de asemenea să apară țintirea celulelor normale și să conducă la reacții adverse mediate imun, care pot fi severe și potențial fatale.
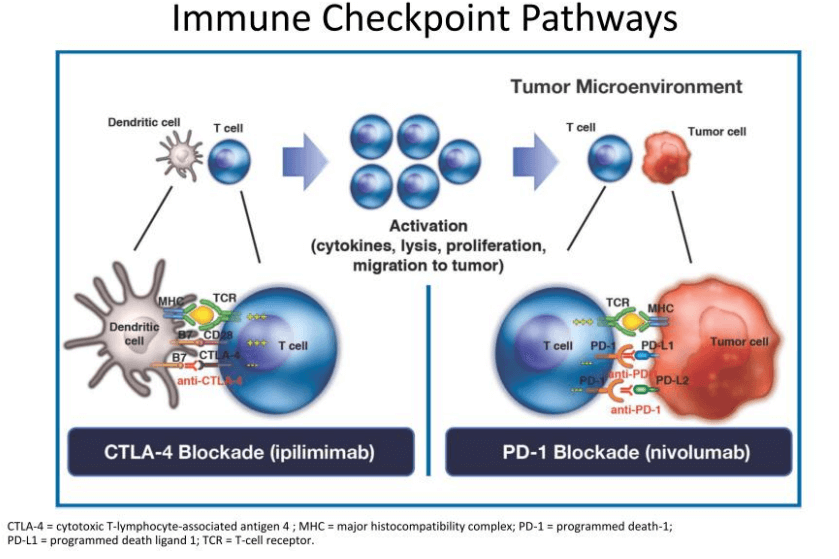
Mecanismul de acțiune al nivolumab și ipilimumab. Sursa foto: Eva Muñoz Couselo, MD, PhD, Hospital Vall d’Hebrón Barcelona, ABordaje Multidisciplinar del Cancer XI
Cancerul pulmonar este principala cauză de deces prin cancer. Cele două tipuri principale de cancer pulmonar sunt cel cu celulele mici (microcelular – SCLC) și cel non-microcelular (NSCLC). NSCLC este unul dintre cele mai frecvente tipuri de cancer pulmonar și reprezintă aproximativ 84% din diagnostice. Cancerul pulmonar non-microcelular este o boală complexă care necesită multiple opțiuni de tratament pentru a răspunde nevoilor diferitelor populații de pacienți. Rata de supraviețuire variază în funcție de stadiul și tipul cancerului în momentul stabilirii diagnosticului.
Opdivo a dat startul unei noi ere și a schimbat modul în care este tratat NSCLC atunci când, în 2015, a devenit prima imunoterapie aprobată pentru utilizare la pacienții cu NSCLC tratat anterior.
Pe 15 mai, FDA a aprobat Opdivo + Yervoy ca tratament de primă linie pentru anumiți pacienți cu NSCLC metastazat ale căror tumori exprimă PD-L1 ≥1% (determinare făcută pe baza unui test aprobat de FDA).
Această a doua aprobare a unei combinații bazate pe Opdivo + Yervoy pentru tratamentul de primă linie a NSCLC avansat, oferă acum acces mai multor pacienți la o abordare de imunoterapie duală care poate fi administrată cu sau fără chimioterapie limitată, în funcție de pacient și de statutul PD-L1.
Lista completă de indicații FDA ale combinației terapeutice Opdivo (nivolumab)+ Yervoy (ipilimumab)
- Cancer pulmonar non-microcelular (NSCLC) metastazat, fără anomalii tumorale genomice EGFR sau ALK, indiferent de expresia PD-L1 – prima linie de tratament la pacienții adulți, în asociare cu chimioterapie limitată;
- Cancer pulmonar non-microcelular (NSCLC) ale cărui tumori exprimă PD-L1 ≥1%, fără anomalii tumorale genomice EGFR sau ALK – prima linie de tratament la pacienții adulți;
- Melanom metastatic sau nerezecabil;
- Carcinom renal avansat netratat în antecedente – la pacienții care prezintă risc scăzut sau intermediar;
- Cancer colorectal metastatic care a progresat în urma tratamentului cu fluoropirimidină, oxaliplatină sau irinotecan – la pacienții cu vârsta de peste 12 ani și cu instabilitate microsatelitară mare (MSI-H);
- Carcinom hepatocelular – la pacienți tratați în prealabil cu sorafenib.
Pentru ultimele doua indicații procesul de aprobare continuă, urmând ca beneficiile să fie confirmate de studiile clinice.

