FDA aprobă o nouă indicație pentru dabrafenib+trametinib: primul tratament tumor-agnostic pentru tumorile solide BRAF V600E pozitive
FDA (U.S. Food and Drug Administration) a aprobat în regim accelerat combinația dabrafenib + trametinib pentru tratamentul pacienților în vârstă de peste 6 ani cu tumori solide nerezecabile sau metastatice și mutație BRAF V600E, fără opțiuni alternative de tratament și care au progresat în urma tratamentului anterior. Acesta este primul și singurul tratament cu inhibitori BRAF/MEK aprobat pentru o indicație tumor-agnostic pentru tumorile solide care prezintă mutația BRAF V600E și este singurul inhibitor BRAF/MEK aprobat pentru utilizare la copii și adolescenți.
Combinația dabrafenib + trametinib a demonstrat o eficacitate semnificativă în mai multe tipuri de tumori BRAF pozitive, inclusiv la unii pacienți cu forme rare de cancer, care nu dispun de alte opțiuni de tratament. Astfel, testarea de rutină a prezenței mutației BRAF în cadrul algoritmului de diagnostic ar putea oferi o nouă opțiune de tratament pentru pacienții cu tumori solide.
Aprobarea FDA s-a bazat pe eficacitatea și siguranța clinică demonstrate în trei studii clinice. În studiul de fază II ROAR și în studiul NCI-MATCH (brațull H), combinația de tratament a dus la rate globale de răspuns de până la 80% la pacienții adulți cu tumori solide BRAF V600E pozitive. Un alt studiu, X2101, a demonstrat beneficiul clinic și profilul de siguranță acceptabil al dabrafenib + trametinib la copii și adolescenți.
Studiul multicentric, non-randomizat, ROAR, a inclus pacienți adulți cu anumite tipuri de tumori cu mutație BRAF V600E prezentă: gliom de grad înalt și scăzut, cancer de tract biliar, adenocarcinom intestinal, tumoră stromală gastrointestinală și cancer tiroidian anaplazic. Brațul H al studiului NCI-MATCH a înrolat de asemenea pacienți adulți cu tumori solide prezentau mutație BRAF V600E: tumori gastrointestinale, cancer pulmonar, tumori ginecologice sau peritoneale, tumori ale sistemului nervos central și ameloblastomul mandibulei, dar a exclus pacienții cu melanom, cancer tiroidian sau cancer colorectal. Dintre cei 131 de pacienți înrolați în ambele studii, vârsta medie la momentul inițial a fost de 51 de ani iar 90% primiseră terapie sistemică anterioară.
Rezultatele suplimentare ale acestor două studii au arătat:
- Rata de răspuns obiectiv obținut în urma tratamentului combinat la cei cu cancer de tract biliar a fost de 46%, cu o durată medie a răspunsului de 9,8 luni.
- În cazul pacienților cu gliom de grad înalt, rata de răspuns obiectiv a fost de 33%, cu o durată medie a răspunsului de 13,6 luni.
- La pacienții cu gliom de grad scăzut, rata de răspuns obiectiv a fost de 50%, cu o durată de răspuns variind între 6 luni și 29 de luni.
- Dabrafenib + trametinib a dus la rate de răspuns obiectiv de 80% și 50% la pacienții cu carcinom ovarian seros de grad scăzut și, respectiv, adenocarcinom intestinal; durata medie a răspunsurilor a variat între 12 – 42 de luni, respectiv, 7 – 8 luni.
Studiul multicentric, X2101, a inclus copii și adolescenți cu tumori solide refractare sau recurente. Eficacitatea asocierii dintre dabrafenib și trametinib a fost examinată la 48 de copii și adolescenți: gliom de grad scăzut (34), gliom de grad înalt (2). Majoritatea pacienților (83%) a beneficiat anterior de intervenție chirurgicală, 92% de terapie sistemică iar 2,8% de radioterapie adjuvantă. Combinația terapeutică a determinat o rată de răspuns obiectiv de 25%. Pentru cei 9 pacienți care au răspuns la tratament, durata răspunsului a fost de peste 6 luni pentru 78% dintre pacienți, respectiv peste 24 de luni pentru 44% dintre pacienți.
Profilul de siguranță al dabrafenib + trametinib observat în cadrul celor trei studii clinice a fost în concordanță cu profilul de siguranță cunoscut anterior.
Imunoterapia țintită în tratarea cancerelor cu mutații BRAF
Mutațiile BRAF V600 stimulează creșterea tumorală într-o gamă largă de tumori solide, inclusiv în tipurile rare de cancer care pot fi dificil de studiat în cadrul studiilor clinice de fază III și au adesea opțiuni limitate de tratament. BRAF V600E este cel mai frecvent tip de mutație BRAF, reprezentând până la 90% dintre cancerele cu mutație BRAF.
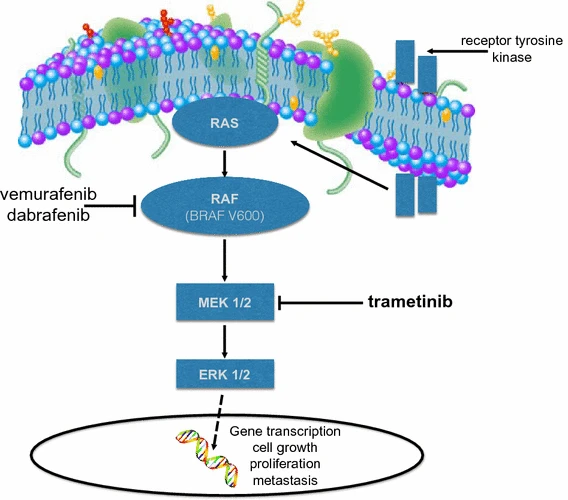
Combinația de terapii țintite dabrafenib + trametinib încetinește creșterea tumorală prin blocarea semnalelor asociate unor kinaze cu rol în proliferarea celulelor cancerigene. Trametinib este un inhibitor specific al MEK1 (kinaza 1 reglată prin semnal extracelular activat de mitogeni), al activării MEK 2 și al activității kinazice. Dabrafenib este un inhibitor al kinazelor RAF. În diferite tipuri de cancer, mutațiile oncogene ale BRAF determină activarea constitutivă a căilor RAS/RAF/MEK/ERK. Astfel, trametinib și dabrafenib inhibă două kinaze pe această cale, MEK și RAF iar asocierea asigură inhibarea concomitentă a căii.
Cele două terapii au fost studiate în rândul a peste 6.000 de pacienți BRAF pozitivi în peste 20 de studii aflate în curs sau deja finalizate, inclusiv la copii și adolescenți cu vârsta de peste 1 an, și au fost prescrise la peste 200.000 de pacienți din întreaga lume. Asocierea dabrafenib + trametinib este, de asemenea, aprobată deja pentru utilizare în mai multe forme de cancer cu mutație BRAF pozitivă: melanom nerezecabil sau metastatic, tratament adjuvant pentru melanom după intervenția chirurgicală, cancer pulmonar non-microcelular metastazat, cancer tiroidian anaplazic.
Citește și:
- STUDIU. Combinația spartalizumab, dabrafenib și trametinib crește supraviețuirea în melanomul BRAF+, chiar și la pacienții cu prognostic nefavorabil
- #ASCO20. Combinația dabrafenib/trametinib crește supraviețuirea fără recidivă la pacienții cu melanom în stadiul III, cu mutații BRAF V600E/K
- #ASCO19. Combinația dabrafenib cu trametinib determină supraviețuire prelungită în melanomul avansat BRAF pozitiv

