FDA aprobă prima terapie celulară anti-BCMA pentru pacienții cu mielom multiplu recidivat și refractar la cel puțin patru terapii anterioare
FDA a aprobat idecabtagene vicleucel (Abecma) pentru tratamentul pacienților adulți cu mielom multiplu recidivant sau refractar la patru sau mai multe linii terapeutice. Aceasta este prima terapie genică și terapie celulară aprobată de FDA pentru mielomul multiplu. Idecabtagene vicleucel este o terapie CAR-T orientată împotriva markerului BCMA.
Siguranța și eficacitatea terapiei au fost evaluate în studiul KarMMa de fază II. Studiul multicentric a înrolat 127 de pacienți cu mielom multiplu recidivat și/sau refractar, care au primit cel puțin trei linii terapeutice anterioare (88% dintre pacienți primiseră patru sau mai multe tratamente anterioare). Eficacitatea a fost evaluată la 100 de pacienți cărora li s-a administrat idecabtagene vicleucel. Rezultatele acestui studiu au fost prezentate în cadrul Programului științific virtual al Societății Americane de Oncologie Clinică (ASCO) 2020.
Rata globală de răspuns a fost de 72% iar rata de răspuns complet a fost de 28%. Timpul mediu până la răspuns a fost de 30 de zile, iar răspunsurile au fost durabile în timp. Durata mediană a răspunsului a fost de 11 luni în grupul de pacienți cu răspuns terapeutic, respectiv de 19 luni în grupul de pacienți care au obținut un răspuns complet strict. În plus, remisiunea a durat cel puțin 12 luni la 65% dintre pacienții care au obținut un răspuns complet. Supraviețuirea mediană globală a fost de 19,4 luni.
“Ide-cel a indus răspunsuri la majoritatea pacienților cu mielom refractar și recidivat în ciuda tratamentului anterior agresiv”, au concluzionat Dr. Nikhil Munshi și colegii săi în revista științifică New England Journal of Medicine.
Cele mai frecvente efecte adverse ale idecabtagene vicleucel includ: sindromul de eliberare de citokine, infecții, fatigabilitate, dureri musculo-scheletice și hipogammaglobulinemie.
Idecabtagene vicleucel a fost aprobat împreună cu o strategie de evaluare și atenuare a riscurilor care necesită ca instituțiile medicale care administrează terapia să fie special certificate pentru a recunoaște și gestiona sindromul de eliberare de citokine și toxicitățile asupra sistemului nervos. Pentru a evalua siguranța pe termen lung, FDA a solicitat producătorului să efectueze un studiu observațional după punerea pe piață a pacienților tratați cu idecabtagene vicleucel.
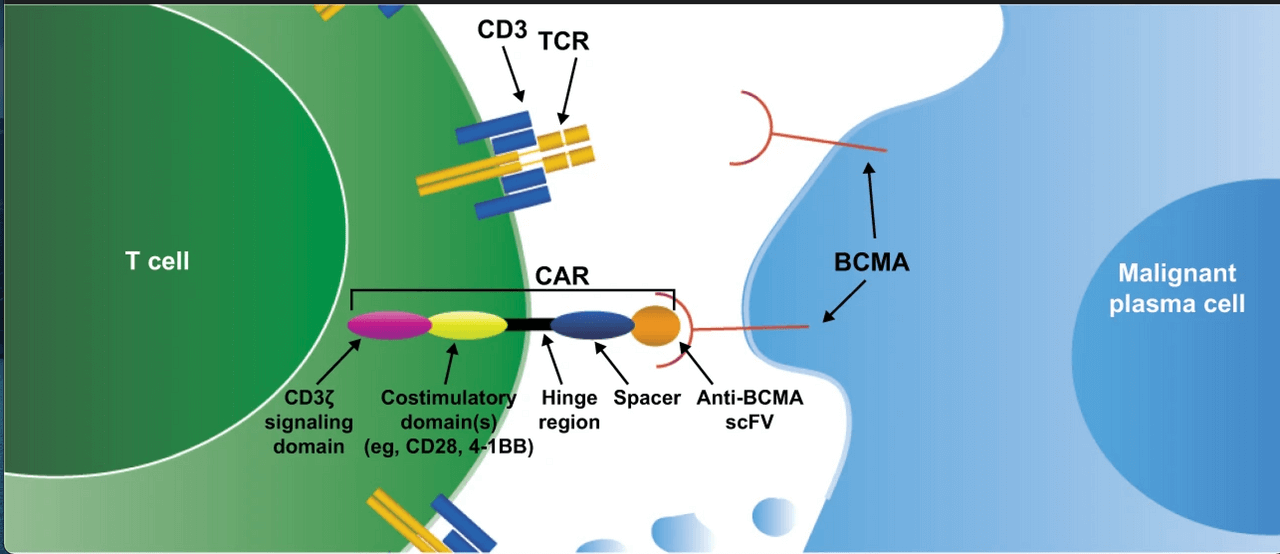
BCMA – țintă terapeutică în mielomul multiplu
Succesul terapiilor CAR-T în tratarea formelor refractare și recidivate de limfom difuz cu celulă B mare (DLBCL) și leucemie limfocitară acută și cronică a încurajat dezvoltarea acestei terapii și pentru mielomul multiplu. Factorul cheie pentru dezvoltarea unei terapii CAR-T eficiente este alegerea țintei potrivite, un antigen de suprafață absent de pe celulele normale.
BCMA (antigenul specific limfocitelor B mature) are rolul de a stimula proliferarea și de a inhiba apoptoza plasmocitelor mature, și mai ales a celulelor tumorale specifice mielomului multiplu. BCMA este un membru al familiei factorului de necroză tumorală, exprimat mai ales de către celulele plasmatice normale și maligne, precum și de unele celule B mature. BCMA nu este exprimat de către celulele stem hematopoietice sau de către celule nonhematologice. Deși BCMA este exprimat uniform de către majoritatea celulelor maligne din mielom, intensitatea exprimării variază între pacienți. Însă gradul de expresie al BCMA nu pare să aibă impact asupra răspunsului la tratament.
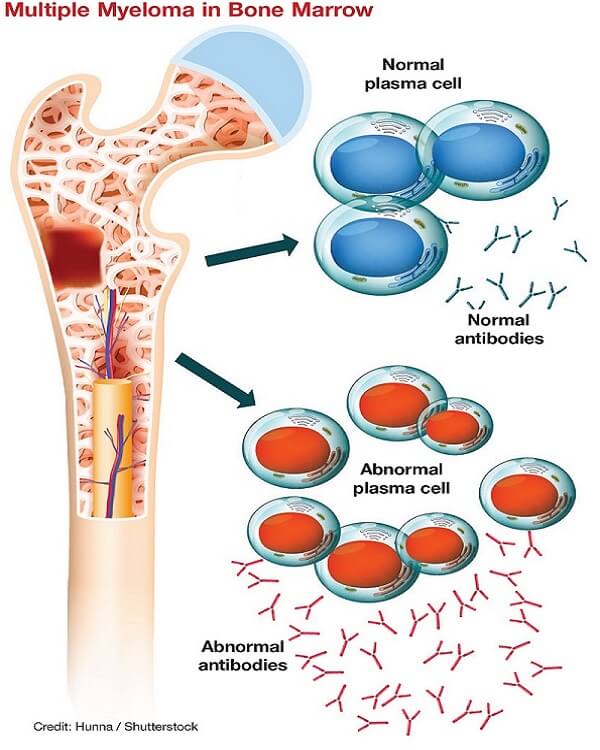
Mielomul multiplu – o boală incurabilă și cu prognostic sever
Mielomul multiplu reprezintă a doua cea mai frecventă formă de cancer hematologic. Anual, 700 de români sunt diagnosticați cu mielom multiplu, iar vârsta pacienților este în continuă scădere.
Celulele afectate sunt plasmocitele de la nivelul măduvei osoase hematogene, care au rol în producerea de anticorpi. Aceste celule se transformă malign, proliferează și produc proteine anormale – utilizate drept markeri pentru diagnosticul și urmărirea pacienților: proteina M (paraproteina) și lanțurile ușoare (componente normale ale imunoglobulinelor, însă produse în cantități anormale de către celulele tumorale). Celulele canceroase și proteinele produse înlocuiesc celulele imune sănătoase de la nivel medular, conducând la slăbirea sistemului imunitar, precum și la afectarea osoasă și renală.
În ciuda tratamentelor disponibile, mielomul multiplu rămâne o boală incurabilă, cu prognostic sever și o povară semnificativă pentru pacienți. Având în vederea lipsa unui tratament curativ, majoritatea pacienților suferă recăderi în evoluția bolii. Odată cu recăderea, de multe ori mielomul capătă rezistență la tratamentele primite anterior. Sunt necesare terapii noi, care să ofere noi opțiuni de tratament odată cu progresia în timp a bolii.
Pacienții cu mielom multiplu recidivat sau refractar care au fost expuși la toate cele trei clase majore de medicamente, inclusiv un agent imunomodulator, un inhibitor al proteazomului și un anticorp anti-CD38, au în general rezultate clinice slabe, cu rate de răspuns foarte scăzute (20-30%), durată scurtă a răspunsului (2 până la 4 luni) și supraviețuire scăzută. Speranţa de viaţă a pacienţilor diagnosticaţi cu mielom multiplu, estimată după apariţia recăderii sau a bolii refractare la tratament, este între 7,5 luni şi 22 de luni, în funcţie de terapia utilizată.
Citește și:
- #ASCO20. CELMoD, o nouă clasă terapeutică pentru mielomul multiplu: primele rezultate favorabile dintr-un studiu de fază I, la pacienți cu forme refractare și recidivate de boală
- FDA aprobă isatuximab pentru pacienții cu mielom multiplu recidivat și refractar la cel puțin două terapii anterioare

