STUDIU. Cardiologia de precizie: un sistem informatic care integrează date clinice și genomice ar putea ghida deciziile terapeutice în anumite cardiomiopatii ereditare
Bolile cardiovasculare reprezintă principala cauză de mortalitate la nivel mondial și o povară majoră pentru sănătatea publică. Totuși, ascensiunea medicinei de precizie a început odată cu oncologia de precizie, datorită cercetărilor pentru descifrarea complexității genetice a cancerului. Însă în ultimii ani, înțelegerea de înaltă definiție a bolilor umane aduce o nouă perspectivă asupra mecanismelor implicate în BCV. Contrar percepției publice, bolile cardiovasculare nu pot fi prevenite întotdeauna prin stilul de viață. Multe afecțiuni cardiovasculare sunt ereditare.
O echipă formată din oameni de știință din cadrul MIT, Wellcome Sanger Institute și Universitatea Lund a dezvoltat un sistem computerizat integrat, genomic, folosind date clinice, care poate ajuta la informarea deciziilor terapeutice și chirurgicale (de ex., montarea defibrilatoarelor și transplantul de inimă) pentru pacienții cu anumite cardiomiopatii ereditare. Mai exact, în cadrul studiului, publicat în npj Genomic Medicine, s-au evaluat variațiile genetice care influențează structura troponinelor, proteine implicate în diferite tipuri de boli cardiace moștenite în care funcționarea mușchiului cardiac este afectată.
Cercetările anterioare, deși multiple, nu au ajuns la acest nivel de acuratețe și integrare la nivel genomic până acum. Conform autorilor, cercetări ulterioare ar putea transforma „punctele fierbinți” genetice identificate în ținte terapeutice.
„Am combinat evaluarea structurală și funcțională avansată a variantelor genetice cu strategii noi de gestionare a datelor, care integrează toate informațiile disponibile anterior în literatura internațională despre fiziopatologie și manifestările clinice ale pacienților cu acele variante genetice. Acest tip de studii sunt esențiale pentru dezvoltarea unui medicament cu adevărat personalizat în bolile cardiovasculare moștenite, abordând nu numai provocările diagnostice și preventive, cum ar fi decizia de a implanta sau nu un defibrilator, ci și pentru dezvoltarea și selecția adecvată a tratamentelor noi”, a declarat Dr. Lorenzo Monserat, co-autor al studiului.
Sistemul informatic biologic integrat genomic
Studiul oferă noi perspective pentru înțelegerea corelațiilor dintre cardiomiopatii și variațiile Tn. Noul model de sisteme biologice (systems biology model) sintetizează datele pacienților cu privire la prognosticul și rezultatele variațiilor Tn, cu date structurale ale complexului Tn. Inițial, au fost determinate regiunile relevante ale proteinelor Tn, pe baza interacțiunilor dependente de calciu și a siturilor aflate sub selecție negativă. Apoi, au fost identificate hotspot-urile de variație, corelațiile și prognosticul genotip-fenotip pentru fiecare regiune prin efectuarea unei metanalize a datelor clinice din literatura științifică medicală cu acces liber și din bazele de date publice.
Pentru crearea sistemului au fost utilizate date provenite din secvențierea genelor care codifică proteinele de la nivelul filamentelor subțiri ale fibrelor musculare, preluate din UniProt (o colecție importantă de secvențe de proteine și adnotările lor – conține milioane de secvențe) și au fost incluse proteinele TnT, TnI, TnC, ACTC1 și TPM1. Iar pentru a acoperi o gamă largă din istoria evolutivă, genele ortoloage specifice proteinelor filamentului subțire uman au fost identificate cu BLASTP (Basic local alignment search tool), din baza de date NCBI RefSeq. Au fost utilizate atât secvențe proteice de la mamifere (om + șoareci), cât și de la anumite specii de păsări și pești.
Algoritmul a fost testat pe date open-access provenite de la nivel global, din aproximativ 100 de studii anterioare, cu peste 980 de pacienți înrolați, în care a fost investigat impactul variațiilor genetice asupra interacțiunilor dintre proteinele din miocard.
Toate detaliile sunt prezentate în lucrarea originală, însă ceea ce este important de subliniat este faptul că toate aceste date și algoritmi de bază erau deja disponibili pentru lumea științifică, iar elementul care a făcut diferența a fost integrarea inovatoare. Mai mult, atât datele, cât și algoritmii personalizați pe acestea sunt disponibile la cerere.
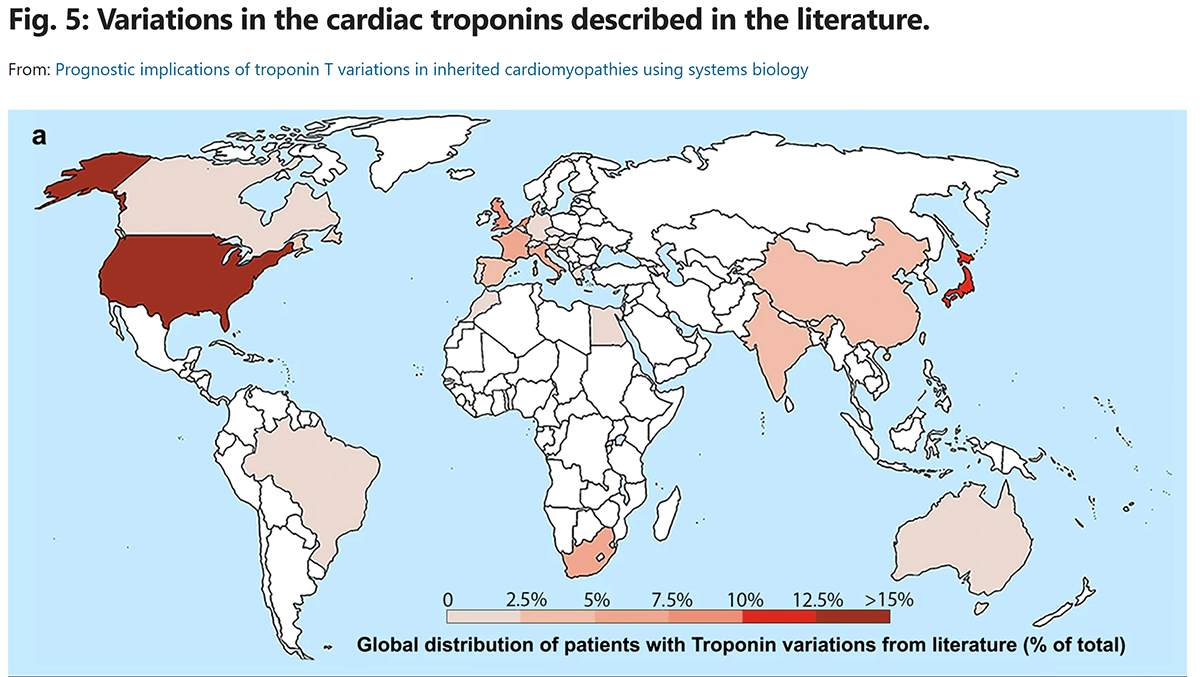
Rolul Tn în BCV ereditare
Cele mai frecvente forme de boli cardiace genetice sunt cardiomiopatiile moștenite (un grup de afecțiuni rare ale mușchiului cardiac, ce afectează structura și funcția fiziologică a miocardului), care afectează aproximativ 0,2% din populația globală – acestea sunt cele mai frecvente forme de BCV genetice (definite până acum). Variațiile genetice se găsesc în mod obișnuit în regiunile care codifică proteinele sarcomerice, care sunt elementele de bază ale mușchiului cardiac și includ proteinele numite troponine.
Variațiile troponinei cardiace T au fost adesea utilizate ca exemplu de aplicare a genotipării clinice pentru diagnosticare și stratificare a riscului pentru pacienții cu antecedente familiale de deces subit cardiac sau cardiomiopatie familială.
Se consideră că variațiile Tn (troponina) contribuie aproximativ la 8-10% din toate cardiomiopatiile proteinelor sarcomerice cunoscute. Deși există multiple date de interacțiune obținute cu microscopie electronică și rezonanță magnetică nucleară, rezoluția este prea limitată pentru a oferi o hartă de interacțiune proteină-proteină.
„Pentru a integra mai bine datele genomice în opțiunile clinice din lumea reală pentru milioane de pacienți cu boli cardiovasculare moștenite și familiile acestora, avem nevoie de o apreciere integrată a datelor genetice, fizice, bio-chimice și clinice, așa cum se arată în acest studiu. Acest studiu reprezintă următorul pas în integrarea cardiologiei de precizie în îngrijirea clinică și în colaborarea mai strânsă cu colegii de genetică clinică și pacienții cu familiile acestora, reducând decalajul dintre cercetare și deciziile de tratament de zi cu zi. Această cercetare ne-a permis să deschidem, de asemenea, ușa către noi terapii potențiale, pe care sperăm să le introducem în curând”, Dr. Rameen Shakur, autor principal al studiului.
Încă de la primele observații care au asociat variațiile genetice ale complexului Tn cu clasificările morfologice – cum ar fi cardiomiopatia hipertrofică (CMH) și riscul crescut de deces cardiac subit (DCS) – au existat multe studii care au încercat să definească implicațiile în gestionarea și prognosticul clinic a relației genotip-fenotip.
De exemplu, variațiile genei cardiace TnT (TNNT2) determină CMH cu fenotipuri clinice variabile: unii pacienți prezintă un risc ridicat de aritmii ventriculare și DCS, însă fără hipertrofie ventriculară stângă vizibilă care să ghideze decizia terapeutică și aproximarea prognosticului. Acest lucru aduce dificultăți în stabilirea momentului optim pentru aplicarea terapiei (cum ar fi defibrilatoarele cardiace implantabile) pentru pacienți. De aceea, stabilirea prognosticului pe baza factorilor genetici este crucială.
„Acest nou instrument reprezintă un progres semnificativ în cardiologia de precizie, cu potențial real de veni în beneficiul pacienților cu boli cardiace moștenite și de a influența asistența medicală genomică. Studiul demonstrează importanța colaborării și a schimbului de cunoștințe în stimularea inovației cu rezultate reale”, a declarat Prof. Sir Mark Caulfield, Chief Scientist, Genomics England
La începutul lunii iunie, multiple organizații au semnat o declarație comună prin care solicită Uniunii Europene să dezvolte un Plan UE comprehensiv pentru bolile cardiovasculare. Mai multe detalii: #BeatCVD. Planul european de luptă împotriva bolilor cardiovasculare: 12 organizații europene și internaționale lansează un apel către CE
Citește și:
- #ACC21. Interviu cu Prof. Dr. G. Andrei Dan: „Congresul Colegiului American de Cardiologie de anul acesta reprezintă o răscruce importantă în cercetare”
- Document de poziție ESC: recomandări pentru implementarea farmacogenomicii în managementul bolilor cardiovasculare
- CONSENS. Prima definiție universală a insuficienței cardiace și o nouă clasificare bazată pe biomarkeri