O nouă terapie genică determină valori normale ale factorului IX la pacienții cu hemofilie B severă
9 din 10 pacienți cu hemofilie B severă sau moderat-severă tratați cu o nouă terapie genică, FLT180a, au atins niveluri normale și durabile ale factorului IX, nu au mai avut deloc episoade de sângerare spontană și nu au mai necesitat administrare profilactică de factor IX.
FLT180a (verbrinacogene setparvovec) este o terapie genică dezvoltată cu scopul de a normaliza nivelurile factorului IX al coagulării, produs în cantități extrem de scăzute la persoanele cu hemofilie B ca urmare a unei mutații genetice. Conform standardului actual de îngrijire, pacienții cu hemofilie B necesită profilaxia episoadelor hemoragice pe tot parcursul vieții prin injecții regulate cu terapie de substituție cu factor IX. Cu toate acestea, pacienții continuă să prezinte dureri articulare potențial severe. Deși au apărut terapii substitutive a factorilor de coagulare cu timpi de înjumătățire prelungiți, profilaxia rămâne invazivă și extrem de costisitoare.
Studiul multicentric, deschis, de fază 1/2, B-AMAZE, a înrolat 10 pacienți în vârstă de peste 18 ani, cu hemofilie B severă sau moderat-severă, definită ca având un nivel de factor IX sub 2% față de valorile normale. Terapia genică a fost administrată o singură dată pe cale perfuzabilă, într-unul dintre cele patru regimuri de doze. Pentru că terapia FLT180a folosește drept vector, virusul adeno-asociat (AAV), toți pacienții au primit, de asemenea, terapie imunosupresoare (glucocorticoizi cu sau fără tacrolimus) pentru o perioadă de la câteva săptămâni până la câteva luni, pentru a împiedica organismul să respingă terapia genică.
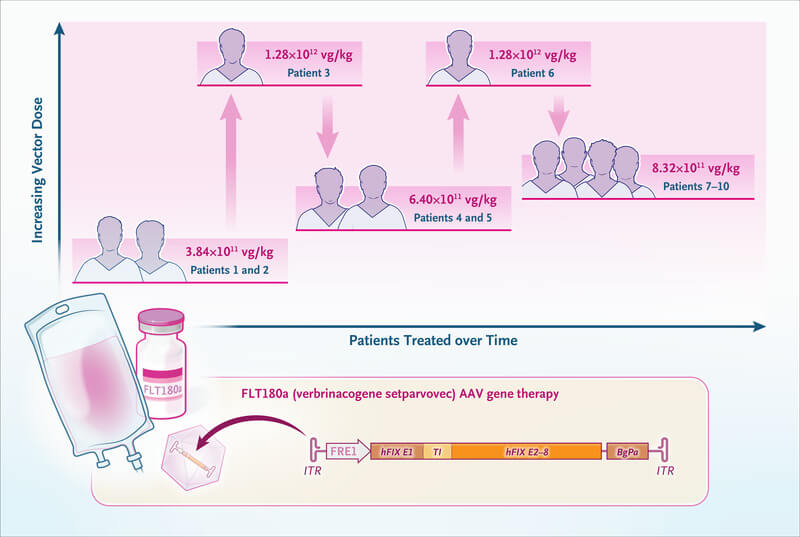
După perfuzia cu FLT180a, toți pacienții au prezentat creșteri dependente de doză ale nivelului factorului IX. După o urmărire mediană de 27 de luni, aproape toți pacienții (9 din 10) au continuat să prezinte activitate susținută a factorului IX. Producția constantă a factorului IX a început în luna 12, asociată cu frecvența scăzută a sângerărilor, ceea ce a permis acestor nouă pacienți să nu mai necesite injecții săptămânale profilactice.
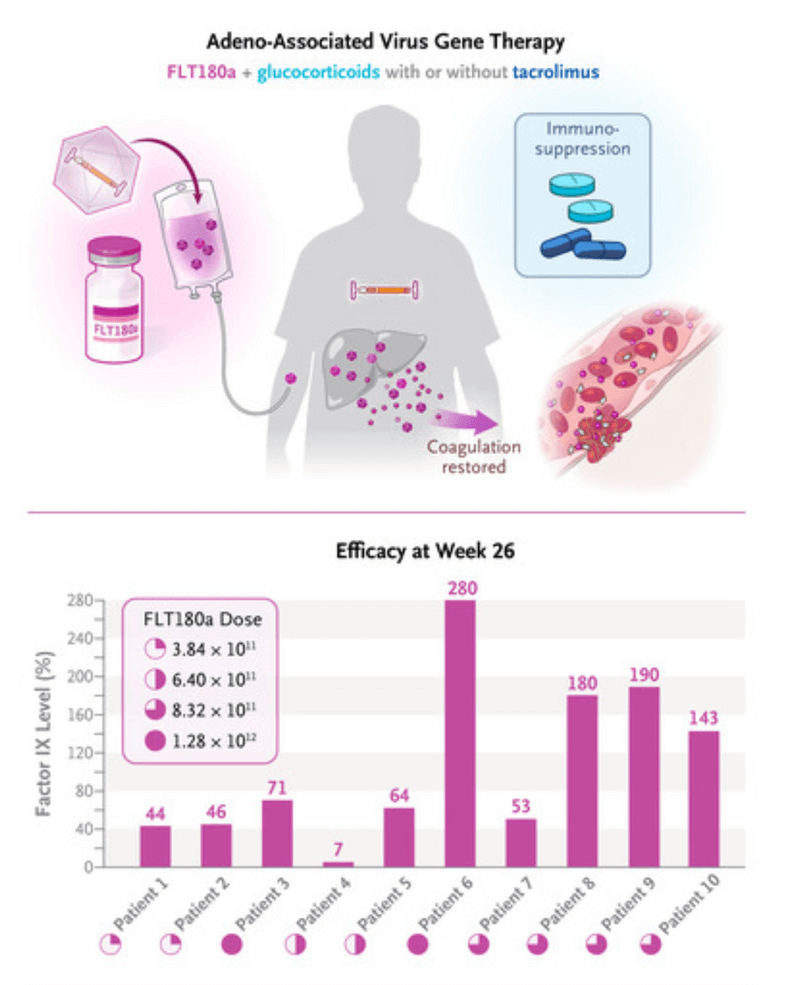
- Cinci pacienți au obținut niveluri ale factorului IX în intervalul normal, între 51%-78%;
- Trei pacienți au avut creșteri mai mici, de 23%-43% față de valorile normale;
- Un pacient, care a primit cea mai mare doză, a avut nivel de 260% față de normal;
- Excepția – un pacient care a necesitat revenirea la profilaxia cu factor IX după ce a înregistrat eșecul regimului de imunosupresie la aproximativ 22 de săptămâni după tratament.
Studiul a arătat astfel, că prin această terapie se pot obține niveluri crescute ale factorului IX, însă rămâne de determinat doza optimă necesară pentru a obține niveluri ale factorului IX între 50-150% din normal.
Terapia a fost în general bine tolerată, fără reacții la administrarea perfuziei sau necesitatea întreruperii administrării, și nu au fost detectați inhibitori ai factorului IX. Dintre evenimentele adverse, aproximativ 10% au fost asociate terapiei genice. Cel mai frecvent eveniment asociat a fost creșterea transaminazelor hepatice, o problemă deja cunoscută a terapiile genice care folosesc AAV drept vector. 24% dintre efectele adverse au fost legate de imunosupresie, în concordanță cu profilurile de siguranță cunoscute ale glucocorticoizilor și tacrolimusului. Singurul eveniment advers sever a fost un episod de tromboză de fistulă arteriovenoasă, apărută la pacientul care a primit cea mai mare doză de terapie genică și care a prezentat cele mai mari niveluri de factor IX.
Vindecarea hemofiliei prin terapie genică, tot mai aproape de realitate
Hemofilia A și B sunt afecțiuni moștenite care decurg din mutații la nivelul unei singure gene, ce determină o producție defectuoasă a unei proteine, oferind o posibilă țintă pentru terapia genică. Cel mai frecvent tip de terapie genică utilizează drept vector, virusul adeno-asociat, prin care o copie corectă a genei defecte este inserată în vectorul viral situat în nucleul celulei, unde poate fi utilizat pentru producerea de proteine. AAV epizomal este un vector bun de livrare a genelor, cu potențial scăzut de imunogenitate, non-inflamator și non-patogen. Pentru tratamentul hemofiliei A și B, terapia genică folosește vectorul AAV pentru a furniza o copie funcțională a genei factorului VIII sau factorului IX la nivel hepatic pentru a facilita expresia factorului VIII sau IX, în funcție de tipul de hemofilie.
Standardul actual de îngrijire pentru hemofilie constă în tratament pe tot parcursul vieții cu terapie de substituție a factorului de coagulare lipsă, iar persoanele cu hemofilie necesită de obicei terapie cronică pentru prevenirea hemoragiei severe. Însă există mai multe limitări ale terapei profilactice de substituție a factorilor de coagulare: accesul venos, nivelurile scăzute de factori de coagulare între administrări, asociate cu sângerări articulare, și potențialul de dezvoltare a inhibitorilor (mai pronunțat în cazul hemofiliei A).
Urmărirea pe termen lung a evoluției este esențială pentru îmbunătățirea înțelegerii hemofiliei și a terapiei genice. Variabilitatea răspunsurilor și durabilitatea observate în studiile clinice au evidențiat diferențe substanțiale între pacienți în atingerea și susținerea nivelurilor factorilor de coagulare. Factorii care pot afecta variabilitatea răspunsului la terapia genică ce utilizează vector AAV includ:
- boala hepatică preexistentă;
- terapia medicamentoasă actuală și afecțiunile asociate;
- factori genetici necunoscuți și celula țintă, având în vedere că hepatocitele nu reprezintă locul natural de producție endogenă a FVIII (sintetizate la nivelul celulelor endoteliale).
Cu toate acestea, variabilitatea răspunsului dintre pacienți nu este limitată la terapia genică, ci este observată și în cazul tratamentelor utilizate în prezent pentru hemofilie; pacienții tratați cu FVIII prezintă o variație de 4 ori a timpului de înjumătățire a concentratului de factor de coagulare.
Rezultatele actuale, împreună cu datele dintr-un alt studiu recent asupra unei terapii genice pentru pacienții cu hemofilie A, subliniază că „răspunsurile imune pot apărea mai târziu decât se credea anterior și pot coincide cu întreruperea terapiei imunosupresoare”, avertizează autorii. Între timp, pacienții înrolați în studiul B-AMAZE vor continua să fie urmăriți pe termen lung pentru a evalua siguranța și durabilitatea terapiei FLT180a pe o perioadă de 15 ani.
La începutul anului, un alt studiu de fază 3, HOPE-B, demonstra că terapia genică AMT-061 (etranacogene dezaparvovec) a permis întreruperea terapiei profilactice a sângerării la 96% din pacienții cu forme severe sau moderat-severe de hemofilie B, a redus cu 64% rata anuală de sângerări și a scăzut cu 77% episoadele de sângerare care necesită administrare de factor IX. Terapia AMT-061 este formată din gena FIX funcțională și un vector reprezentat de virusul AAV5. În acest studiu, însă, nu s-a utilizat corticoterapie profilactică, tratamentul steroid fiind necesar pentru 16% dintre pacienți pentru o durată medie de numai 79 de zile.
Citește și:
- Carta Albă a Hemofiliei 2020 – o analiză asupra managementului hemofiliei în România, cu scopul de a sprijini dezvoltarea politicilor de sănătate bazate pe dovezi
- STUDIU. Impactul socio-economic al hemofiliei în România
- BREAKING NEWS. Vindecarea hemofiliei A și B prin terapii genice este mai aproape de a deveni realitate

