Rata de remisiune completă este superioară în cancerul de sân HER2-negativ tratat cu durvalumab și olaparib, adăugate la paclitaxel, comparativ cu chimioterapia clasică
O nouă combinație terapeutică, formată din durvalumab (Imfinzi, inhibitor de PD-1/PD-L1) și olaparib (Lynparza, inhibitor PARP) în combinație cu chimioterapia neoadjuvantă clasică (paclitaxel), a arătat o rată de remisiune completă superioară administrării exclusiv a chimioterapiei. Aceste rezultate au fost evidențiate în cazul tuturor subtipurilor de cancer de sân HER2-negativ, inclusiv în cazul celor estrogen-receptor pozitiv, HER2-negativ și triplu negativ.
„Aceste rezultate oferă dovezi suplimentare pentru valoarea clinică a imunoterapiei în stadiile incipiente ale cancerul de sân și sugerează noi căi pentru utilizarea acestor medicamente în cazul cancerelor mamare cu receptori hormonali pozitivi.”- a afirmat Prof. Lajos Pusztai, Yale Cancer Center.
Despre studiu
I-SPY2 este un studiu clinic randomizat care a înrolat 73 de pacienți cu cancer de sân HER2-negativ. Acesta cuprinde mai multe brațe experimentale dintre care un braț de control comun, în cadrul căruia pacienților li s-au administrat, o dată pe săptămână, timp de 12 săptămâni, perfuzii cu chimioterapie clasică cu paclitaxel, urmate de patru cure de chimioterapie pe bază de antracicline.
Tratamentele au fost administrate înainte de intervenția chirurgicală, iar rezultatul principal evaluat a fost dacă tratamentele experimentale cresc proporția pacienților care au un răspuns histopatologic complet (pCR), detectat în țesutul mamar și ganglionii limfatici îndepărtați în timpul intervenției chirurgicale.
Rezultatele au arătat că adăugarea de durvalumab și olaparib la paclitaxel a îmbunătățit semnificativ rata pCR pentru pacienții cu cancer de sân HER2-negativ în comparație cu chimioterapia standard citotoxică. Rata estimată a pCR pentru pacienții cu cancer de sân HER2-negativ a fost de 37% pentru cei care au primit durvalumab, olaparib și paclitaxel standard și 20% pentru pacienții tratați în grupul control.

Dintre cei 73 de pacienți, 21 au avut cancer de sân triplu negativ și 52 au avut cancer de sân HR-pozitiv cu caracteristici Mammaprint de risc ridicat (test genetic diagnostic ce evaluează 70 de gene și prezice în fază incipientă riscul unei tumori de sân de a metastaza; este utilizat în decizia terapeutică de a administra sau nu chimiotarapie). Îmbunătățirea ratei pCR estimate a fost cea mai mare în cazul pacienților care au avut cancer de sân triplu negativ. Rata estimată a pCR pentru pacienții cu cancer de sân triplu negativ a fost de 47% pentru cei care au primit durvalumab, olaparib și paclitaxel standard și 27% pentru pacienții tratați cu terapie de control. În rândul pacienților cu cancer de sân HER2-negativ cu HR-pozitiv, ratele pCR estimate au fost de 28% pentru cei care au primit durvalumab, olaparib și paclitaxel standard și 14% pentru cei din brațul de control.
,,Analizele exploratorii sugerează existența posibilă a mai multor markeri predictivi care arată beneficiile durvalumab/olaparib față de administrarea doar a chimioterapiei.”- a adăugat Prof. Pusztai.
În legătură cu acest studiu, Prof. Pamela Munster, de la Helen Diller Family Comprehensive Cancer Center a afirmat că integrarea inhibitorilor punctelor de control imun în tratamentul cancerului mamar aflat în stadiu incipient este un domeniu interesant de cercetare. Deși datele arătate sugerează că adăugarea de durvalumab și olaparib la paclitaxel determină rezultate promițătoare, rămâne de stabilit cât de mult din beneficii a fost conferite de olaparib. Aceasta a concluzionat că vor fi necesare studii randomizate confirmatorii care includ analiza expresiei PD-L1 și a expresiei mutației BRCA înainte ca terapiile combinate ale inhibitorilor PARP să poată fi introduși ca tratament pentru cancerul mamar în stadiu incipient.

Despre reacțiile adverse, Prof. Lajos a afirmat că cele două terapii aduc reacții adverse adiționale, dar acestea au fost cele așteptate în cazul oricărui tip de imunoterapie: colită, hipotiroidie, insuficiență adrenală. Acesta a adaugat că numărul pacienților care au experimentat anemie sau fatigabilitate a fost mai mic în cazul combinației durvalumab/olaparib și paclitaxel, comparativ cu administrarea doar a terapiei cu paclitaxel. Despre rata de toxicitate cumulată rezultatele oferite sunt unele preliminarii, calculate în cazul a 44 dintre pacienți care au experimentat toxicitate completă. Ratele de toxicitate de grad 3 sau 4 au fost înregistrate în cazul a 56% de paciente în grupul cu terapie combinată și 48% în cazul grupului control.

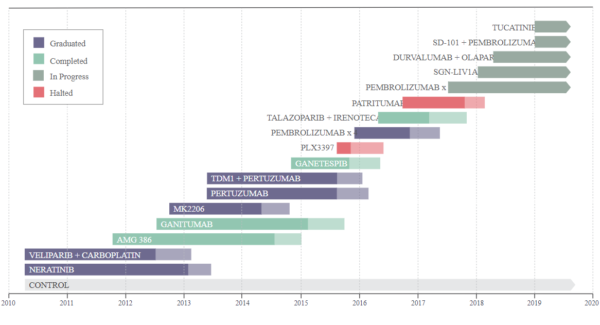
Despre studiul I-SPY2
I-SPY este un studiu randomizat atipic care are ca scop creșterea eficacității unui studiu clinic prin minimizarea numărului de participanți și a timpului alocat evaluării agenților experimentali. Acesta este o platformă în curs de dezvoltare care explorează utilizarea de noi medicamente în combinație cu o terapie neoadjuvantă standard pentru tratamentul cancerului cu risc ridicat.
În acest studiu, femeile cu cancer de sân în stadiul II sau III cu tumori cu dimensiuni de 2,5 cm sau mai mult sunt evaluate pentru unul din cele opt subtipuri de biomarkeri, în funcție de statutul HER2, HR și factorii de risc genetici, după cum s-a determinat pe baza unui test pentru 70 de gene. Pacienții sunt repartizați aleatoriu pentru a primi terapie standard, cu sau fără agentul cercetat. Pentru fiecare subtrial, un efect principal este o îmbunătățire a pCR în comparație cu standardul prezent.
Modificările tumorale de volum identificate cu ajutorul RMN sunt utilizate pentru a prezice dacă pacienții vor atinge un răspuns complet, evaluat histopatologic (pCR). Cei care sunt considerați a avea o probabilitate statistică mare (estimată prin analiza matematică Bayesiană) de de a avea succes sunt eligibili pentru a trece la studiile de faza 3.
Despre durvalumab
Durvalumab este un anticorp monoclonal care blochează interacțiunea ligandului PD-L1 cu moleculele PD-1 și CD80. Durvalumab este aprobat pentru tratarea pacienților cu carcinom urotelial avansat sau metastatic local în anumite condiții, pentru cancerul pulmonar non-microcelular stadiul 3 nerezecabil în monoterapie și reprezintă tratamentul de primă linie aprobat FDA în cancerul pulmonar cu celule mici extins (ES-SCLS) în combinație cu etoposid și carboplatin sau cisplatin.
Mai multe articole despre durvalumab:
- FDA aprobă durvalumab în tratamentul de primă linie al cancerului pulmonar cu celule mici extins
- #ASCO19. Durvalumab crește rata de supraviețuire pentru cancerul pulmonar non-microcelular avansat la pacienții care beneficiază concomitent de chimioterapie și radioterapie
- Durvalumab: prima imunoterapie aprobată în UE pentru cancerul pulmonar non-microcelular stadiul 3, nerezecabil
Despre olaparib
Olaparib este un inhibitor PARP (enzima poli ADP- riboză polimerază implicată în repararea ADN-ului). Acționează împotriva cancerului la persoanele cu mutații BRCA1 sau BRCA2, care includ unele tipuri de cancer ovarian, de sân și prostată. Este aprobat pentru cancerul ovarian avansat cu mutare BRCA (gBRCAm), care a primit trei sau mai multe linii anterioare de chimioterapie. Olaparib este primul inhibitor PARP care a fost aprobat de FDA pentru cancerul de sân metastatic gBRCAm.
Mai multe articole despre olaparib:
- Olaparib, aprobat de FDA pentru tratamentul de menținere a cancerului pancreatic metastatic BRCA-pozitiv
- #ESMO19. Olaparib, asociat tratamentului de întreținere cu bevacizumab, crește supraviețuirea fără progresie a bolii la pacientele cu cancer ovarian avansat
- #ASCO19. Olaparib dublează numărul de pacienți în remisiune, în cazul cancerului pancreatic metastatic, BRCA-pozitiv
- #ESMO18. Cancerul ovarian avansat- risc de recurență cu 70% mai mic sub tratament cu olaparib
Citește și:
- #ASCO20. Imunoterapia avelumab, eficientă într-o formă rară de cancer ginecologic rezistent la chimioterapie
- #ASCO20. Tratamentul adjuvant cu osimertinib reduce cu 83% riscul de deces sau recurență în cancerul pulmonar non-microcelular EGFR+
- Combinația de pertuzumab cu trastuzumab și docetaxel crește cu 37% supraviețuirea la 8 ani în cancerul de sân HER-2 pozitiv metastazat

