Olaparib, în curs de aprobare în UE pentru cancerul pancreatic metastatic BRCA pozitiv
Comitetul pentru Produse Medicamentoase de Uz Uman al Agenției Europene a Medicamentului (CHMP) recomandă adăugarea unei noi indicații a olaparib (denumire comercială Lynparza): monoterapie în tratamentul de menținere a pacienților adulți cu adenocarcinom pancreatic metastatic BRCA1/2 pozitiv, care nu a progresat cel puțin 16 săptămâni după un tratament chimioterapic de primă linie cu compuși de platină.
Această opinie va fi transmisă Comisiei Europene în sprijinul adoptării deciziei de autorizare a punerii pe piață în UE. De obicei, Comisia finalizează o astfel de decizie în aproximativ 2 luni de la primirea opiniei pozitive din partea CHMP. Olaparib este aprobat din ianuarie 2020 în Statele Unite.
„Tratamentul pacienților cu cancer pancreatic avansat a evoluat puțin în ultimele decade. Acum suntem cum un pas mai aproape de a aduce prima medicație țintită în cancerul pancreatic avansat, din UE, unui subgrup de pacienți selectați cu ajutorul unui biomarker”- José Baselga, vicepreședinte executiv, Departamentul de cercetare și dezvoltare oncologică, Astra-Zeneca.
Studiul care a dus la aprobare – POLO
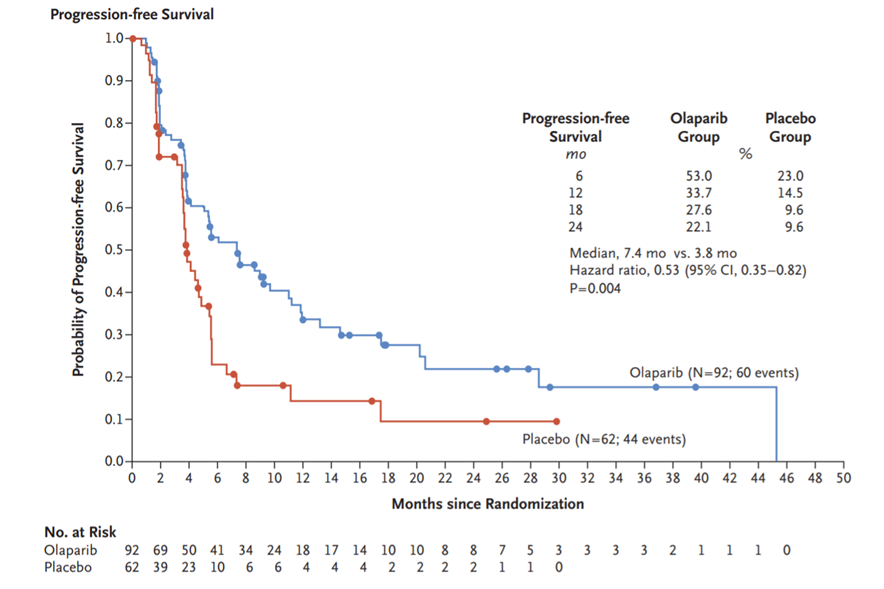
Recomandarea are la bază rezultatele pozitive ale studiului POLO, publicate în The New England Journal of Medicine.
„Diagnosticul de cancer pancreatic este devastator. Noi suntem dedicați cercetării care urmărește să schimbe prognosticul acestor pacienți. Studiul de fază III POLO a demonstrat că tratamentul cu Lynparza crește timpul de supraviețuire fără progresia bolii la anumiți pacienți cu cancer pancreatic avansat. Suntem încrezători că vom putea să aducem curând acest medicament, pacienților din UE” – Roy Baynes, vicepreședinte senior și șeful Departamentului de dezvoltare clinică globală, MSD Research Laboratories.
Studiul randomizat, dublu-orb, controlat cu placebo de fază III, a inclus 154 de pacienți cu cancer pancreatic BRCA-pozitiv metastatic, care nu a evoluat sub chimioterapia de linia I (care include compuși de platină). Astfel, 92 de pacienți au primit 300 mg olaparib oral de două ori pe zi, iar 62 au primit placebo. Rezultatele au fost semnificative:
- Supraviețuirea fără progresia bolii a fost de 7,4 luni în cazul tratamentului cu olaparib, față de 3,8 luni în cazul placebo;
- După 6 luni de la debutul studiului, de două ori mai mulți pacienți au supraviețuit fără progresia bolii în cazul olaparib, față de placebo (53%, față de 23%);
- În urma unei analize interimare a datelor, supraviețuirea globală a fost similară între cele două grupuri;
- Rata de răspuns a fost de 20% în cazul olaparib, față de 10% în grupul placebo;
- Profilul de siguranță a fost similar cu cel al studiilor anterioare (grupul olaparib a suferit în proporție de 24% reacții adverse grave, față 15% în cazul grupului placebo).
Olaparib
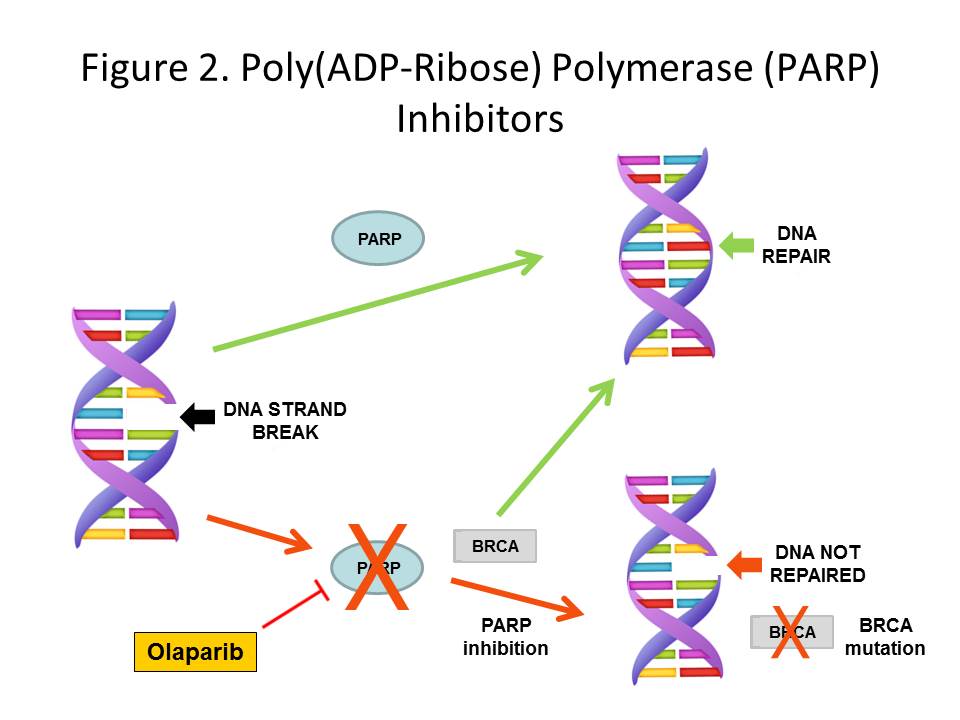
Olaparib (denumire comercială Lynparza), este primul medicament din clasa inhibitorilor PARP. Celulele cu modificări metabolice cauzate de mutația BRCA sunt sensibile la acțiunea acestei clase terapeutice, prin intermediul unei enzime de reparare a ADN-ului, denumită PARP (poly-adenosine diphosphate–ribose polymerase). În cazul tumorilor BRCA-pozitive, celulele tumorale utilizează frecvent calea enzimatică PARP pentru a repara genomul și pentru a se multiplica. Astfel, prin inhibarea PARP, olaparib împiedică proliferarea tumorilor BRCA-pozitive.
În prezent, Lynparza este aprobat de Agenția Europeană a Medicamentului în tratamentul de întreținere a pacienților adulți cu tumori BRCA-pozitive, recidivate, sensibile la chimioterapie pe bază de platină:
- epiteliale, seroase, de grad înalt ovariene sau de trompă uterină;
- primare peritoneale.
Cancerul pancreatic BRCA pozitiv
Cancerul pancreatic are una dintre cele mai scăzute rate de supraviețuire dintre cancerele comune. Este al 11-lea cel mai comun cancer la nivel global și a 7-a cauză de mortalitate oncologică. În 2018, a cauzat peste 400.000 de decese la nivel global.
Mutația BRCA este cel mai frecvent asociată cu apariția cancerului mamar sau ovarian. 72% dintre femeile ce prezintă mutația BRCA1 dezvoltă cancer mamar până la vârsta de 80 de ani, iar procentul este de 69% pentru mutatia BRCA2.
În afară de aceste tipuri tumorale, mutația BRCA reprezintă un factor de risc și pentru alte tumori, precum cancerul pancreatic. În funcție de tipul mutației, riscul de cancer pancreatic este de 2,2 – 3,5 ori mai ridicat printre purtătorii de mutație BRCA, față de populația generală.
Tumorile pancreatice cu mutații la nivelul genelor BRCA1 sau BRCA2 reprezintă o proporție scăzută din totalul acestor tumori, de 4-7%. Tumorile pancreatice metastatice prezintă o agresivitate semnificativă: tratamentul actual conduce la o supraviețuire lipsită de progresie a bolii de aproximativ 6 luni, iar mai puțin de 10% dintre pacienți supraviețuiesc mai mult de 5 ani de la diagnostic.
Citește și:
- Rata de remisiune completă este superioară în cancerul de sân HER2-negativ tratat cu durvalumab și olaparib, adăugate la paclitaxel, comparativ cu chimioterapia clasică
- Olaparib, aprobat de FDA pentru tratamentul de menținere a cancerului pancreatic metastatic BRCA-pozitiv
- #ASCO20. Terapia de întreținere cu olaparib crește supraviețuirea în cancerul ovarian recidivat BRCA-pozitiv cu peste 1 an
Sursă imagine feature: kjpargeter, freepik.com.

