Raport EFPIA: Provocări și facilitatori în dezvoltarea medicamentelor orfane și pediatrice. Recomandări pentru adoptarea inovației
Federația Europeană a Industriilor și Asociațiilor Farmaceutice (EFPIA), împreună cu Oficiul de Economie Sanitară (OHE – Office of Health Economics), au lansat recent un raport asupra provocărilor cu privire la dezvoltarea medicamentelor orfane sau pediatrice. Raportul oferă și o serie de recomandări, sumarizate astfel:
Multe dintre barierele identificate în acest raport – în special lipsa de flexibilitate și pragmatism în politicile de reglementare și de rambursare – ar putea fi reduse printr-o colaborare mai strânsă și timpurie între industrie și autoritățile de reglementare sau plătitori. O astfel de colaborare ar putea reduce incertitudinea, timpul și costurile în procesul de dezvoltare și ar putea încuraja dezvoltări majore în domenii care adresează nevoi urgente neacoperite.
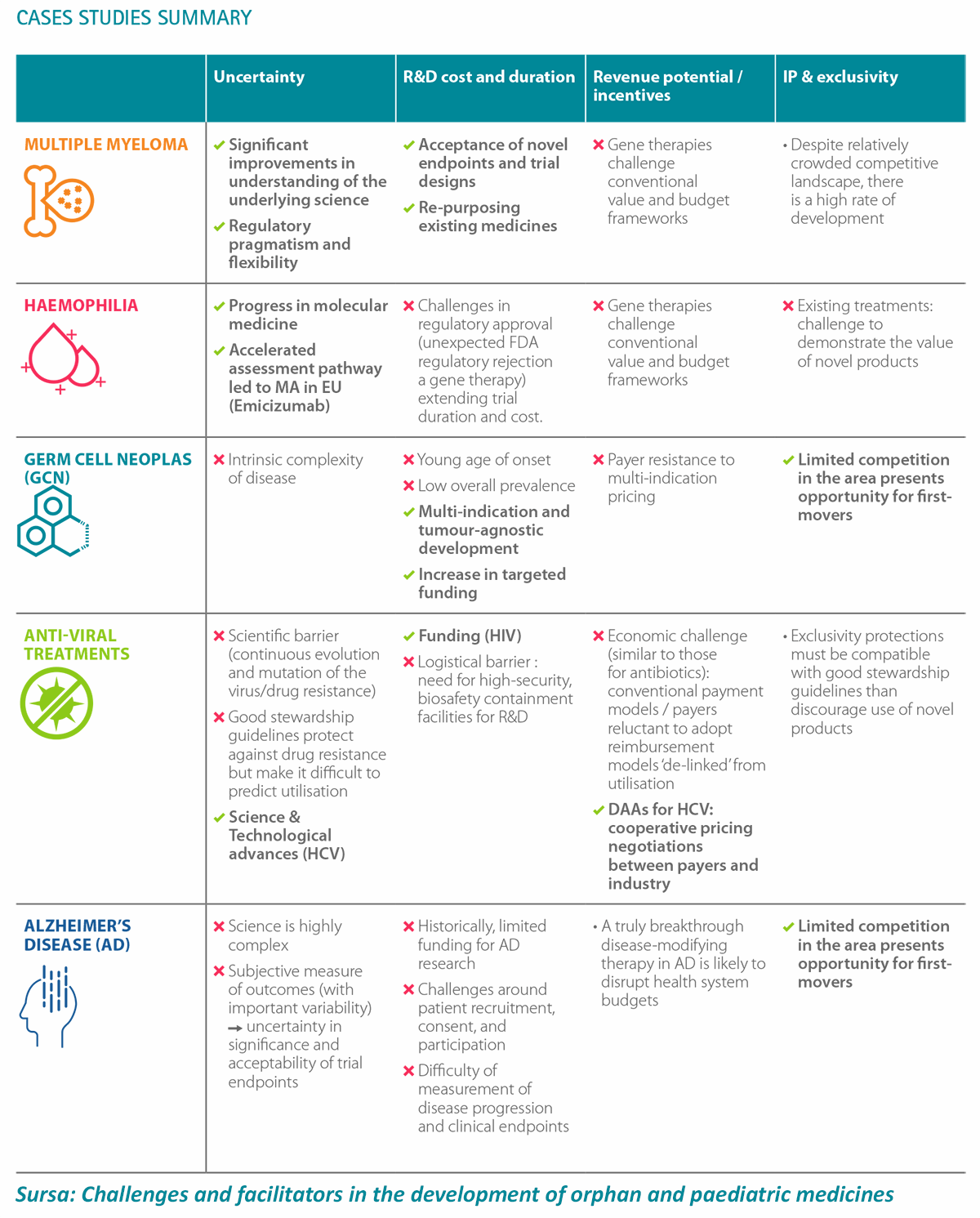
Pentru a înțelege mai bine provocările și abordarea actorilor implicați, specialiștii au utilizat conceptul rNPV ( RISK-ADJUSTED NET PRESENT VALUE), care ia în considerare 4 dimensiuni:
- Riscurile și necunoscutele/ incertitudinile: succesul științific, aprobarea, eficacitatea produselor competitoare
- Costurile și timpul pentru R&D (Cercetare și dezvoltare): acceptarea noilor dovezi științifice, costurile pentru dezvoltare, costurile/durata studiilor clinice – inclusiv dificultăți privind recrutarea
- Potențialul câștig: prețul de rambursare, modelul de plată
- Exclusivitatea pe piață: timpul până la intrarea pe piață, protecția drepturilor de proprietate intelectuală, tabloul competitiv
Cinci studii de caz, asupra a cinci boli, sunt prezentate în raport: mielom multiplu, hemofilie, neoplasme ale celulelor germinale, tratamente anti-virale și boala Alzheimer.
Mielomul multiplu (incidența de 4,5-6 la 100.000 loc./an în EU)
Evaluat în funcție de conceptul propus în raport, MM reprezintă una dintre bolile în care s-au înregistrat progrese importante în accesul la medicamente orfane. Deși este un cancer rar al celulelor plasmatice din măduva osoasă și afectează pacienți cu o vârstă mediană de diagnostic de 72 de ani, datorită noilor opțiuni terapeutice, supraviețuirea s-a îmbunătățit semnificativ în ultimii ani.
Un facilitator notabil a fost aprobarea de medicamente vechi în indicații noi (drug repurposing). Dezvoltările în MM au fost, de asemenea, facilitate de îmbunătățiri semnificative în înțelegerea științei din spatele bolii, cum ar fi o înțelegere mai profundă a fiziopatologiei mielomului multiplu. Nu în ultimul rând, terapiile în MM au beneficiat de un process flexibil de reglementare, trialuri clinice cu design inovator, permițând autorităților să ofere aprobări pe baza unor studii cu un număr de participanți redus.
Hemofilia A și B
- Prevalență Hem. A în UE: aprox. 0,7 la 100.000 loc.
- Prevalență Hem. B în UE: aprox. 0,2 la 100.000 loc.
Hemofilia este o boală rară genetică, ereditară, caracterizată de deficiențe la nivelul factorilor de coagulare VIII și IX. Aproximativ 90% dintre persoanele cu hemofilie severă au afectare cronică severă care implică cel puțin o articulație principală, până la 30 de ani.
Datorită progreselor făcute în medicina moleculară, care a revelat mecanismele genetice ale bolii, tot mai multe tratamente apar în ultimele decenii pentru această boală. Terapia genică în hemofilie aduce promisiunea administrării unui singur tratament, o singură dată în viață, însă aprobarea unei astfel de terapii este încă provocatoare. În ciuda progreselor, FDA a amânat aprobarea terapiei genice pentru hemofilie, motivând insuficiența datelor. În același timp, eficiența terapiilor profilactice deja aprobate scade șansa ca autoritățile să susțină un tratament cu un cost singular mult mai ridicat, cum ar fi terapia genică, deși beneficiile pe termen lung sunt majore.

Neoplasmele de la nivelul celulelor germinale
Neoplasmele cu celule germinale (GCN), cunoscute și sub numele de tumori de celule germinale gonadale sunt cancere care se formează în ovare sau testicule. Acest tip de cancer reprezintă între 2 și 4% din totalul cancerelor care apar înainte de vârsta de 20 de ani.
Tratamentele actuale pentru NCG includ intervenții chirurgicale pentru îndepărtarea tumorii, radioterapie și terapii combinate medicamentoase. Neoplasme de celule germinale au fost caracterizate în 2015 ca fiind un „punct alb de dezvoltare”, fără niciun tratament medicamentos eficient și nici dezvoltare clinică de noi produse farmaceutice. De la identificarea din 2015, a existat o activitate semnificativă în cercetare, iar la momentul actual, între 29 și 57 de studii se află în desfășurare. Două bariere foarte importante în dezvoltare și cercetare țin de caracteristicile bolii, care se dezvoltă în uter și este latentă până după naștere, dar și de heterogenitatea și vârsta pacienților, îngreunând studiile și punând bariere etice.
Soluția în cazul acestei clase de neoplasme vine din rândul studiilor pentru terapiile tumor-agnostic, care permit înrolarea unor grupuri diverse de pacienți, cu neoplasme diferite. De asemenea, statutul de medicament orfan a jucat un rol important în accelerarea cercetării.
Tratamentele antivirale
În ciuda impactului substanțial al infecțiilor virale asupra sănătății (inclusiv COVID-19 acum), dezvoltarea medicamentelor antivirale a fost limitată. Acest lucru este similar cu ceea ce s-a văzut în „paradoxul antibioticului”: un dezechilibru între povara bolilor infecțioase și ritmul lent (și în scădere) al inovației în acest domeniu. Există medicamente antivirale disponibile doar pentru 10 din mai mult de 220 de virusuri despre care se știe că infectează în prezent oamenii. Dintre cele 90 de medicamente antivirale dezvoltate între 1959 și 2016, aproape jumătate sunt aprobate pentru o singură boală – HIV.
Numărul mare de medicamente HIV, dezvoltate într-o perioadă relativ scurtă, a transformat HIV / SIDA de la un diagnostic terminal la o afecțiune cronică și demonstrează potențialul științei farmaceutice de a găsi soluții pentru problemele de sănătate publică.
Boala Alzheimer
Această afecțiune nu este nici rară, nici pediatrică, dar ilustrează perfect provocările dezvoltării chiar și acolo unde potențialul comercial din punct de vedere al dimensiunii populației de pacienți și valoarea prevenirii sau inversării declinului cognitiv, ar sugera că orice produs de succes ar deveni rapid un „blockbuster” comercial. BA este prezentat ca un caz contrastant, care evidențiază multe dintre provocările observate în jurul dezvoltării de medicamente pentru bolile rare sau pediatrice.
Motivele ratei scăzute de succes în BA sunt multifactoriale. În primul rând, știința BA este extrem de complexă și există ipoteze multiple ale cauzelor și mecanismului de acțiune. Între 2002 și 2014, au existat 413 studii clinice pentru BA. 99.6% dintre acestea au eșuat.
Recomandări
Studiile de caz individuale evidențiază lecții importante. În primul rând, după cum este ilustrat în Cazul Alzheimer, potențialul comercial în sine nu este suficient pentru a garanta succesul. Știința din jurul bolii Alzheimer este complexă și acest obstacol fundamental a fost exacerbat prin provocări în jurul măsurării obiectivelor finale din studii și recrutarea participanților pentru studii clinice. Similar, provocări au fost observate în jurul neoplasmelor celulelor germinale, care se dezvoltă încă din etapa de dezvoltare intrauterină.
Recenta aprobare accelerată a aducanumab, totuși, demonstrează cum autoritățile de reglementare pot promova dezvoltarea continuă printr-o raportare pragmatică la obiectivele finale ale studiilor clinice. Dezvoltările tehnologice în imagistica creierului și biomarkerii pot ajuta la abordarea unor ținte subiective în BA, dar flexibilitatea de reglementare în ceea ce privește design-ul studiilor, inclusiv creșterea acceptabilității pentru obiectivele surogat, dovezile din lumea reală și pentru brațele de control „sintetice” pot ajuta la reducerea costului și a duratei studiilor, promovând eforturile de cercetare-dezvoltare.
Valoarea potențială a dezvoltărilor din BA, hemofilie și antivirale cu acțiune directă, la fel ca în multe alte afecțiuni rare și pediatrice, prezintă o provocare pentru cadrele și conceptele valorice existente. Mulți plătitori acordă prioritate bugetelor peste valoarea pacientului în rambursarea acestor medicamente revoluționare.
Modele inovatoare de rambursare, în special prețurile bazate pe indicații, ar putea să fie utile în stimularea dezvoltării produselor cu indicații multiple sau agnostic-tumorale pentru boli rare și ultra-rare, în cazul în care o singură indicație poate să nu ofere suficiente stimulente economice pentru dezvoltare.
În cele din urmă, o temă consistentă în toate cazurile a fost importanța flexibilității și a pragmatismului proceselor de reglementare. Acest lucru poate reduce timpul pentru accesul pe piață, costurile studiilor clinice, și incertitudinea în jurul probabilității de aprobare în diferite etape de dezvoltare.
Citește și:
- RAPORT. „Every day Counts”: Impactul COVID-19 asupra accesului la servicii medicale oncologice în UE
- Raportul „Access to Personalised Oncology in Europe”: oncologia personalizată, esențială pentru dezvoltarea politicilor de sănătate din Europa
- Raportul „Unlocking the potential of precision medicine in Europe”: accesul redus la testarea biomarkerilor în UE limitează implementarea medicinei de precizie în oncologie. Care este situația României?

