Cilta-cel, a doua terapie celulară CAR-T anti-BCMA pentru mielomul multiplu, aproape de aprobare condiționată în UE
În cadrul întâlnirii de la finalul lunii martie, Comitetul pentru produse medicamentoase de uz uman (CHMP) din cadrul EMA a emis recomandarea de aprobare condiționată pentru terapia celulară CAR-T, ciltacabtagene autoleucel (denumire comercială Carvykti), cu indicație în tratamentul pacienților adulți cu mielom multiplu recidivat și refractar, care au primit cel puțin trei linii terapeutice anterioare și al căror cancer s-a agravat de la ultimul tratament.
Odată aprobată, Cilta-cel va deveni a doua terapie CAR-T pentru mielomul multiplu care a primit o autorizație condiționată de punere pe piață în UE. Prima terapie, Abecma (idecabtagene vicleucel), a fost aprobată condiționat în august 2021. Asistăm așadar la un ritm accelerat de aprobare a terapiilor celulare CAR-T, considerate a fi cel mai înalt grad de personalizare terapeutică disponibil în practică.
Evaluarea CHMP s-a bazat pe raportul oferit de Comitetul pentru Terapii Avansate – comitetul de experți al EMA pentru terapii celulare și genetice. La fel ca majoritatea terapiilor celulare și genice, Cilta-cel a fost inclusă în schema PRIME a EMA.
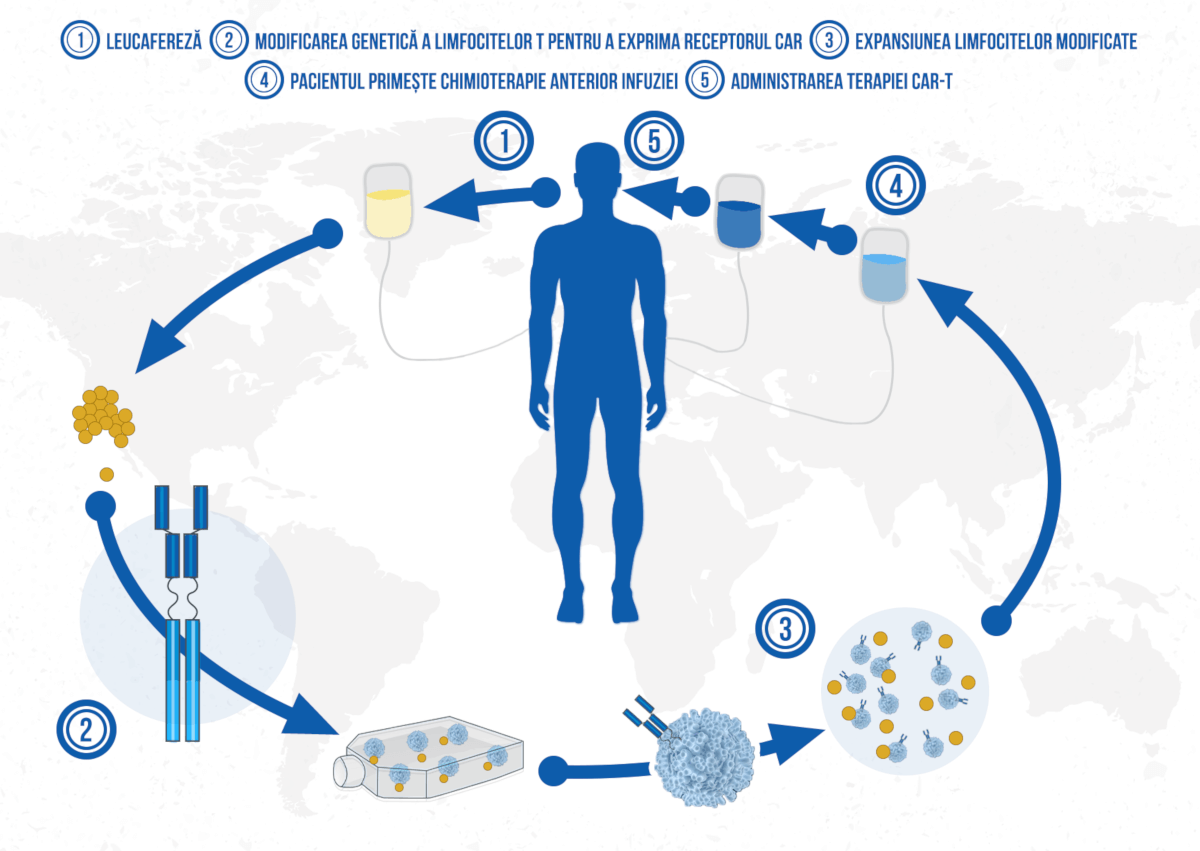
Principiul de acțiune al CAR-T (chimeric antigen receptor) îi permite să fie adaptat pentru diferite tipuri tumorale, țintind diferiți markeri de la suprafața celulelor maligne. Dacă CD19, antigenul exprimat mai ales pe suprafața limfocitelor B, a reprezentat o țintă importantă pentru primele terapii CAR-T (precum Kymriah și Yescarta), Cilta-cel este o terapie CAR-T anti-BCMA (antigenul specific limfocitelor B mature), exprimat mai ales de către celulele plasmatice normale și maligne, precum și de unele celule B mature.
Mai multe detalii despre aceste terapii, în următorul articol: Terapiile celulare CAR-T anti-BCMA pentru mielomul multiplu
Mielomul multiplu
Mielomul multiplu este un cancer rar al celulelor plasmatice, un tip de globule albe din sânge (leucocite), care produc anticorpi și se găsesc în măduva osoasă. În mielomul multiplu, proliferarea celulelor plasmatice este scăpată de sub control, ceea ce duce la multiplicarea celulelor plasmatice anormale, imature. Când celulele plasmatice devin canceroase, ele nu mai protejează organismul de infecții și produc proteine anormale care pot cauza probleme care afectează rinichii, oasele sau sângele. Deși este un cancer rar, mielomul multiplu (MM) este unul dintre cele mai frecvente cancere hematologice la adulți.
În ciuda dezvoltării și aprobării unei game de noi medicamente pentru tratamentul mielomului multiplu în ultimii ani, există opțiuni terapeutice limitate pentru pacienții care au primit deja trei clase majore de medicamente (agenți imunomodulatori, inhibitori de proteazom și anticorpi monoclonali) și a căror boală a revenit sau nu mai răspunde la aceste medicamente.
Studiul clinic pe care se bazează recomandarea
Studiul principal pe care se bazează recomandarea este un studiu clinic multicentric, deschis, cu un singur braț – CARTITUDE. Studiul a investigat eficacitatea și siguranța ciltacabtagen-autoleucel la 113 pacienți adulți cu mielom multiplu recidivat și refractar care au primit cel puțin trei terapii anterioare, inclusiv un agent imunomodulator, un inhibitor de proteazom și un anticorp anti-CD38, și care nu au răspuns la ultimul regim de tratament. Aproximativ 84% dintre pacienții înscriși în studiu au prezentat un răspuns durabil la tratament (o perioadă fără semne sau simptome de boală după tratament). Aproximativ 69% au prezentat un răspuns complet, fără semne de cancer detectabile după primirea terapiei.
La fel ca în cazul tuturor terapiilor CAR-T aprobate până acum, cel mai frecvent efect secundar este sindromul de eliberare de citokine (CRS) – un răspuns sistemic al organismului persoanei la activarea și proliferarea celulelor CAR-T.
Citește și:
- #ASCO20. Studiu KarMMa. Ide-cel, terapia celulară anti-BCMA, arată o rată generală de răspuns de 73% pentru pacienții cu mielom multiplu care nu mai au alte opțiuni de tratament
- FDA aprobă prima terapie celulară anti-BCMA pentru pacienții cu mielom multiplu recidivat și refractar la cel puțin patru terapii anterioare
- Ce este mielomul multiplu?

