Anul 2023 din perspectiva accesului pacienţilor la terapii inovatoare în Uniunea Europeană. Care sunt medicamentele aprobate în al doilea trimestru de EMA
La finalul anului 2023, raportuldegarda.ro vă prezintă principalele progrese înregistrate în domeniul medicamentelor în Uniunea Europeană (UE) în ultimele 12 luni, cele mai inovatoare terapii care au devenit disponibile sau au primit aviz pozitiv pentru aprobare în UE, precum și rezultatele studiilor care au constituit baza autorizării pentru comercializare.
Cele mai importante realizări din al doilea trimestru al anului 2023:
- a fost aprobat primul vaccin pentru profilaxia infecțiilor cu virusul respirator sincițial la adulții de minim 60 de ani
- primul medicament pentru repigmentare adresat pacienților cu vitiligo non-segmental cu afectare facială a fost aprobat
- au fost extinse indicațiile terapiei CAR-T Breyanzi pentru o serie de tipuri de limfom cu celulă B mare refractare sau recidivante
- a fost aprobat primul inhibitor alosteric și reversibil al miozinei cardiace în Uniunea Europeană și primul inhibitor al miozinei cardiace care țintește fiziopatologia cardiomiopatiei hipertrofice obstructive

Cu ce noutăți a venit luna aprilie 2023?
Primul medicament pentru repigmentare adresat pacienților cu vitiligo non-segmental a fost aprobat în aprilie de către Comisia Europeană. Opzelura (ruloxitinib) este indicat adulților și adolescenților în vârstă de minim 12 ani cu vitiligo non-segmental cu afectare facială. Este un medicament sub formă de cremă, care conține ruloxitinib, inhibitorul selectiv al kinazelor Janus (JAK) 1 și 2.
Eficacitatea Opzelura a fost confirmată în cadrul studiilor de fază III TRuE-V1 și TRuE-V2, care au inclus peste 600 de persoane. După 24 de săptămâni de terapie, aproximativ 30% dintre participanții la studiu au prezentat o îmbunătățire de minim 75% a leziunilor faciale, conform scorului F-VASI (facial Vitiligo Area Scoring Index). După 52 de săptămâni, procentul acestora a crescut la aproximativ 50%.
O șansă pentru pacienții cu cancer prostatic metastatic rezistent la castrare
Comisia Europeană a autorizat comercializarea Akeega (niraparib/abiraterone acetat), administrat împreună cu prednison sau prednisolon, pentru tratamentul adulților cu cancer de prostată metastatic rezistent la castrare (mCRPC), cu mutații BRCA 1/2 (germinale sau somatice), la care chimioterapia nu este indicată.
Conform rezultatelor studiului clinic de fază III MAGNITUDE, noua terapie a îmbunătățit semnificativ supraviețuirea în absența progresiei bolii, stabilită radiologic (rPFS), în special la pacienții cu mutații ale genelor BRCA 1/2, la care riscul a fost redus cu aproape 50%. Mediana rPFS a fost aproape dublă la pacienții care au primit Akeega, în comparație cu grupul de control.
Akeega conține niraparib, inhibitor selectiv al PARP (poly ADP ribose polymerase), precum și abiraterone acetat, un inhibitor androgenic de biosinteză. În luna aprilie 2023, Comisia Europeană a acordat acestei noi terapii prima aprobare de comercializare la nivel mondial.
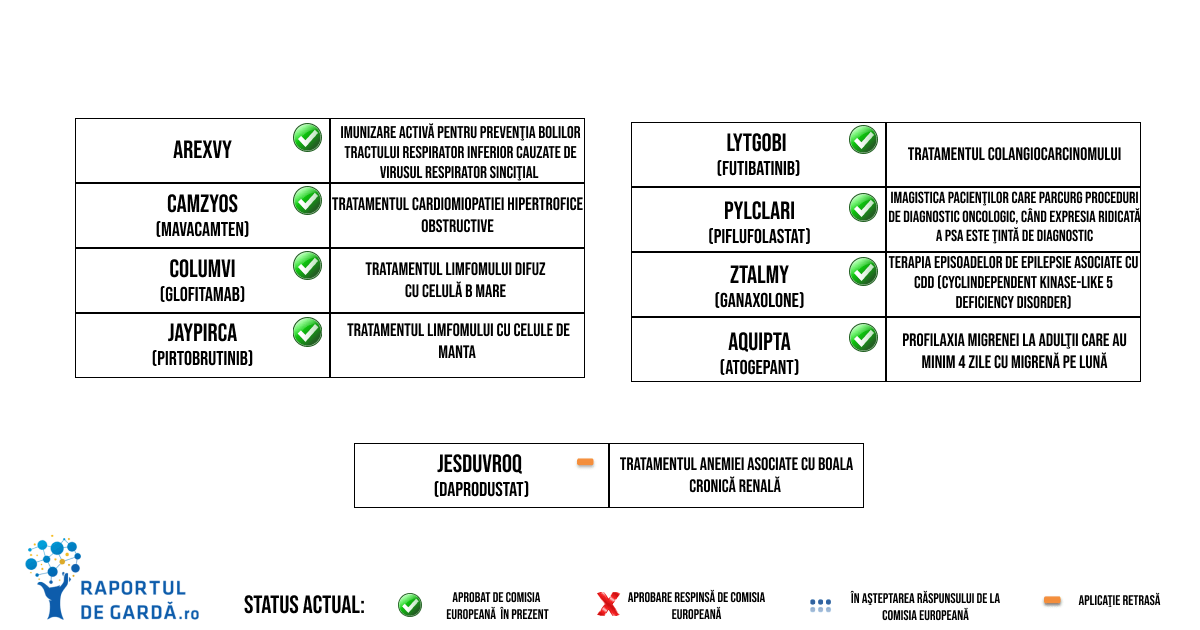
În luna aprilie, au obținut aviz pozitiv din partea CHMP următoarele medicamente: Arexvy, Camzyos (mavacamten), Columvi (glofitamab), Jaypirca (pirtobrutinib), Lytgobi (futibatinib). Detalii despre întâlnirea lunară CHMP din aprilie aici.
Principalele realizări care au avut loc în luna mai 2023
Comisia Europeană a aprobat Breyanzi (lisocabtagene maraleucel; liso-cel) pentru tratamentul adulţilor cu limfom difuz cu celulă B mare (DLBCL), limfom cu celulă B de grad înalt (HGBCL), limfom primar mediastinal cu celulă B mare (PMBCL) şi limfom folicular de grad 3B (FL3B), care au boală refractară sau care a recidivat în 12 luni de la completarea regimului de chimioimunoterapie de primă linie.
Rezultatele studiului clinic de fază III TRANSFORM se află la baza acestei noi aprobări. După 6 luni de urmărire, supraviețuirea mediană în urma administrării Breyanzi a fost de peste 4 ori mai crescută în comparație cu terapiile standard. Rata de supraviețuire în absența progresiei bolii a fost de peste 2,5 ori mai ridicată la persoanele care au primit terapia CAR-T.
De asemenea, două noi medicamente, Pylclari (piflufolastat) și Ztalmy (ganaxolone), au primit aviz pozitiv din partea CHMP în cadrul întâlnirii din luna mai 2023. Detalii despre întâlnirea lunară CHMP din mai aici.
Ce noutăți au marcat luna iunie 2023?
În luna aprilie, CHMP (Committee for Medicinal Products for Human Use) din cadrul EMA (European Medicines Agency) a recomandat aprobarea comercializării în Uniunea Europeană a vaccinului Arexvy pentru profilaxia bolilor tractului respirator inferior cauzate de virusul respirator sincițial (RSV). Acesta este primul vaccin pentru imunizarea activă a adulților cu vârste de minim 60 de ani împotriva RSV. Noul vaccin a fost autorizat de Comisia Europeană în iunie, devenind disponibil în statele membre ale Uniunii Europene și Spațiul Economic European.
Arexvy conține o versiune modificată a glicoproteinei de suprafață pentru fuziune a RSV, care este esențială pentru capacitatea de infectare și care reprezintă ținta principală a anticorpilor produși împotriva acestui virus în cursul infecției. La baza avizului pozitiv se află rezultate studiului clinic randomizat care a cuprins 25 000 de adulți din 17 state. Imunizarea cu Arexvy a asigurat un nivel de protecție de 83% pentru minim 6 luni post-vaccinare.

Comisia Europeană a aprobat Camzyos (mavacamten) pentru tratamentul cardiomiopatiei hipertrofice obstructive simptomatice la pacienții adulți. Acesta este primul inhibitor alosteric și reversibil al miozinei cardiace aprobat în Uniunea Europeană și primul inhibitor al miozinei cardiace care țintește fiziopatologia cardiomiopatiei hipertrofice obstructive. Eficacitatea și siguranța Camzyos au fost demonstrate în cadrul studiilor de fază III EXPLORER-HCM și VALOR-HCM.
În cadrul întâlnirii CHMP din luna iunie 2023, două noi medicamente au fost recomandate pentru aprobare: Aquipta (atogepant) și Jesduvroq (daprodustat). Detalii despre întâlnirea lunară CHMP din iunie aici.
Despre cum are loc autorizarea medicamentelor în Uniunea Europeană și ce categorii de terapii există poți afla citind primul articol din seria Anul 2023 din perspectiva accesului pacienţilor la inovaţie în medicină în Uniunea Europeană.
Citește și:
- Transparența, principiu fundamental în activitatea EMA: Curtea de Justiție Europeană confirmă dreptul de acces la informațiile pe care se bazează aprobarea unui medicament în UE
- EMA publică, în premieră, o listă cu subiecte de cercetare în domeniul reglementării medicamentelor, cu scopul de a facilita accesul la inovație în UE
- Comisia Europeană permite restricții asupra comerțului paralel cu medicamente, dacă acestea servesc interesului public

