Raport FDA: 39% dintre medicamentele aprobate în 2020 au fost terapii personalizate
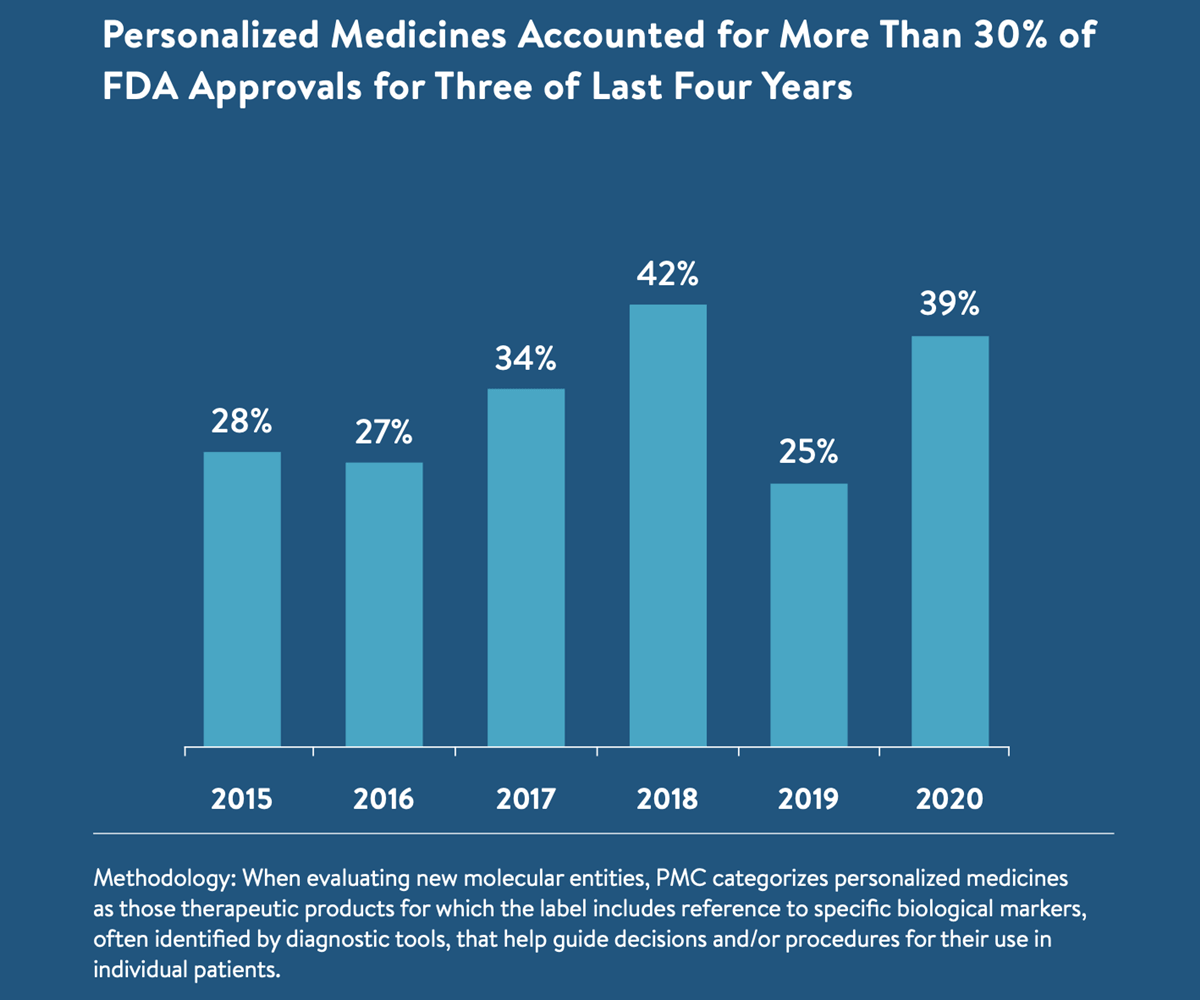
Anul trecut, FDA a aprobat 19 terapii personalizate, o imunoterapie celulară și 8 noi indicații de diagnostic, care vor ajuta medicii să aloce tratamente țintite pacienților care pot beneficia de ele. Terapiile personalizate au reprezentat 39% din medicamentele nou-aprobate anul trecut de FDA, reprezentând o treime din medicamentele aprobate pentru a treia oară în ultimii patru ani. Aceasta reprezintă o creștere semnificativă față de acum un deceniu, când medicamentele personalizate reprezentau mai puțin de 10% din noile terapii aprobate în fiecare an.
În acest sens, Coaliția pentru Medicina Personalizată (PMC) a lansat un raport care accentuează schimbarea de paradigmă a sistemului american de sănătate către era medicinei personalizate într-un mod eficient, inclusiv în contextul pandemiei COVID-19. În plus, demonstrează implicarea continuă a companiilor biofarmaceutice și a industriei de diagnostic în aria medicinei personalizate. Raportul Medicina personalizată în cadrul FDA: Scopul și semnificația progresului din 2020 descrie modul în care testele și terapiile recent aprobate vor ajuta la transformarea îngrijirii subseturilor de pacienți cu cancer, boli rare, dar și boli comune sau infecțioase.
Realizările FDA în domeniul medicinei personalizate în 2020
- Aprobarea a 19 terapii personalizate care reprezintă aproximativ 39% din toate entitățile moleculare terapeutice nou aprobate. Medicamentele personalizate au reprezentat peste o treime din aprobările de medicamente noi în trei din ultimii patru ani.
- Aprobarea primei imunoterapii CAR-T (Tecartus) pentru pacienții cu limfom cu celule de manta, refractar la tratamentele anterioare. Această aprobare extinde frontierele tratamentului CAR-T, care oferă o promisiune extraordinară pentru îmbunătățirea managementului cancerului.
- Lansarea a șapte documente cu îndrumări privind producția și dezvoltarea clinică a produselor terapeutice genetice și celulare. Aceste documente îndrumătoare vor ajuta la eficientizarea dezvoltării terapiilor potențial curative.
- Autorizarea sau aprobarea a opt noi indicații ale testelor de diagnostic care pot informa deciziile terapeutice în mod țintit, inclusiv aprobarea primelor două indicații tumor-agnostic pentru identificarea pacienților cu tumori solide de toate tipurile care au fuziuni ale genelor NTRK sau încărcătură mutațională înaltă (TMB-H), în stadii avansate. Aprobările indicațiilor NTRK și TMB-H extind frontierele tratamentului tumor-agnostic, care se concentrează pe utilizarea biomarkerilor ca bază pentru deciziile terapeutice, spre deosebire de clasificarea pe baza localizării tumorii.
- Aprobarea unei noi terapii pe baza interferenței ARN (Oxlumo, lumasiran), care oferă pacienților cu hiperoxalurie primară de tip 1 (PH1) primul tratament care abordează cauza principală a bolii (o tulburare metabolică genetică rară care determină insuficiență renală progresivă și poate duce la deteriorarea altor organe).
- Aprobarea primului test NGS (secvențiere de nouă generație) tip biopsie lichidă pan-tumorală, ca test diagnostic complementar pentru detecția mai multor biomarkeri din ADN-ul izolat din plasmă. Acest test permite detecția biomarkerilor în sângele pacienților, înlăturând necesitatea biopsiilor tisulare mai invazive la anumite grupuri de pacienți.
Impact: șapte dintre tratamentele personalizate aprobate abordează cauzele bolilor rare; unul este un antiretroviral de primă clasă pentru pacienții cu HIV, altele oferă noi opțiuni pentru pacienții cu cancer
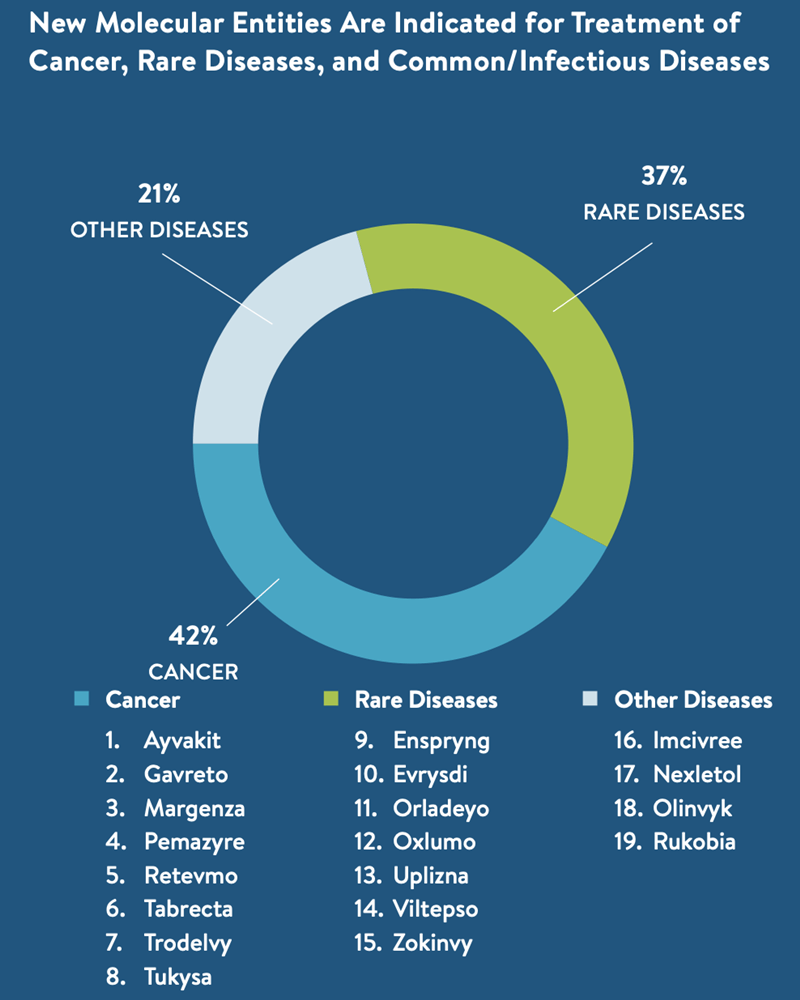
Șapte dintre cele 19 entități moleculare nou aprobate sunt concepute pentru a contracara cauzele principale ale anumitor boli genetice rare, care nu au mai fost adresate anterior. Mulți pacienți cu tulburare a spectrului de neuromielită optică (NMOSD), atrofie musculară spinală (AMS), distrofie musculară Duchenne, progeria, deficit de pro-opiomelanocortină (POMC) și hiperoxalurie primară beneficiază acum de tratamente disponibile, care vizează mecanismele moleculare de bază ale afecțiunilor în cauză.
Aprobarea Rukobia (fostemsavir) oferă o terapie de primă linie pentru pacienții cu HIV care nu pot gestiona boala cu medicamentele antiretrovirale disponibile din cauza rezistenței, intoleranței sau considerentelor de siguranță.
Nouă dintre cele 20 de tratamente personalizate recent aprobate și peste 20 de indicații recent aprobate pentru medicamentele personalizate existente deja oferă noi opțiuni de tratament pentru pacienții cu cancer. Aceste tratamente pot îmbunătăți semnificativ perspectivele pentru mulți pacienți, reducând progresia bolii și extinzând supraviețuirea. Aprobarea Pemazyre (pemigatinib) marchează primul tratament țintit pentru pacienții cu colangiocarcinom. Keytruda (pembrolizumab), aprobat inițial pentru pacienții cu cancer pulmonar cu celule mici, avansat, a fost aprobat în 2020 pentru o nouă indicație tissue-agnostic. Acum, pacienții cu tumori solide metastatice TMB-H, care sunt de obicei identificate prin testare genomică, pot beneficia de Keytruda ca a doua linie de tratament.
Citește și:
- Indicele European de Medicină Personalizată: România, locul 32 din 34. Deficiențe în infrastructura digitală din sănătate și investiții scăzute în cercetare și dezvoltare
- Raport IHE. Progrese în diagnosticul cancerului: cum au schimbat testarea genomică și biomarkerii standardul european?

