Noile generații de terapii CAR-T: cele mai importante studii prezentate la ASH 2019
Terapia genică, celulară și imunoterapia CAR-T a reprezentat un punct de turnură în înțelegerea și tratarea cancerului, cu rezultate pozitive durabile în cazul unor pacienți care nu mai aveau alte opțiuni terapeutice. Cele două terapii aprobate în 2017 în SUA și în 2018 în UE, Kymriah și Yescarta, sunt deja utilizate în mai multe sisteme de sănătate din lume. În cadrul Congresului Societății Americane de Hematologie ASH 2019, au fost prezentate mai multe detalii despre provocările CAR-T în practica reală, care confirmă siguranța și eficacitatea acestora.
Confirmarea Yescarta și Kymriah în practica medicală curentă
Kymriah este aprobat pentru tratamentul a două tipuri de cancere hematologice: leucemia limfoblastică acută cu precursori de celule B (LAL) și limfomul cu celule B mari difuz (DLBCL). Studiile prezentate la ASH 2019 au confirmat datele din studiile JULIET și ELIANA, care au condus la aprobarea inițială.
Datele prezentate la ASH 2019 au descris o rata generală de răspuns de 58% în cazul DLBCL refractar sau recidivant, și o rată de 40% de răspuns complet. În cadrul studiului JULIET, rata generală de răspuns a fost de 52%, iar 38% au obținut răspunsuri complete.
Sursa foto: novartis.gcs-web.com
În ceea ce privește LAL, datele post-marketing au demonstrat o rată de răspuns complet de 85%, față de rata de 82% din studiul ELIANA.
Profilul de siguranță a fost similar, iar în cazul LAL, superior, în studiile post-marketing. Pentru pacienții cu DLBCL care au prezentat sindrom de eliberare de citokine (reacție adversă specifică terapiilor CAR-T) s-a administrat tocilizumab la 20% dintre pacienți și corticosteroizi la 4% dintre pacienți.
În studiul JULIET, 27% și, respectiv, 19% dintre pacienți au primit aceste tratamente. În cazul LAL, sindromul de eliberare de citokine de grad 3 sau mai mare a apărut la 14% dintre pacienți iar reacțiile adverse neurologice la 8%. În cazul studiului ELIANA, proporțiile au fost de 48% și, respectiv, 13%.
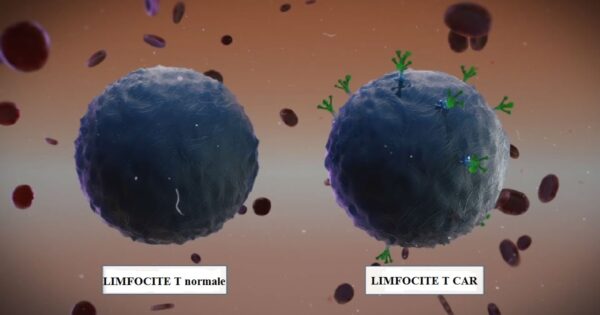
Sursa foto: Associated Press
În cazul Yescarta, au fost analizați pacienții cu DLBCL din studiul ZUMA-1, pe baza căruia a fost acordată aprobarea, la 3 ani de la administrarea tratamentului. Supraviețuirea globală pentru pacienții cu limfom difuz cu celula mare tip B, refractar, a fost de 47%, tratamentul prelungind supraviețuirea pacienților cu 25.8 luni. Această supraviețuire este conformă cu rezultatele obținute la 2 ani de la tratament, de 51% supraviețuire globală.
Terapiile CAR-T, sigure în cadrul grupelor de vârstă extreme
Datele din viața reală prezentate în cadrul ASH 2019 sugerează că terapiile CAR-T sunt sigure pentru o gamă mai largă de pacienți față de cohortele din cadrul studiilor clinice: este vorba despre copii și vârstnici.
Studiile PLAT-02 și PLAT-05 au implicat administrarea terapiei CAR-T la 18 copii cu o vârstă medie de 20 de luni, care au fost diagnosticați cu leucemie acută limfoblastică înainte de vârsta de 1 an. Din cei 16 pacienți la care s-a înregistrat răspuns terapeutic, 71,4% au rămas în remisiune la 1 an iar supraviețuirea globală a fost de 73,3%. Copiii mici au tolerat bine terapia CAR-T, similar celor mari și adolescenților. Toxicitatea a fost considerată acceptabilă. Doi pacienți au prezentat sindrom de eliberare a citokinelor de grad maxim 3.

Sursa foto American Society of Hematology
În ceea ce privește vârstnicii, provocarea este reprezentată de multiplele comorbidități, care complică prognosticul. În cadrul studiului prezentat la ASH 2019, au fost identificați 207 pacienți cu o vârstă medie de 70 de ani care au primit terapia celulare CAR-T pentru DLBCL. Aproximativ jumătate dintre aceștia era incluși în studii clinice, în timp ce restul au avut comorbidități care probabil le-ar fi blocat accesul în studiile clinice cu terapia celulară CAR-T. Datele colectate prin sistemul de asigurări medicale din SUA au arătat că aproape trei sferturi dintre pacienți au rămas în viață la 6 luni după tratament. În plus, terapia CAR-T a condus la un număr mai mic de internări în perioada post-infuzie, ceea ce a scăzut costul general al asistenței medicale cu 39%.

Noi tipuri de celule imunitare modificate
Metoda de modificare și adaptare a celulelor imunitare proprii pacientului poate fi aplicată și în cazul altor celule, în afară de limfocitele T. Două studii prezentate în cadrul ASH 2019 au propus soluții pentru producția și distribuția complexă a CAR-T și pentru situațiile de recădere precoce.
Un studiu preclinic propune modificarea unei celule care, spre deosebire de limfocitul T, face parte din apărarea înnăscută a organismului: NK (natural killer cells). Aceasta poate fi modificată pentru a exprima mai mulți markeri tumorali (CD19, CD16, IL15). Celulele CAR-NK ar putea reprezenta o alternativă off-the-shelf pentru celulele CAR-T, care necesită preluarea și modificarea celulelor fiecărui pacient în parte.

Sursă foto: ASH/Scott Morgan 2019
O altă celulă, rezultată din modificarea celulelor pacientului, este T-APC (limfocit T, prezentator de antigene), care a demonstrat în studiul PLAT-03 capacitatea de a stimula celulele CAR-T să persiste în sânge, să mențină un răspuns imunitar susținut și să prelungească remisiunea. Acest demers se datorează observației că, în ciuda răspunsului terapeutic rapid și spectaculos, o parte din pacienți prezintă recăderi în urma terapiilor CAR-T. Astfel, în cadrul studiului, 12 pacienți cu LAL au beneficiat de un rapel de celule T-APC, în urma infuziei CAR-T. Acest protocol a condus la o rată medie de supraviețuire fără urme de boală la 1 an de 71%.
Noi ținte, noi cancere: CAR-T în mielomul multiplu
Cele două terapii CAR-T aprobate, Yescarta și Kymriah, utilizează aceeași țintă moleculară: CD19, de pe suprafața celulelor tumorale. Însă principiul de acțiune al CAR-T îi permite să fie adaptat pentru diferite tipuri tumorale, cu diferiți markeri de suprafață. În cadrul ASH 2019, au fost prezentate rezultate favorabile în cazul mielomului multiplu, țintind unul sau chiar doi markeri tumorali.

Sursa foto © ASH/Scott Morgan 2019
Cel mai frecvent studiat marker de suprafață în cazul mielomului multiplu este BCMA. Studiul de fază Ib CARTITUDE-1 a inclus adulți diagnosticați cu mielom multiplu, care erau refractari sau rezistenți la minim 3 linii terapeutice anterioare. Astfel, au fost selectați 25 de pacienți, care au primit o infuzie de celule CAR-T. Dimensiunile tumorii au scăzut la toți cei 21 de pacienții care au fost evaluați, iar în total, rata de răspuns a fost de 91%.

Pentru a asigura o eficiență crescută a terapiilor CAR-T, studiile noi propun utilizarea a două ținte moleculare simultan. Această strategie a fost aplicată în cazul mielomului multiplu, care prezintă frecvent markerii BCMA și CD38. Rezultatele obținute în faza I au fost promițătoare: 87.5% dintre pacienți au prezentat răspuns la tratament, iar dintre aceștia 50% au obținut răspuns complet.
Terapiile CAR-T au reprezentat o schimbare de paradigmă la momentul apariției, și sunt în continuare una dintre cele mai importante inovații în oncologie. Însă, există în continuare o serie de provocări: metoda complexă de producție și distribuție, recidiva precoce, utilizarea de noi ținte moleculare pentru noi tipuri tumorale și utilizarea CAR-T în tumorile solide.
Citește și:
- State of Innovation 2019. Terapiile celulare CAR-T: momentul actual și direcții viitoare
- Terapiile CAR-T, eficiente și în cazul tumorilor solide: primele rezultate pozitive în studii de faza I
- Topul inovațiilor în medicină #RaportuldeGardă 2018. Publicul și editorii au decis: terapiile CAR-T, marele câștigător

